Veresterung
Carbonsäure-Ester sind Verbindungen R-CO-O-R', die sich formal aus einer Carbonsäure R-COOH und einem Alkohol R'-OH zusammensetzen.
Synthese
Gebildet werden Ester durch Kondensation einer Carbonsäure mit einem Alkohol:
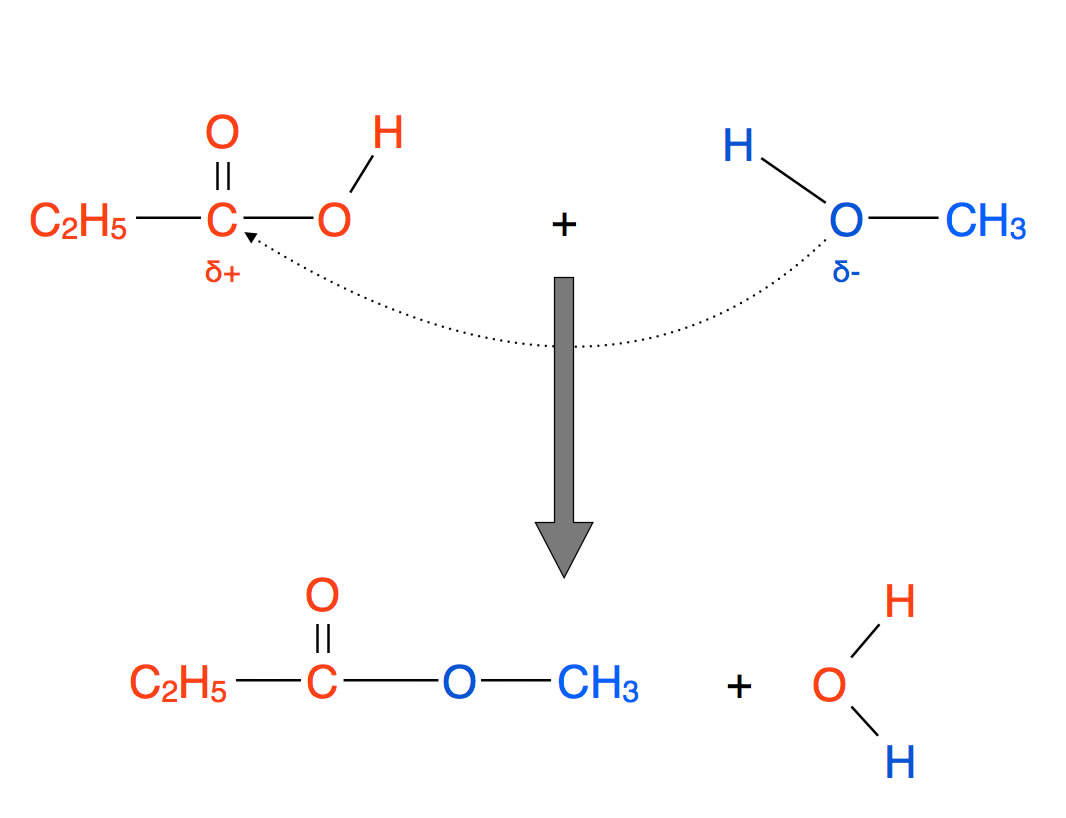
Bildung eines Esters aus Propionsäure und Methanol
Autor: Ulrich Helmich 2022, Lizenz: Public domain.
Andere Synthese-Möglichkeiten sind die Reaktion eines Carbonsäure-Chlorids mit einem Alkohol unter Freisetzung von HCl (statt H2O) oder die Umsetzung eines Carbonsäure-Anhydrids mit zwei Molekülen Alkohol unter Freisetzung von zwei Molekülen H2O.
Führt man die Veresterung von Essigsäure mit Ethanol ohne Zusatz einer Säure durch, so läuft die Reaktion extrem langsam ab. Bis zur Einstellung eines chemischen Gleichgewichts können Monate bis Jahre vergehen. Durch Zusatz weniger Tropfen Schwefelsäure kann man diesen Vorgang aber erheblich beschleunigen. Schauen wir uns den Mechanismus der säurekatalysierten Veresterung jetzt einmal etwas näher an.
Die säurekatalysierte Veresterung läuft nach dem A/E-Mechanismus ab
Um deutlich zu machen, dass diese Reaktion tatsächlich nach dem A/E-Mechanismus abläuft, habe ich einfach die Graphik, die ich für den säurekatalysierten A/E-Mechanismus erstellt habe, so abgewandelt, dass sie die säurekatalysierte Esterbildung aus einer Carbonsäure und einem Alkohol zeigt. Eine etwas übersichtlichere und für Schüler(innen) der Sek. II geeignetere Darstellung finden Sie auf der Seite zur säurekatalysierten Esterbildung in der Chemie-Abteilung für die Sek. II.
Schritt 1
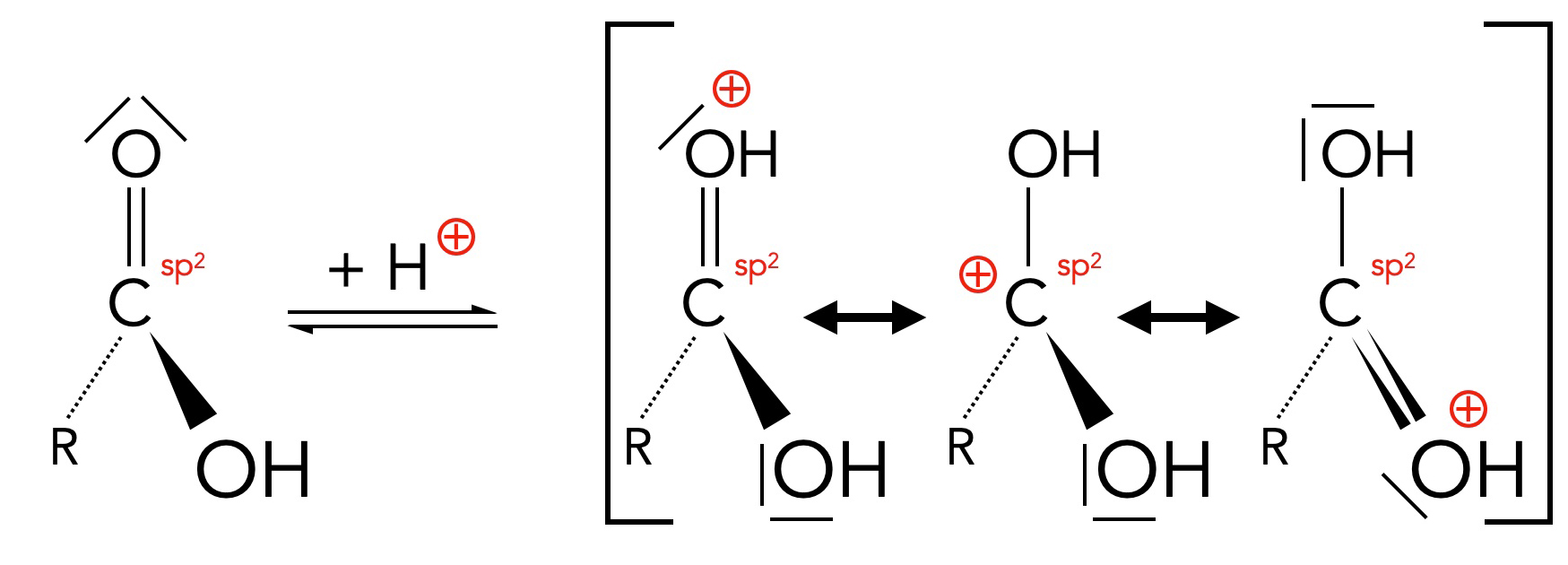
Schritt 1 der säurekatalysierten Esterbildung
Autor: Ulrich Helmich 06/2024, Lizenz: Public domain
Im ersten Schritt der säurekatalysierten Esterbildung wird die Carbonsäure protoniert. Das Proton - meistens von Schwefelsäure gespendet - setzt sich an das O-Atom der Carbonyl-Gruppe. Das so gebildete Kation wird aber durch mehrere Grenzstrukturen stabilisiert, eine der wichtigsten Grenzstrukturen ist das Carbenium-Ion, das in der Mitte des rechten Kastens zu sehen ist.
Schritt 2
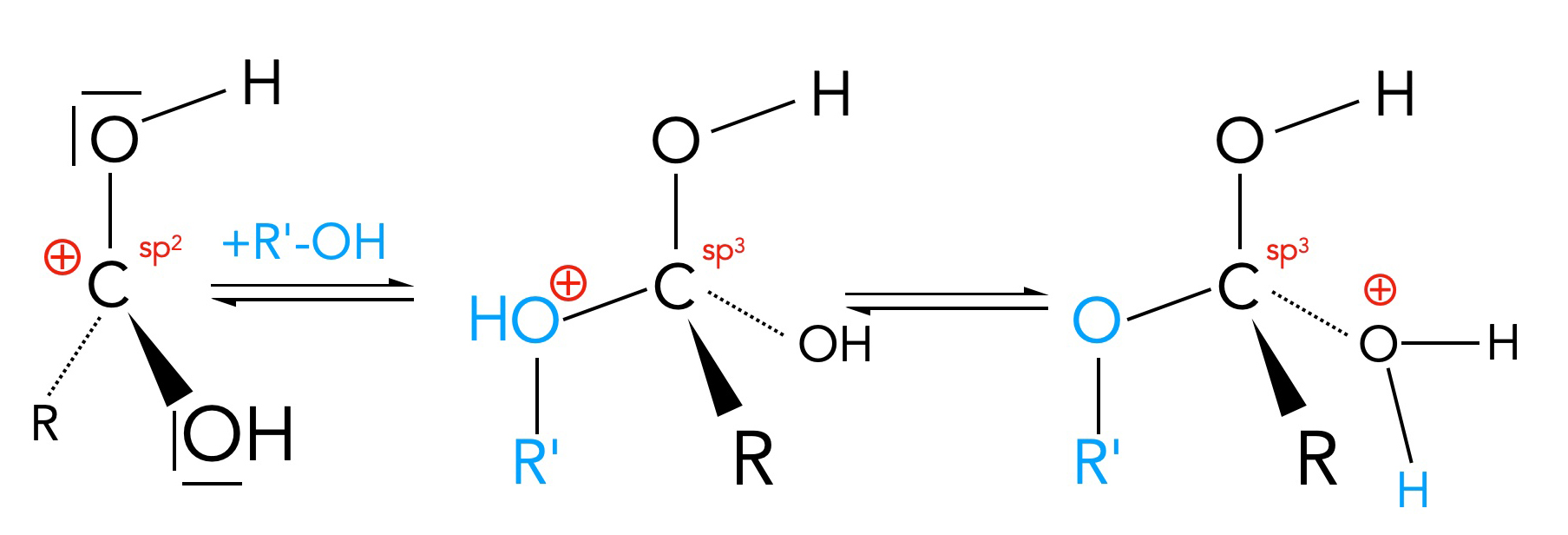
Schritt 2 der säurekatalysierten Esterbildung
Autor: Ulrich Helmich 06/2024, Lizenz: Public domain
Das Carbenium-Ion aus Schritt 1 wird nun von dem Alkohol nucleophil angegriffen (Addition). Die positive Ladung wird dann von dem O-Atom des Alkohols übernommen (mittleres Bild). Das "mitgebrachte" H-Atom (blau gekennzeichnet) wandert dann aber mit der positiven Ladung zu dem O-Atom der OH-Gruppe der Carbonsäure (rechtes Bild).
Schritt 3
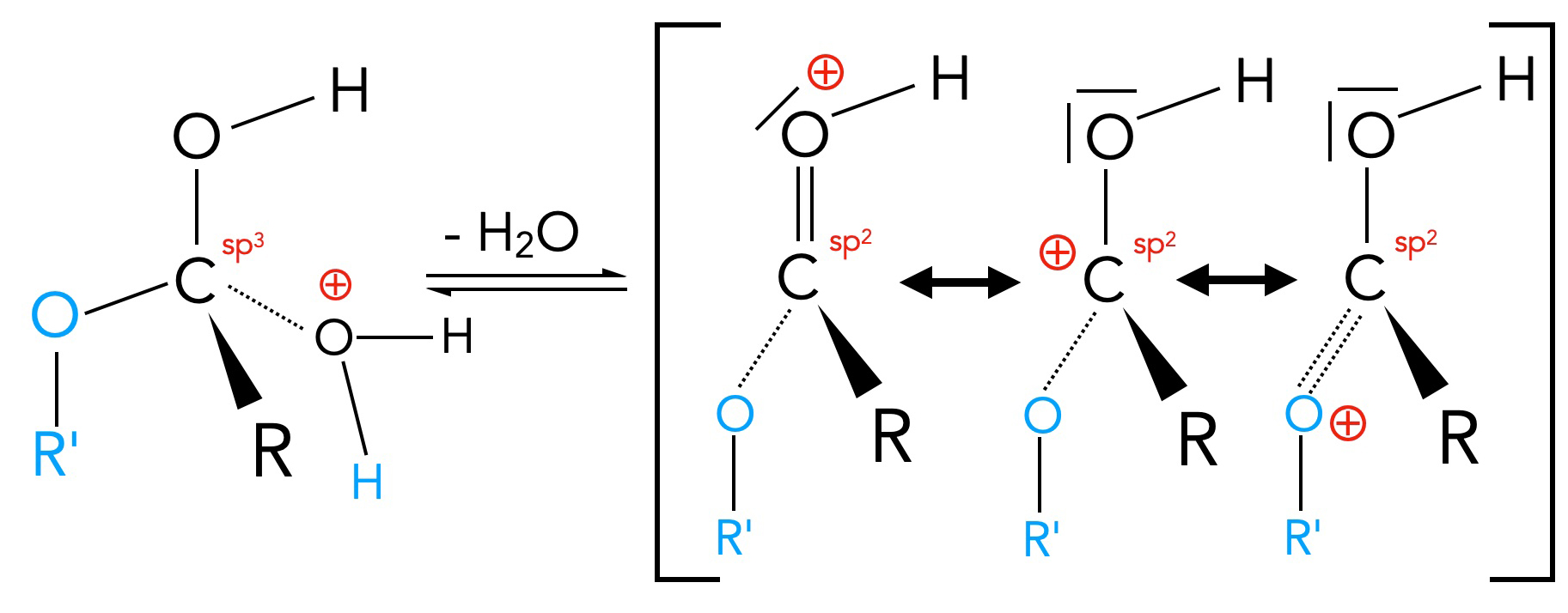
Schritt 3 der säurekatalysierten Esterbildung
Autor: Ulrich Helmich 06/2024, Lizenz: Public domain
Die positiv geladene OH2-Gruppe wird nun als H2O-Molekül abgespalten (Eliminierung). Es bildet sich ein neues Zwischenprodukt, das durch mehrere Grenzstrukturen mesomeriestabilisiert ist.
Schritt 4
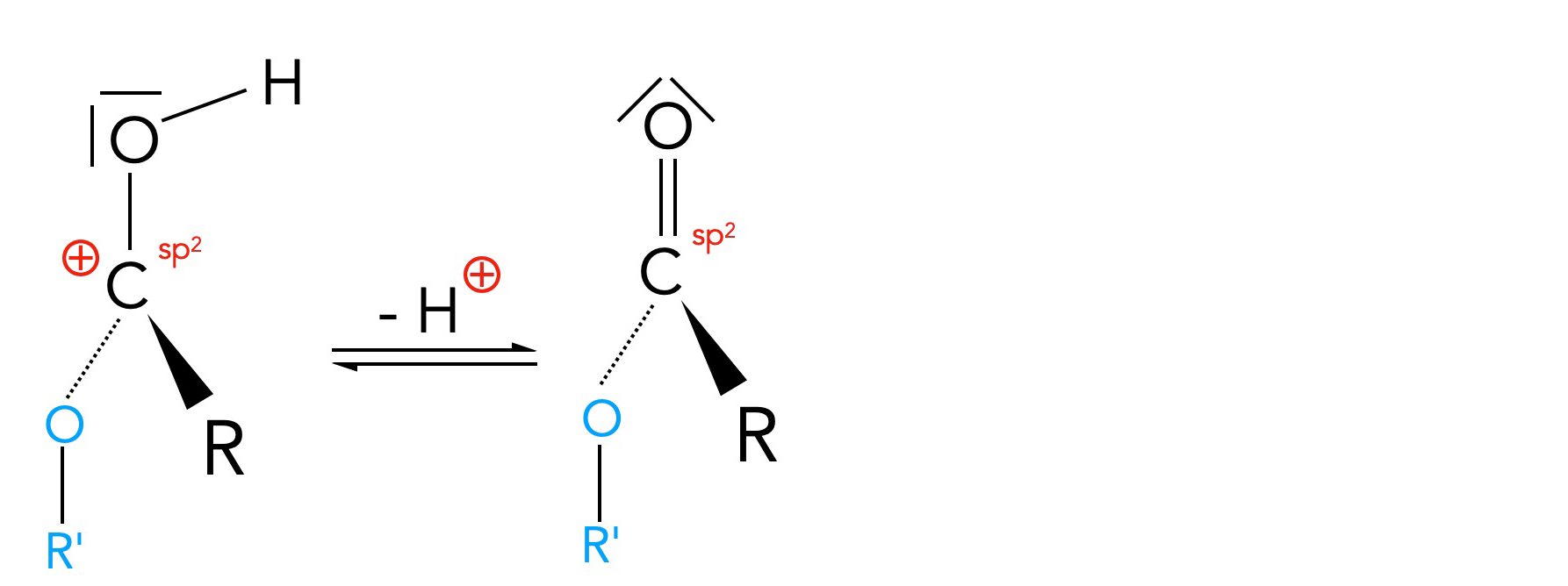
Schritt 4 der säurekatalysierten Esterbildung
Autor: Ulrich Helmich 06/2024, Lizenz: Public domain
Im letzten Schritt der säurekatalysierten Esterbildung aus einer Carbonsäure wird das zuvor eingesetzte Proton regeneriert, und es bildet sich das Endprodukt.
Insgesamt entspricht die säurekatalysierte Esterbildung also dem allgemeinen Additions-Eliminierungs-Mechanismus, der für die nucleophile Substitution an der COOH-Gruppe charakteristisch ist.
Auf dieser Lexikon-Seite finden Sie weitere Informationen zur Stoffklasse der Ester. Nicht nur Carbonsäure-Ester werden hier behandelt, sondern auch Ester von Mineralsäuren wie zum Beispiel Phosphorsäure.
Diese Seite wurde für Schüler(innen) der Sek. II geschrieben. Hier finden Sie - bei Bedarf - grundlegende Informationen zur Stoffklasse der Ester, zur Synthese (einschließlich einem bekannten Schulversuch) und zu den Reaktionen der Ester.
Hier sehen Sie in Einzelschritten, wie sich ein Ester aus einem Carbonsäure-Chlorid bildet.
Quellen:
- VollhardT, Schore: Organische Chemie. 6. Auflage, Weinheim 2020.
- Buddrus, Schmidt, Grundlagen der Organischen Chemie, 5. Auflage, De Gruyter-Verlag 2014.
- engl. Wikipedia, Artikel "Carboxylic acid"
- Wikipedia, Artikel "Carbonsäurechloride, Darstellung"
Seitenanfang -
Weiter mit den Carbonsäure-Chloriden...