In dieser NRW-Abituraufgabe aus dem Jahre 2007 (Leistungskurs) geht es um die industrielle Herstellung des Antiklopfmittels MTBE (Methyltertiärbutylether).
Die Aufgabe
Material:
Betrachten wir zunächst kurz das vorgegebene Material, das im NRW-Abitur als "Informationstext" bezeichnet wird.
Zunächst wird dargestellt, wie man den Treibstoffzusatz MTBE eigentlich herstellen können sollte, nämlich durch Reaktion von Methanol mit 2-Chlor-2-methyl-propan.
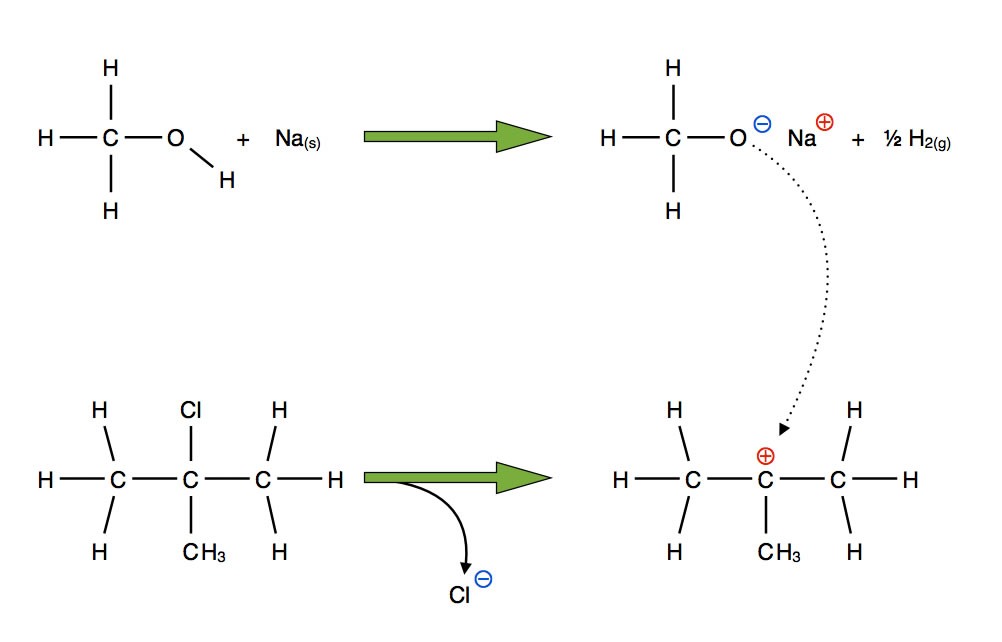
So könnte theoretisch MTBE synthetisiert werden, nach dem Verfahren der Williamson-Ethersynthese, einer nucleophilen Substitution.
Dieses Bild stand den Abiturienten damals nicht zur Verfügung, ich habe es ergänzt, um die Aufgabenstellung transparenter zu machen.
Autor: Ulrich Helmich 2020.
Dummerweise funktioniert dieses Vorgehen aber nicht, die gewünschte Verbindung tritt nur als Nebenprodukt auf. Als Hauptprodukt findet man ein Gas, "das eine positive Bromwasserreaktion zeigt". Dann kommt ein meiner Meinung nach eher verwirrender Hinweis, nämlich dass außerdem Methanol und NaCl entstehen.
Dann wird das "richtige" industrielle Verfahen vorgestellt: Reaktion von 2-Methyl-propen mit Methanol unter saurer Katalyse.
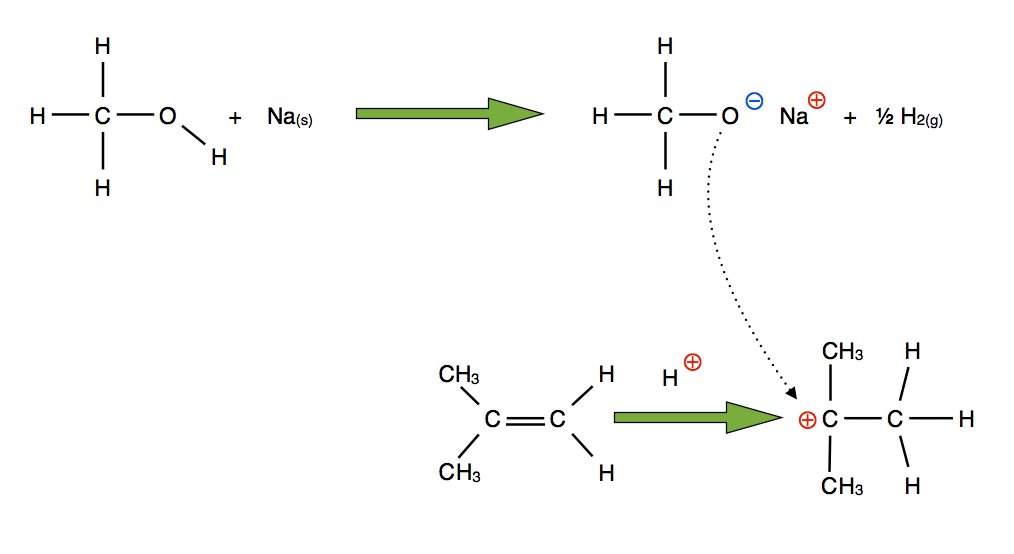
So wird MTBE synthetisiert, durch eine elektrophile Addition
Dieses Bild stand den Abiturienten damals nicht zur Verfügung, ich habe es ergänzt, um die Aufgabenstellung transparenter zu machen.
Autor: Ulrich Helmich 2020.
Den Schüler(innen) wurden außerdem mitgeteilt, dass man das 2-Methyl-propen aus 2-Methyl-propan-2-ol erhält, das mit ein wenig konz. Schwefelsäure erhitzt wird.
Dann folgen in dem Informationstext weitere Fakten, die sich auf den radikalischen Mechanismus der Verbrennung des Treibstoffs beziehen. Diese Fakten sind allerdings nur für die LK-Version der Aufgabe wichtig, daher werde ich jetzt nicht weiter darauf eingehen. Diese Webseite richtet sich in erster Linie an GK-Schüler.
Aufgabenstellung:
Welche Aufgaben wurden nun im Jahre 2007 gestellt? Schauen wir uns die Aufgabenstellung mal kurz an. Allerdings gehe ich hierbei nur auf die ersten drei Aufgaben ein; die vierte ist eine typische LK-Aufgabe, die ich hier nicht weiter berücksichtige. Hier sollte auf die Wirkung des Antiklopfmittels MTBE näher eingegangen werden.
Aufgabe 1
Die S. sollen hier das theoretisch mögliche, aber nicht praktizierte Verfahren zur MTBE-Synthese erläutern, also die Reaktionsgleichungen mit Strukturformeln aufstellen und die Reaktionsmechanismen erläutern.
Aufgabe 2
Hier geht es nochmal um das theoretisch mögliche Verfahren. Die S. sollen begründen, warum das gewünschte Produkt nur als Nebenprodukt auftritt und wieso die Bildung des Hauptprodukts "unerwartet" ist.
Aufgabe 3
Hier soll das tatsächlich durchgeführte Verfahren erläutert werden, ebenfalls wieder mit Reaktionsgleichungen. Außerdem soll hier die Bildung von 2-Methyl-propen erläutert werden.
Erwartungen
Aufgabe 1
Es wurde erwartet, dass die Schüler(innen) die Reaktion so ähnlich erklären wie in der Abbildung 1 gezeigt. Es handelt sich hier um eine klassische nucleophile Substitution. Da die Abgangsgruppe im 2-Chlor-2-methyl-propan an einem tertiären C-Atom hängt, sollte theoretisch der SN1-Mechanismus bevorzugt werden, bei dem sich zunächst das Chlorid-Ion abspaltet (langsamer, geschwindigkeitsbestimmender Schritt) und ein tertiäres stabiles Carbenium-Ion hinterlässt. Die relativ hohe Stabilität erhält das Carbenium-Ion durch den dreifachen +I-Effekt der drei Methylgruppen.
Das Methanolat-Ion setzt sich dann im zweiten Reaktionsschritt (schneller Schritt) an das Carbenium-Ion, so dass das Endprodukt entsteht.
Aufgabe 2
Da es sich um eine SN1-Reaktion mit einem Carbenium-Ion als Zwischenprodukt handelt, besteht immer die Möglichkeit einer alternativen Reaktion: Das Carbenium-Ion kann die "unerwünschte" positive Ladung loswerden, indem es ein Proton abgibt. Genau das passiert auch bei dieser Reaktion, es findet nämlich eine Eliminierung nach dem E1-Mechanismus statt, bei der ein Alken entsteht.
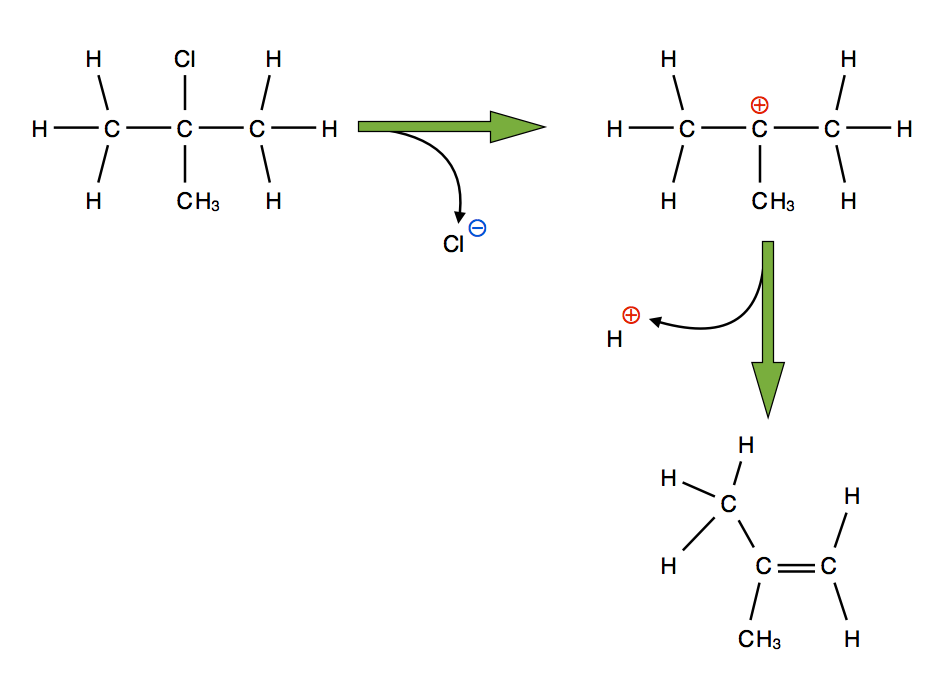
So könnte eine von den Schüler(innen) gezeichnete Lösung für die Aufgabe 2 aussehen.
Autor: Ulrich Helmich 2020.
Es bildet sich das Alken 2-Methyl-propen.
Das wird die Lösung sein, auf die die meisten Schüler wahrscheinlich recht schnell kommen. Es wird dann aber laut offizieller Vorgaben auch erwartet, dass die S. Gründe für die Bevorzugung der Eliminierung nennen, zum Beispiel dass die drei Methylgruppen die Substitution sterisch behindern und dass das Methanolat-Ion doch recht groß ist, außerdem ist es eine starke Base, die sich vielleicht lieber mit Protonen verbindet als sich an ein Carbenium-Ion zu setzen. Darauf werden aber wohl nur die wenigsten Schüler kommen, und auch die wenigsten Schülerinnen.
Dann wird sogar erwartet, dass die S. auf den sich verändernden Bindungswinkel eingehen. Während der Bindungswinkel beim Carbenium-Ion 120º beträgt, hat er sich nach erfolgter Substitution auf 109,5º verringert. Bei der Eliminierung bleibt der Bindungswinkel jedoch bei 120º. Ich glaube nicht, dass meine Schüler von selbst darauf kommen, obwohl ich im Unterricht kurz auf die Veränderung der Bindungswinkel eingegangen bin, nämlich bei der Besprechung der SN2-Reaktion.
Aufgabe 3
Diese Aufgabe ist recht leicht. Das 2-Methyl-propen kann durch Dehydratisierung von 2-Methyl-propan-2-ol gewonnen werden. Diese Dehydratisierung ist nichts anderes als eine weitere Eliminierung nach dem E1-Mechanismus.
Im nächsten Schritt findet dann eine elektrophile Addition an die C=C-Doppelbindung des gebildeten Alkens statt, und zwar lagert sich Methanol an. Das H-Atom als Proton an das eine C-Atom, das Methanolat-Ion als Anion an das entstandene Carbenium-Ion.
Fazit
Insgesamt eine sehr schöne Aufgabe, finde ich. Ich persönlich hätte starke Schwierigkeiten, selbst eine solche Aufgabe zu konstruieren. Also Hut ab vor den Kollegen, die sich die Arbeit machen, solche Aufgaben zu entwickeln!
Abitur NRW
Die Aufgaben von 2007 bis 2016 stehen online nicht mehr zur Verfügung, jedenfalls nicht mehr offiziell. Man munkelt ja, dass die alten Aufgaben irgendwann wiederverwertet werden. Ich persönlich kann mir das aber nicht vorstellen, weil sich inzwischen ja die Kernlehrpläne vollständig geändert haben. Wissen spielt ja fast so gut wie keine Rolle mehr, dafür jede Menge Kompetenzen, die in den zentralen Abituraufgaben überprüft werden sollen. Ich muss da immer an den Spruch eines Bildungsforschers denken, der gesagt hatte "Kompetenzen ohne Fachwissen ist wie Stricken ohne Wolle". Ich bin ja schon mal gespannt auf die nächsten NRW-Aufgaben.