Im vierten Schritt wird die durch zwei Phosphat-Gruppen aktivierte Glucose in zwei Bruchstücke zerlegt. Damit ist die Vorbereitungsphase der Glycolyse abgeschlossen.
Schritt 4.1
Jetzt erfolgt die Spaltung des Fructose-1,6-bisphosphats in zwei kleinere Moleküle, nämlich in Glycerinaldehyd-phosphat und Dihydroxyaceton-phosphat.
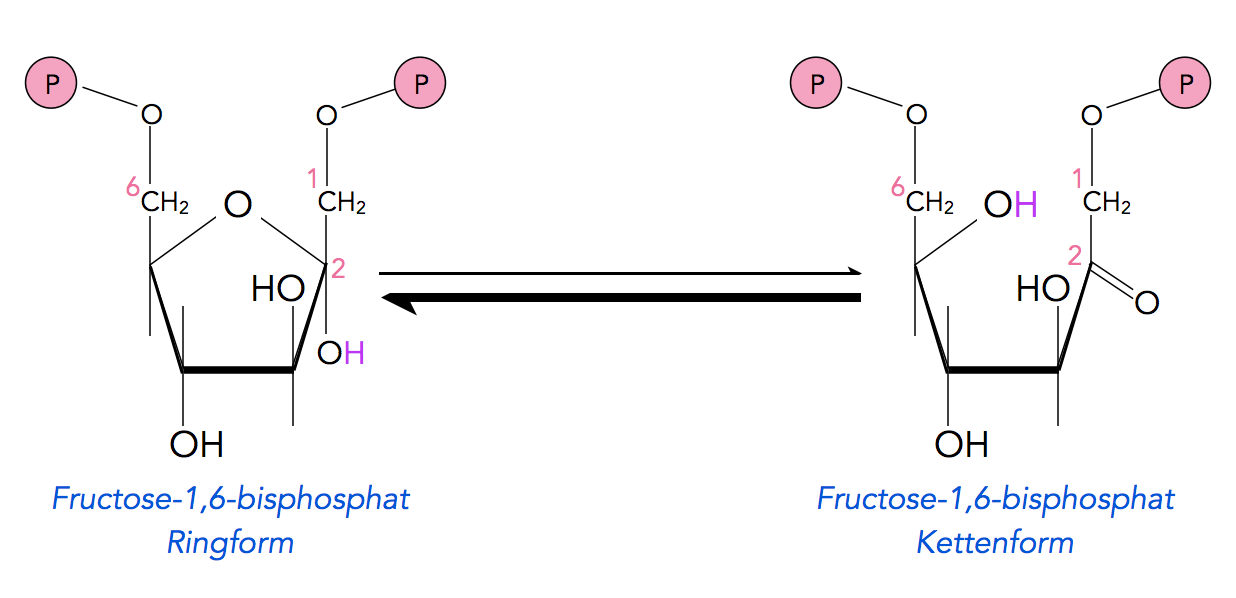
Damit diese Spaltung erfolgen kann, muss die Ringform des Fructose-1,6-bisphosphats zunächst in die isomere Kettenform umgewandelt werden. Das ist aber überhaupt kein Problem, denn in einer wässrigen Lösung liegt sowieso immer ein kleiner Bruchteil der Moleküle in der Kettenform vor. Bei der Glycolyse wird die Ringspaltung aber durch das Enzym Aldolase gefördert.
Das Gleichgewicht dieser Reaktion liegt stark auf der linken Seite; die Ringform ist energetisch stabiler als die Kettenform.
Aber wie wir bereits des Öfteren gesehen haben, kann ein solches Gleichgewicht auf die rechte Seite verschoben werden, wenn man das Reaktionsprodukt aus dem Stoffgemisch entfernt. Und das passiert ja im Schritt 4, das kettenförmige Fructose-1,6-bisphosphat wird chemisch in zwei Spaltprodukte zerlegt und wird damit dem Gleichgewicht entzogen.
Schritt 4.2
Nach dieser Ringaufspaltung wird die Bindung zwischen den C-Atomen 3 und 4 durch das Enzym Fructose-1,6-bisphosphat-aldolase(kurz: Aldolase) gespalten, und es entstehen die beiden Spaltprodukte Glycerinaldehyd-phosphat und Dihydroxyaceton-phosphat:
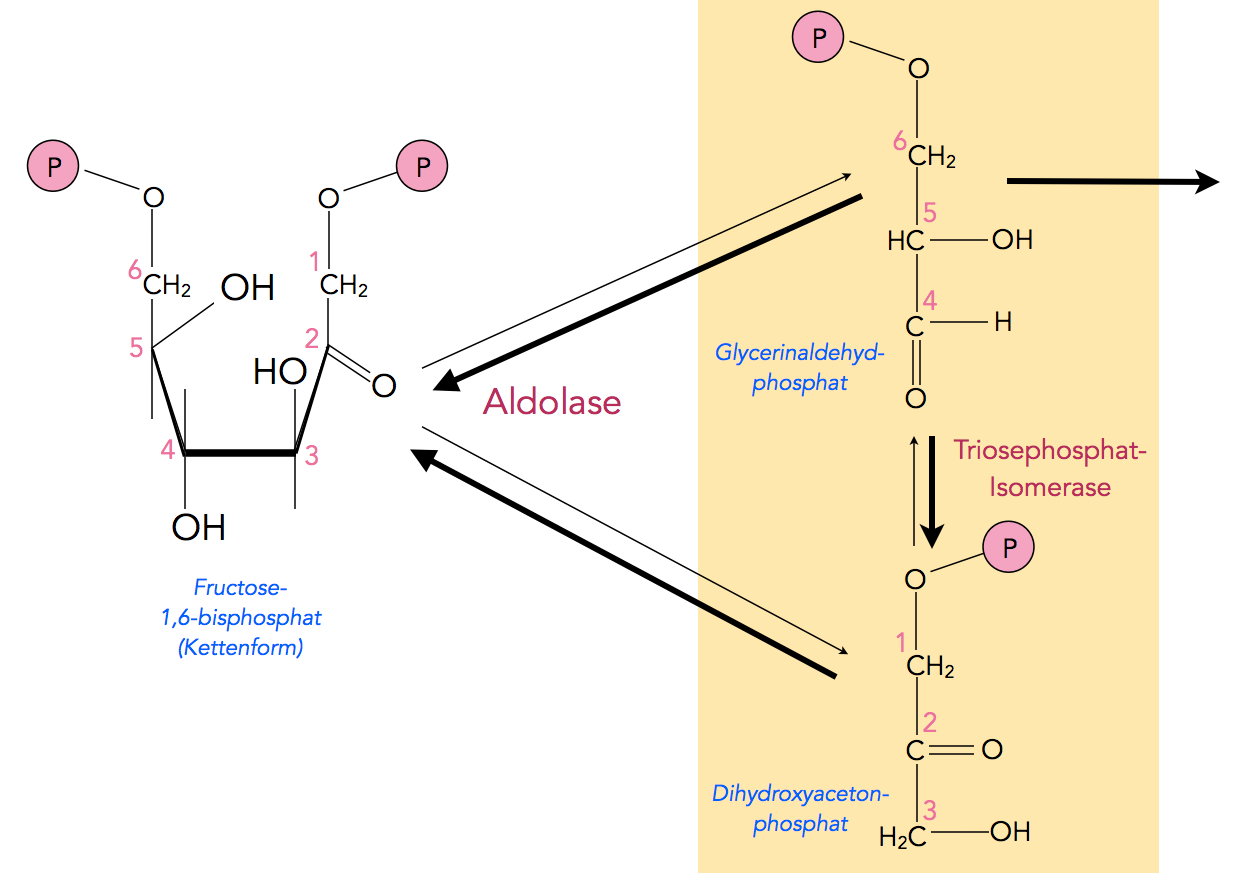
Die Spaltung des offenkettigen Fructose-1,6-bisphosphats durch Aldolase
Autor: Ulrich Helmich 2021, Lizenz: Public domain.
Beim Glycerinaldehyd-phosphat müssen die Kohlenstoff-Atome neu durchnummeriert werden; aus dem C-Atom 6 des Fructose-1,6-bisphosphats wird das C-Atom 3 des Glycerinaldehyd-phosphats und so weiter.
Das chemische Gleichgewicht dieser Spaltung liegt weit links, auf der Seite des Eduktes, also des Fructose-1,6-bisphosphats. Das liegt u.a. daran, dass die Reaktion endotherm ist. Aber nach dem Prinzip des kleinsten Zwangs (Le CHATELIERsches Prinzip) kann man das Gleichgewicht einer Reaktion zur Produktseite verschieben, wenn man ein Endprodukt entfernt (Gleichgewichtsverschiebung).
Und genau das passiert hier; die beiden Spaltprodukte Glycerinaldehyd-3-phosphat und Dihydroxyaceton-phosphat reagieren permanent weiter und werden daher aus dem Gleichgewicht entfernt. Eine Rückreaktion zum Zwischenprodukt Fructose-1,6-bisphosphat wird dadurch stark erschwert. Obwohl also das Gleichgewicht der Reaktion auf der linken Seite liegt, findet die Reaktion ständig statt und die Produkte entstehen in ausreichenden Mengen.
Gleichgewicht zwischen den beiden Produkten
Das Dihydroxyaceton-phosphat steht mit dem isomeren Glycerinaldehyd-phosphat im Gleichgewicht, wobei das chemische Gleichgewicht zu 96% auf der Seite des Dihydroxyaceton-phosphats liegt. Katalysiert wird diese Umwandlung durch das Enzym Triosephosphat-Isomerase.
Da aber nur das Glycerinaldehyd-3-phosphat im nächsten Schritt der Glycolyse weiterverarbeitet werden kann, kommt es auch hier wieder zu einer Gleichgewichtsverschiebung. Wenn die Konzentration an Glycerinaldehyd-3-phosphat durch die weiterverarbeitenden Schritte kleiner wird, wird sofort Dihydroxyaceton-phosphat in Glycerinaldehyd-3-phosphat umgewandelt, um das Gleichgewicht aufrecht zu erhalten (chemisches Gleichgewicht bei 4% Glycerinaldehyd-3-phosphat heißt, dass stets 4% der Moleküle als Glycerinaldehyd-3-phosphat vorliegen müssen. Sinkt die Konzentration unter diesen Wert, entstehen neue Moleküle, bis wieder die Marke von 4% erreicht ist).
Im Grunde entstehen so aus einem Molekül Fructose-1,6-bisphosphat zwei Moleküle Glycerinaldehyd-phosphat.
Das Glycerinaldehyd-phosphat ist jetzt so energiereich, dass es nicht nur oxidiert werden kann, sondern dass bei dieser Oxidation sogar mehr Energie freigesetzt wird, als vorher in Form der beiden ATPs hineingesteckt wurde.
Einzelheiten zum Enzym Aldolase finden Sie auf dieser Lexikon-Seite.
Quellen:
- Alberts, Bruce et al. Molekularbiologie der Zelle, 6. Auflage, Weinheim 2017.
- Nelson, Cox. LEHNINGER Principles of Biochemistry. Macmillan Learning, New York 2021.
- Berg, Tymoczko, Gatto jr., Stryer: Stryer Biochemie, 8. Auflage, Springer Berlin Heidelberg 2018.
Seitenanfang -
Direkt weiter mit Schritt 5...
Erstmal weiter mit dem Überblick zur Energiegewinnungsphase der Glycolyse...