1. Der Osmometer-Versuch
Einen Versuch zur Osmose haben wir ja bereits auf der letzten Seite kennengelernt:
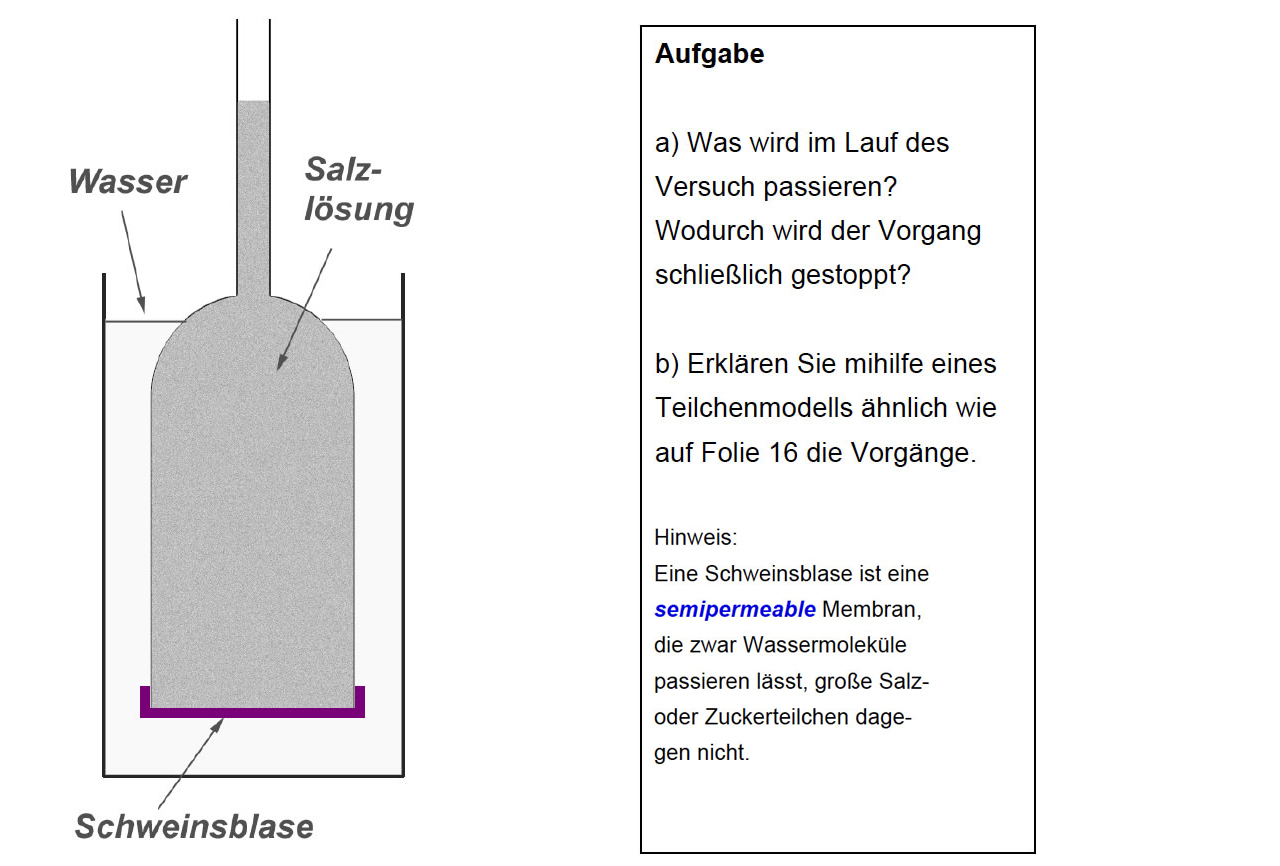
Eine häufig gestellte Aufgabe in Klausuren
Autor: Ulrich Helmich, Lizenz: Public domain
Im Innern des Osmometers herrscht eine geringere Wasser-Konzentration als außerhalb, daher diffundieren Wasser-Moleküle durch die Schweinsblase von außen nach innen; sie "versuchen" quasi, einen Konzentrationsausgleich herzustellen, was natürlich nicht gelingt, da die Salz- oder Zuckerteilchen im Osmometer nicht einfach "verschwinden" können. Durch die eingedrungenen Wasser-Moleküle baut sich aber langsam ein hydrostatischer Druck in der Salzlösung auf, der dem Einströmen der Wasser-Moleküle entgegenwirkt. Nach einer bestimmten Zeit ist dieser hydrostatische Druck so groß, dass im Endeffekt keine Wasser-Moleküle mehr in die Salzlösung eindringen können. Es hat sich ein dynamisches Gleichgewicht eingestellt.
2. Plasmolyse
Versuch:
Plasmolyse von Pflanzenzellen
Durchführung:
Man schneidet eine Zwiebel in kleine Stücke und zieht mit der feinen Pinzette ein dünnes Häutchen von einer der Zwiebelschalen ab. Mit der Schere schneidet man nun ein kleines Quadrat aus diesem Häutchen aus und mikroskopiert es. Allerdings legt man das kleine Zwiebelhäutchen nicht in einen Tropfen Leitungswasser, sondern in einen Tropfen einer 10%igen Kochsalzlösung. Besonders anschaulich wird dieser Versuch, wenn man die Zellen vorher einfärbt hat (oder wenn man gleich rote Zwiebeln verwendet, bei denen man den Protoplasten besonders gut sehen kann).
Beobachtungen:
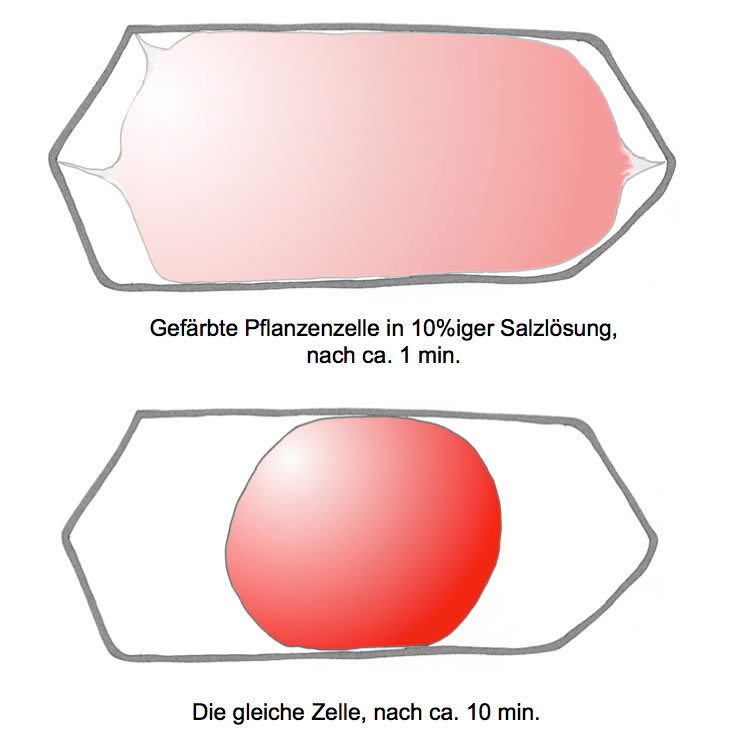
Plasmolyse einer Pflanzenzelle
Autor: Ulrich Helmich, Lizenz: Public domain
Man kann nun beobachten, dass sich der Protoplast recht schnell zusammenzieht, er wird innerhalb weniger Minuten deutlich kleiner.
Deutung:
Die 10%ige Kochsalzlösung (NaCl-Lösung) ist hypertonisch gegenüber dem Protoplasten der Zwiebelzelle, enthält also mehr gelöste Teilchen (Na+- und Cl--Ionen). Die Wasser-Konzentration in der Kochsalzlösung ist daher kleiner als die Wasser-Konzentration im Protoplasten, es besteht also ein Wasser-Konzentrationsgefälle von innen nach außen. Das führt dazu, dass Wasser-Moleküle durch die Membranen des Protoplasten (1. Tonoplast = Membran der Vakuole, 2. Zellmembran) nach außen diffundieren. Da Wasser aus sehr kleinen und elektrisch ungeladenen Molekülen besteht, ist diese Diffusion durch die Lipid-Doppelschichten auch kein großes Problem.
Neben dem Wasser-Konzentrationsgradienten gibt es zwei weitere Konzentrationsgradienten, nämlich einen Na+-Gradienten von außen nach innen und einen Cl--Gradienten, ebenfalls von außen nach innnen. Die Kochsalz-Ionen haben daher das Bestreben, in die Zwiebelzelle hinein zu diffundieren, bis diese Konzentrationsunterschiede ausgeglichen sind. Aber das ist nicht möglich, weil die Membran keine geladenen Teilchen durchlässt. Die Na+- und Cl--Gradienten bleiben also bestehen, während immer mehr Wasser nach außen diffundiert.
Im Endeffekt verliert die Zelle (genauer die Vakuole) also immer mehr Wasser an das Außenmedium, ohne dafür Teilchen zurück zu bekommen. Im Mikroskop sieht man dann, wie die Protoplasten immer kleiner werden und sich schließlich kugelförmig zusammenziehen.
Weiterführende Fragen
Wann kommt dieser Prozess zum Stillstand? Verschwinden die Protoplasten schließlich ganz?
Durch das Austreten der Wasser-Moleküle wird die Konzentration der anderen Verbindungen im Innern des Protoplasten immer größer. Man denke an die Definition des Begriffs "Konzentration": Stoffmenge pro Volumen. Da das Volumen der Protoplasten immer kleiner wird, wird die Konzentration der verschiedenen gelösten Stoffe im Protoplasten immer größer.
Irgendwann ist die Gesamtkonzentration der im Protoplasten gelösten Teilchen genau so groß wie die Salzkonzentration im Außenmedium. Jetzt herrscht also eine Art Konzentrationsausgleich, und die Diffusion der Wasser-Moleküle nach außen kommt zu einem scheinbaren Stillstand; es hat sich ein dynamisches Gleichgewicht eingestellt.
Vergleich mit dem Osmometer-Versuch
Beim Osmometer-Versuch hat sich der Gleichgewichtszustand dadurch eingstellt, dass der hydrostatische Druck in der Salzlösung immer größer wurde, nämlich durch die Aufnahme der Wasser-Moleküle, die aus dem Außenmedium eindiffundierten.
Bei der Plasmolyse stellt sich das dynamische Gleichgewicht dadurch ein, dass die Stoffkonzentration im Protoplasten immer größer wird, bis sie schließlich den Wert des Außenmediums erreicht hat.
3. Deplasmolyse
Noch besser kann man den Vorgang der Deplasmolyse mit dem Osmometer-Versuch erklären. Wenn man das Zwiebelhäutchen mit den zusammengeschumpften Protoplasten nun mit der Pinzette anfasst in einen Tropfen Leitungswasser legt, so kann man einen umgekehrten Prozess beobachten: Die Protoplasten nehmen wieder an Volumen zu, bis sich der ursprüngliche natürliche Zustand eingestellt hat.
Die Erklärung für diese Deplasmolyse ist nun recht einfach: Im Protoplasten herrscht eine größere Stoffkonzentration als im Leitungswasser - oder anders gesehen: Im Leitungswasser herrscht eine größere Wasser-Konzentration als im Protoplasten, daher diffundiert Wasser vom Außenmedium in die Protoplasten hinein.
Interessant wird die Deplasmolyse, wenn man sie nicht mit Leitungswasser, sondern mit destilliertem Wasser durchführt. Jetzt werden die Protoplasten noch größer, die Zellen werden richtig "prall". Allerdings wird die Volumenzunahme durch die starre Zellwand begrenzt. Jetzt kann man diesen Versuch durchaus mit dem Osmometer-Versuch vergleichen: Durch die Aufnahme von Wasser aus dem Außenmedium baut sich in der Zelle ein hydrostatischer Druck auf, der mit jedem aufgenommenen Wasser-Molekül größer wird. Dieser hydrostatische Druck ist dem Einströmen von Wasser entgegengerichtet. Da sich im Protoplasten viele gelöste Stoffe befinden, im destillierten Wasser jedoch gar keine, kommt es nie zu einem völligen Konzentrationsausgleich. Die Zelle würde immer mehr Wasser aufnehmen und der Protoplast würde immer größer werden - wenn da nicht die Zellwand wäre, welche die Volumenzunahme des Protoplasten begrenzt.
Führt man den Versuch mit Tierzellen durch, beispielsweise mit Mundschleimhautzellen, so kann man tatsächlich ein Platzen der Zellen beobachten, wenn man sie in destilliertes Wasser legt. Dies ist auch der Grund dafür, dass man destilliertes Wasser auf gar keinen Fall trinken darf.
4. Der Kartoffelzylinder-Versuch
Dieser Versuch wird im Unterricht gern durchgeführt und war auch schon mal das Thema verschiedener Klausuren.
Versuch:
Plasmolyse mit Kartoffelzellen
Durchführung:
Aus einer Kartoffel wird eine rechteckige Scheibe geschnitten, die dann in sechs gleichlange "Pommes frites" gleicher Dicke, gleicher Breite und gleicher Länge zerschnitten wird. Die Länge der Kartoffelzylinder wird notiert.
Sechs Erlenmeyerkolben oder Bechergläser werden mit Zuckerlösungen folgender Konzentration vorbereitet: 0 mol/l, 0,2 mol/l, 0,4 mol/l, 0,6 mol/l, 0,8 mol/l und 1,0 mol/l.
In jedes Glasgefäß wird nun jeweils einer der Kartoffelzylinder gelegt. Nach einem Tag werden die Zylinder herausgenommen und die Länge gemessen.Die Länge der Zylinder wird dann in einem Koordinatensystem gegen die Konzentration der Zuckerlösung graphisch dargestellt.
Beobachtungen:
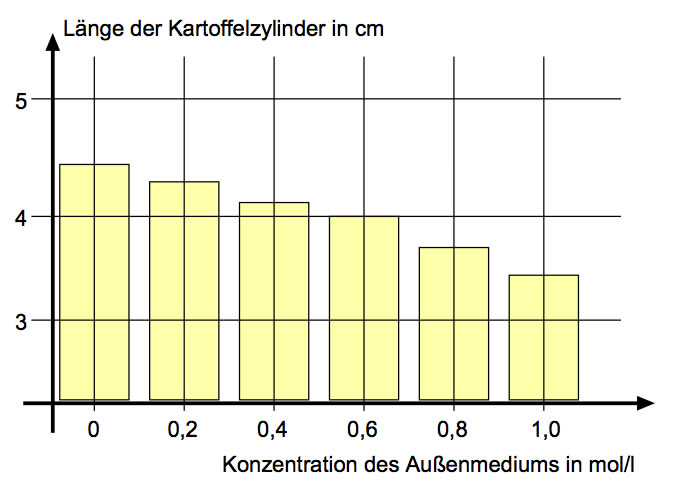
Ergebnisse des Kartoffel-Versuchs
Hier sieht man die Ergebnisse des Kartoffel-Versuchs. Man kann deutlich erkennen, dass die Länge der Kartoffelzylinder von der Zuckerkonzentration im Außenmedium abhängt. Je höher die Zuckerkonzentration, desto kürzer die Zylinder. Die Werte schwanken zwischen 4,7 cm in destilliertem Wasser und 3,4 cm in der 1-molaren Zuckerlösung. Interessant ist auch, dass sich bei einer Konzentration von 0,6 mol/l die Länge der Kartoffelzylinder überhaupt nicht verändert hat.
Deutung:
Bei einer Konzentration < 0,6 mol/l ist die Zuckerlösung hypoton gegenüber den Kartoffelzellen, enthält also weniger gelöste Teilchen pro Volumeneinheit. Da die Wasserkonzentration in einer hypotonen Lösung größer ist als in den Kartoffelzellen, diffundiert Wasser in die Zellen hinein. Diese nehmen dadurch an Volumen zu (natürlich in Grenzen, wegen der starren Zellwand), und der Kartoffelzylinder wird länger.
Bei einer Konzentration von > 0,6 mol/l ist die Zuckerlösung hyperton gegenüber den Kartoffelzellen, also diffundiert Wasser aus den Kartoffelzellen in die Zuckerlösung. Die Kartoffelzellen werden dadurch kleiner (auch hier wieder begrenzt durch die starre Zellwand), und die Kartoffelzylinder schrumpfen.
Die Konzentration 0,6 mol/l ist isoton gegenüber den Kartoffelzellen, enthält also genau so viele gelöste Teilchen pro Volumeneinheit wie das Protoplasma, und daher ist auch die Wasser-Konzentration gleich. Es findet keine sichtbare Diffusion von Wasser statt, die Zylinder verändern ihre Länge nicht.
5. Der Phenolphthalein-Versuch
Hier ein weiterer interessanter Versuch zum Thema "Osmose":
Versuch
Osmose mit NaOH und Phenolphthalein
Durchführung:
Aus Einmachfolie wird ein Beutel geformt, der mit verdünnter Phenolphthalein- Lösung gefüllt wird. Oben wird der Beutel durch eine Schnur oder einen Gummiring zusammengehalten.
Der so gefüllte Beutel wird in ein großes Glasgefäß gehängt, das mit verdünnter Natronlauge gefüllt ist. Nun wird einige Zeit beoachtet.
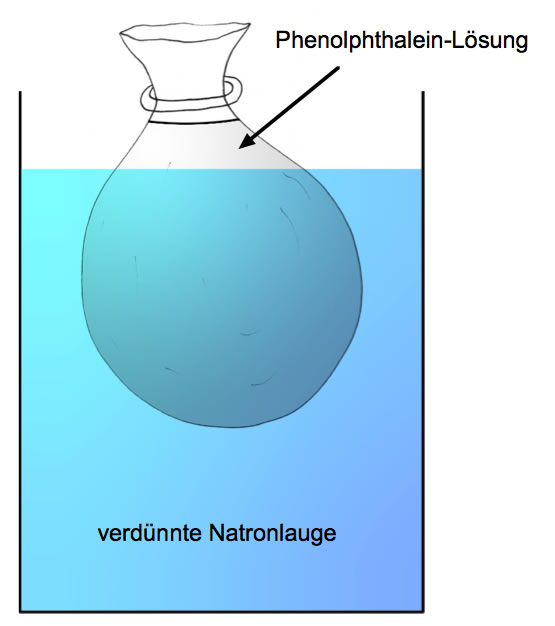
Der Phenolphthalein-Versuch
Beobachtungen:
Eine Volumenzunahme des Beutels ist so gut wie nicht zu beobachten, aber der ursprünglich farblose Beutel färbt sich langsam violett.
Deutung:
Wie man aus dem Chemie-Unterricht weiß, ist Phenolphthalein ein Indikator für Hydroxid-Ionen. Liegt der pH-Wert der Lösung unter 8, so ist Phenolphthalein farblos, bei einem pH-Wert über 8 nimmt der Indikator jedoch eine tiefviolette Farbe an. Warum das so ist, habe ich auf meinen Chemieseiten zum Phenolphthalein erklärt.
Das Phenolphthalein immer Innern des Beutels ist zunächst farblos, weil die Lösung in dem Beutel einen pH-Wert < 8 hat. Wenn man den Beutel in verdünnte Natronlauge hängt, diffundieren Hydroxid-Ionen in den Beutel hinein. Die "Membran" des Beutels ist offensichtlich permeabel für Hydroxid-Ionen. Wenn eine bestimmte Anzahl von Hydroxid-Ionen in den Beutel eingedrungen ist, erreicht der pH-Wert im Beutel einen Wert von 8 oder größer, und der Indikator schlägt farblich um, das Phenolphthalein wird violett.
Warum wird die verdünnte Natronlauge nicht ebenfalls violett?
Ganz einfach: Phenolphthalein-Moleküle sind sehr groß, und die Membran des Beutels ist nicht permeabel für diese großen Moleküle.
6. Der Ionenfallenversuch
Dieser Versuch, der eine wichtige Rolle bei der Aufklärung der Membranstruktur und -funktion gespielt hat, wird auf einer eigenen Lexikon-Seite erklärt.
Lesen Sie sich die Versuchsanleitung, die Beobachtungen und die ausführlichen Erklärungen auf dieser Seite durch und kommen Sie dann wieder hierhin zurück.
Anwendung
Einige Stoffe, die von der Zelle benötigt werden, können "aktiv" in die Zelle transportiert werden, ohne dass ein richtiger aktiver Transport (Pumpenproteine, die ATP verbrauchen) vorliegt. Solche Transportvorgänge verlaufen über einen Mechanismus, der so ähnlich wirkt wie der Ionenfallenversuch.
Glucose ist ein wichtiger Nährstoff für alle Zellen; Gehirnzellen können sich sogar ausschließlich durch Glucose ernähren, während Körperzellen sich auch mit anderen Zuckern oder Fettsäuren zufriedengeben, wenn keine Glucose vorhanden ist. Die Glucose gelangt aus dem Blutkreislauf durch passive Diffusion in diese Zellen.
Allerdings wird die Glucose im Zellplasma sofort durch ein Enzym mit einer Phosphatgruppe versehen, man spricht hier von einer Phosphorylierung. Dadurch wird die Glucose in einen anderen Stoff umgewandelt, der wegen der negativen Ladungen der Phosphatgruppe die Membran nicht mehr passieren kann. Das hat zur Folge, dass die Glucose-Konzentration im Zellinnern immer sehr niedrig bleibt. Die passive Diffusion kann also fortgesetzt werden, auch wenn schon sehr viel Glucose von der Zelle aufgenommen wurde.
Bei diesem Glucose-Transport werden also ebenfalls Ionen erzeugt, welche die Zelle nicht mehr verlassen können.
Seitenanfang -
Das war die letzte Seite zum Thema "Diffusion und Osmose"