Der Neutralrot-Versuch wurde von Biologen lange vor der Entdeckung der Zellmembranen durchgeführt, dieser Versuch und ähnliche waren wichtige Eckpunkte auf dem Weg zur Entwicklung der heutigen Vorstellungen zum Aufbau der Zellmembran. Charles Ernest Overton fand beispielsweise 1899 heraus, dass nicht nur Wasser die Zellmembran passieren kann, sondern auch ungeladene Moleküle, während geladene Ionen die Membran nicht passieren können [1].
Der Ionenfallen-Versuch
Durchführung:
Man schneidet eine Zwiebel in kleine Stücke und zieht mit der feinen Pinzette ein dünnes Häutchen von einer der Zwiebelschalen ab. Mit der Schere schneidet man nun ein kleines Quadrat aus diesem Häutchen aus und mikroskopiert es. Allerdings legt man das kleine Zwiebelhäutchen nicht in einen Tropfen Leitungswasser, sondern in einen Tropfen einer Lösung des Farbstoffs Neutralrot in Leitungswasser mit einem leicht alkalischen pH-Wert ( > 7,5). Destilliertes Wasser darf man hierzu nicht verwenden (Begründung siehe weiter unten).
Beobachtungen:
Man kann nun beobachten, dass sich der Protoplast der Zellen rot färbt, und zwar "richtig" rot, nicht orange oder braun. Mit der Zeit wird diese Färbung immer intensiver, wie das folgende Bild zeigt:
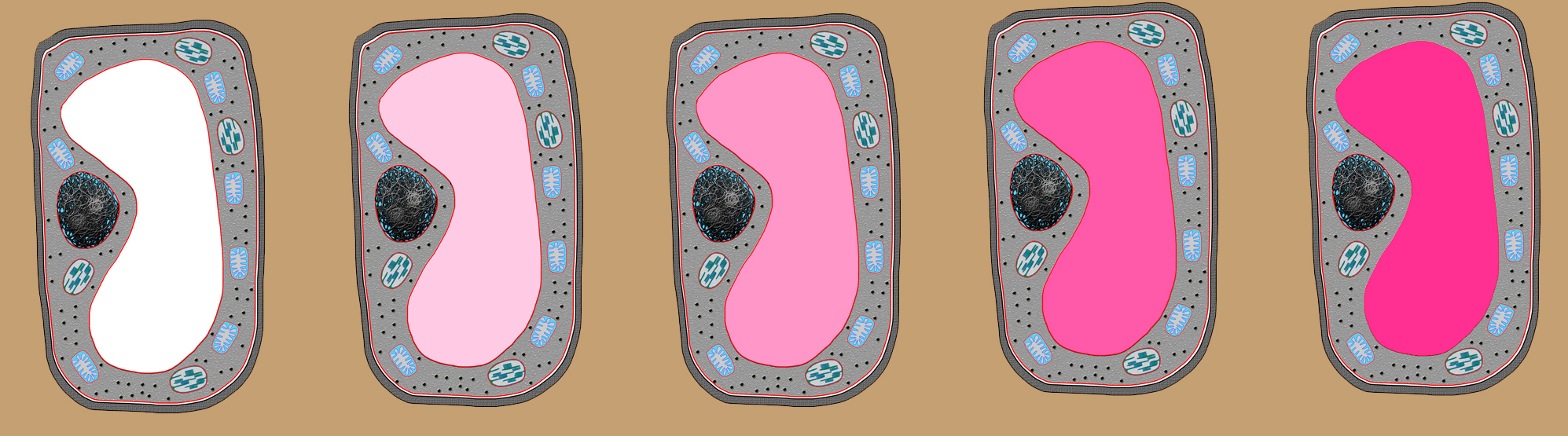
Die Rotfärbung der Zelle wird immer intensiver
Autor: Ulrich Helmich. Lizenz: Public domain.
Mit einem guten Lichtmikroskop kann man vielleicht sogar erkennen, dass nicht das Cytoplasma rot gefärbt wird, sondern nur die Vakuole, die aber einen Großteil des Volumens der erwachsenen Pflanzenzelle ausmacht. Mit einem einfachen Schüler-Mikroskop wird man das wahrscheinlich nicht erkennen.
Erklärung der Beobachtungen
Der Farbstoff Neutralrot
Neutralrot ist ein sogenannter Phenazin-Farbstoff, in fester Form ein graugrünes Pulver, das sich mit gelboranger bis roter Farbe in Wasser gut löst. Die genaue Farbe ist vom pH-Wert des Wassers abhängig. Neutralrot ist nämlich ein pH-Indikator. Eine saure Lösung wird von Neutralrot deutlich rot gefärbt, eine alkalische Lösung gelborange. Der Farbumschlag von rot nach gelborange findet bei einem pH-Wert zwischen 6,8 und 8 statt [2]. Unterhalb von pH 6,8 ist Neutralrot deutlich rot, oberhalb von pH 8 ist Neutralrot deutlich gelb bis gelborange.
Ursache für den Farbumschlag:
In einem sauren Milieu nehmen Neutralrot-Moleküle ein Proton auf und werden dann zu Neutralrot-Ionen, so wie in dem Bild unten dargestellt:

Das Neutralrot-Molekül und das Neutralrot-Ion
Autor: Ulrich Helmich. Lizenz: Public domain.
Während die Neutralrot-Moleküle der Lösung eine gelborange Farbe verleihen, sieht eine Lösung mit Neutralrot-Ionen rot aus.
Erklärung der Beobachtungen:
Bei dem Versuch wurde Neutralrot in Leitungswasser mit einem schwach alkalischen pH-Wert gelöst, die Lösung hat eine gelborange Färbung, weil das Neutralrot hier in Form von Molekülen vorliegt.
In der Vakuole einer Pflanzenzelle herrscht ein eher saures Milieu, der pH-Wert liegt meistens unterhalb von 6 [2]. Die Neutralrot-Moleküle sind hydrophob und nicht elektrisch geladen. Daher können sie die Lipid-Doppelschichten der Zellmembran und der Membran der Vakuole leicht passieren.
In der Vakuole angekommen, reagieren die Neutralrot-Moleküle mit den dort vorhandenen Protonen und werden zu Neutralrot-Ionen. In der Vakuole ändert sich dann die Farbe des Neutralrots von gelborange zu rot.
Die Neutralrot-Ionen können aufgrund ihrer Ladung Wasser-Moleküle anziehen, es bildet sich eine Hydrathülle. Dadurch werden die Neutralrot-Ionen einerseits deutlich größer als die Neutralrot-Moleküle, was eine Diffusion durch die Membranen erschwert. Andererseits sind die Neutralrot-Ionen elektrisch geladen, was für eine Passage durch die Lipid-Doppelschichten der Membranen ebenfalls stark hinderlich ist. Mit anderen Worten: Die Neutralrot-Ionen können nicht mehr aus der Zelle heraus, sie sind in der Zelle "gefangen". Daher heißt dieser Versuch auch "Ionenfallen-Versuch".
Warum nimmt die Rotfärbung der Zellen immer mehr zu; stellt sich nicht irgendwann ein dynamisches Gleichgewicht ein?
Der Trick bei der Sache ist der: Neutralrot-Ionen sind ein anderer "Stoff" als Neutralrot-Moleküle. Die Konzentration der Neutralrot-Moleküle im Zellinnern ist immer sehr gering, während die Konzentration der Neutralrot-Moleküle im Außenmedium immer sehr hoch ist. Die Diffusion der Neutralrot-Moleküle ins Zellinnere kommt also nie zum Stillstand. Jedes eingedrungene Neutralrot-Molekül wird sofort in ein Neutralrot-Ion umgewandelt und kann dann nicht mehr aus der Zelle heraus. Die Pflanzenzelle wird quasi zu einer Gefängniszelle.
Über diesen Ionenfallen-Mechanismus ist eine Anreicherung des Neutralrots in der Vakuole um den Faktor 1000 möglich [3].
Was passiert nun, wenn man den Versuch mit einer sauren Neutralrot-Lösung durchführt?
In einer sauren Neutralrot-Lösung liegen die Neutralrot-Teilchen bereits als Kationen vor, sind also positiv geladen. In diesem Zustand können sie bereits die Zellmembran nicht passieren, und den Tonoplasten (Membran der Vakuole) natürlich auch nicht. Die Vakuole bleibt also farblos. Aber die Zellwand färbt sich langsam rot, denn die Zellwand von Pflanzenzellen enthält neben Cellulose auch jede Menge Pektine, und diese sind zum Teil negativ geladen. Die Neutralrot-Kationen werden also von den Pektinen regelrecht angezogen, daher färbt sich die Zellwand langsam rot.
Quellen:
- Stillwell, William. An Introduction to Biological Membranes (S.28). Elsevier Science 2016.
- Römpp Chemie-Lexikon, 9. Auflage 1992
- Wikipedia, Artikel "Ionenfalle"