Substitution der Hydroxygruppe EF, Q1
Kommen wir nun zu den "richtigen" chemischen Reaktionen der Carbonsäuren. Eine der wichtigsten Reaktionstypen ist die Substitution (Ersetzung) der OH-Gruppe. Hierbei handelt es sich um eine nucleophile Substitution, denn das C-Atom der Carboxygruppe ist ja stark positiv polarisiert.
Bildung von Säurechloriden Q1
Die Bildung von Säurechloriden ist sicherlich die wichtigste Substitutionsreaktion der Carbonsäuren. Säurechloride sind sehr reaktive Derivate der Carbonsäuren und dienen zur Synthese vieler anderer wichtiger Verbindungen, beispielsweise von Estern oder Amiden.
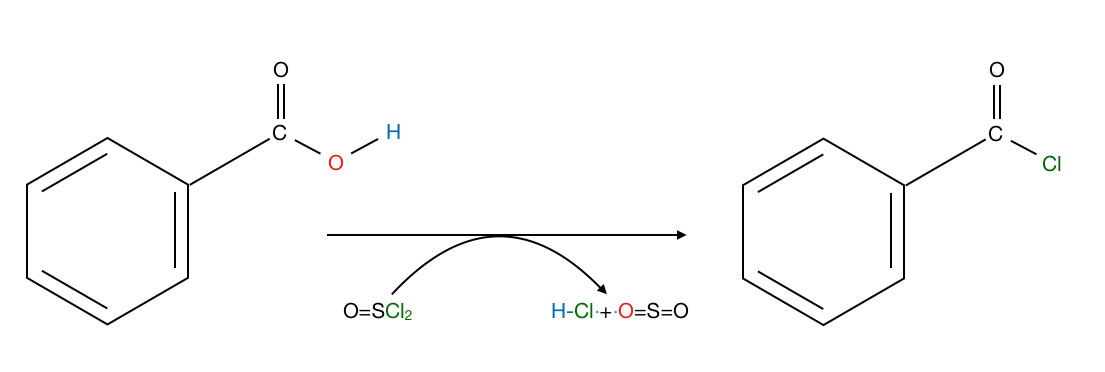
Bildung von Benzoylchlorid aus Benzoesäure und Thionylchlorid
Eine gängige Methode zur Herstellung eines Säure-Chlorids aus einer Carbonsäure ist die Umsetzung der Säure mit der Verbindung Thionylchlorid O=SCl2. Kocht man z.B. Benzoesäure C6H5-COOH mit Thionylchlorid O=SCl2, so erhält man das Säurechlorid BenzoylchloridC6H5-COCl.
Diese Seite im Chemie-Lexikon enthält weiterführende Informationen zur Herstellung von Carbonsäure-Chloriden aus Carbonsäuren, außerdem wichtige Ausführungen zu den Reaktionen der Carbonsäure-Chloride.
Bildung von Estern EF, Q1
Auch die Bildung eines Esters aus einer Carbonsäure und einem Alkohol ist eine nucleophile Substitution. Den Reaktionsmechanismus der säurekatalysierten Estersynthese finden Sie auf der folgenden Seite:
Auf dieser Seite finden Sie die säurekatalysierte Bildung eines Esters aus einer Carbonsäure und einem Alkohol Schritt für Schritt erklärt.
Die Umsetzung einer Carbonsäure mit einem Alkohol ist eine Gleichgewichtsreaktion, und meistens stellt sich das chemische Gleichgewicht bereits ein, wenn erst 40 bis 70% der Säure reagiert haben. Eine Ausbeute von 100%, was der Idealfall wäre, kann man so nicht erzielen.
Wie kann man die Ausbeute an Ester erhöhen?
A) Prinzip des kleinsten Zwangs
Es gibt natürlich die Möglichkeit, das Prinzip des kleinsten Zwangs anzuwenden. Wenn man den entstehenden Ester beispielsweise einfach abdestillieren kann, weil er einen niedrigeren Siedepunkt hat als die Säure und der Alkohol, dann kann man das chemische Gleichgewicht nach rechts verschieben, auf die Produktseite.
Eine andere Möglichkeit, die ebenfalls dieses Prinzip ausnutzt, ist die Erhöhung der Konzentration der Ausgangsstoffe. Dabei spielen auch wirtschaftliche Überlegungen eine wichtige Rolle. Ist beispielsweise die Carbonsäure billiger als der Alkohol, setzt man die Carbonsäure in drei- oder vierfach hoher Konzentration zu, so dass sich das Gleichgewicht nach rechts verschiebt. Ist umgekehrt der verwendete Alkohol billiger als die Carbonsäure, arbeitet man mit einem starken Alkohol-Überschuss.
B) Aktivierung der Carbonsäure
Wenn eine solche Gleichgewichtsverschiebung nicht möglich ist, weil das Reaktionsprodukt einen ähnlichen Siedepunkt hat wie die Ausgangsstoffe, dann kann man statt der Carbonsäure das entsprechende Säurechlorid verwenden, das viel reaktiver ist als die Carbonsäure. Das chemische Gleichgewicht einer solchen Reaktion liegt fast vollständig auf der Produktseite, also auf der Seite des gewünschten Esters. Genau genommen sind beide Schritte einer solchen Estersynthese nahezu irreversibel, sowohl die Bildung des Säurechlorids wie auch die Bildung des Esters aus dem Säurechlorid.
Bildung von Amiden Q1
Amide sind Carbonsäure-Derivate, bei denen die OH-Gruppe der Carboxygruppe durch eine NH2-Gruppe (Aminogruppe) ersetzt wurde. Im Allgemeinen werden Amide nicht direkt aus der Carbonsäure und Ammoniak NH3 hergestellt, sondern aus Säurechloriden und Ammoniak oder Aminen (Amine sind Derivate des Ammoniaks, bei denen ein oder mehrere H-Atome durch Alkylgruppen ersetzt wurden).
Kleine Klausurfrage:
Wieso kann man kein Amid herstellen, indem man einfach Essigsäure mit Ammoniak reagieren lässt?
Antwort:
Ammoniak ist eine starke Base. Die Essigsäure würde sofort ein Proton auf diese Base übertragen, wobei dann das Salz Ammoniumacetat entsteht. Ein Amid könnte so nicht entstehen.
Auf dieser Seite im Chemie-Lexikon finden Sie weitere Informationen zu diesem Thema.
Weiterführende Seiten
Wenn Sie vorhaben, nach Ihrem Abitur Chemie, Biologie oder Medizin zu studieren, dann sollten Sie sich vielleicht ein paar der folgenden Seiten anschauen, die ich extra für Studieninteressierte und auch für Leute, die bereits eines dieser Fächer studieren, geschrieben habe.
Das ist die Einleitungsseite zum Thema "Reaktionen der Carbonsäuren". Hier wird auf die verschiedenen Reaktionen (Substitution der OH-Gruppe, Reduktion, Decarboxylierung etc.) kurz eingegangen.
Hier wird vertiefend erklärt, wie Carbonsäure-Ester aus Carbonsäuren hergestellt werden.
Das Gleiche für die Stoffklasse der Carbonsäure-Anhydride.
Und hier eine Seite zur Synthese von Carbonsäure-Chloriden.
Und schließlich eine Seite zur Herstellung von Carbonsäure-Amiden.
Quellen:
- Morrison, Boyd, Organic Chemistry, 7th Edition 2011
- Römpp Chemie-Lexikon, 9. Auflage 1992
- Wikipedia, Artikel zu den einzelnen Säuren
- Chemgapedia, Artikel "Reaktion von Carbonsäuren"