Azofarbstoffe sind eine wichtige Klasse von Farbstoffen, die in der Chemie und Industrie eine bedeutende Rolle spielen - und auch im Chemie-Abitur!
Struktur
Charakteristisches Merkmal der Azofarbstoffe sind eine oder mehrere Azo-Gruppen (-N=N-), die zwei aromatische Kohlenwasserstoffe miteinander verbinden. Schauen wir uns doch einmal den allereinfachsten Azofarbstoff an, den man sich denken kann: Zwei Benzolringe, verbunden über die Azo-Gruppe. Azobenzol heißt dieser intensiv rote Farbstoff.
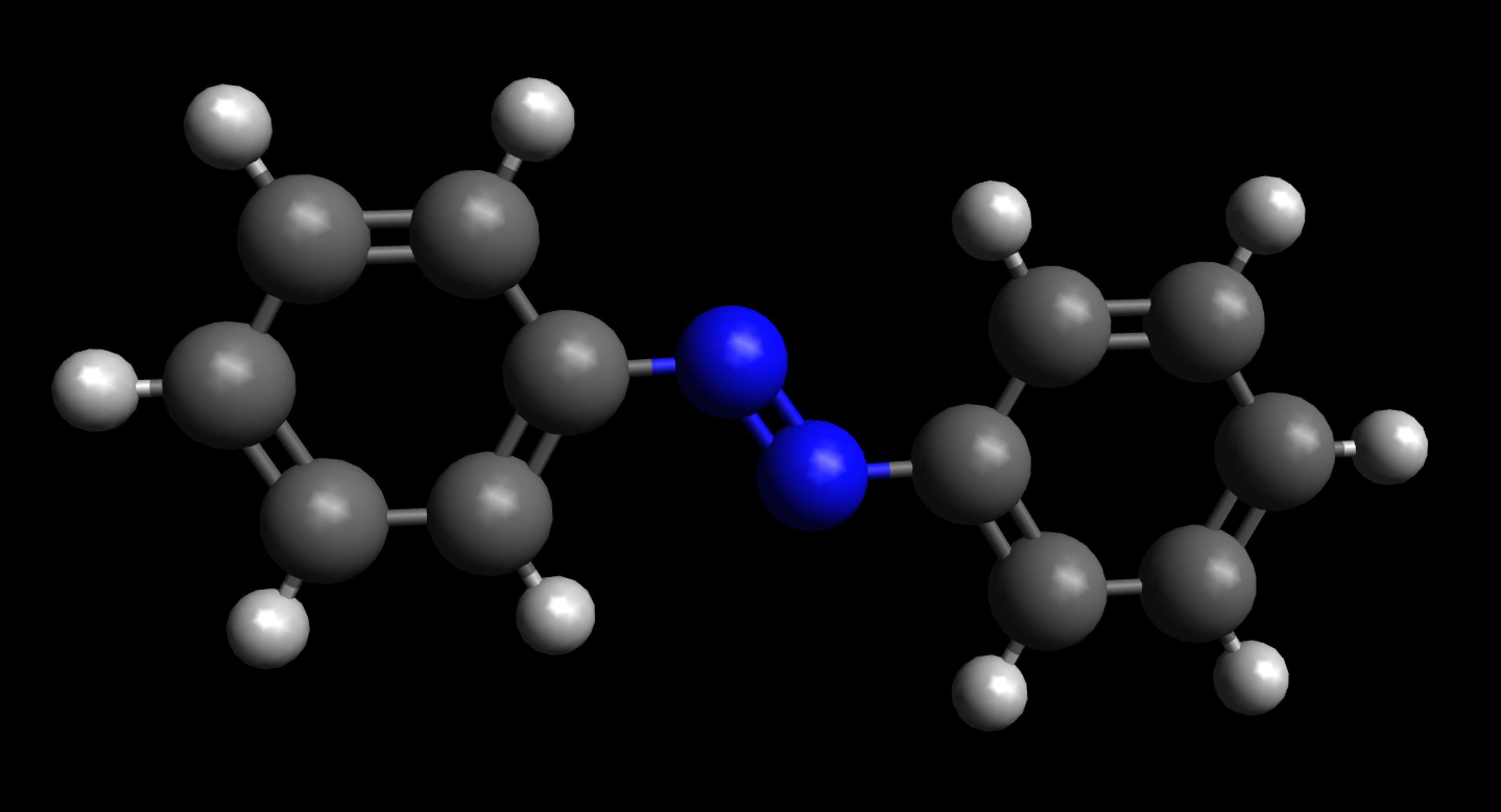
Molekülmodell von Azobenzol, Aufsicht
Autor: Ulrich Helmich, Lizenz: Public domain
Das gesamte Azobenzol-Molekül ist planar, alle C-Atome und die beiden N-Atome sind sp2-hybridisiert, und alle pz-Orbitale können sich daher überlappen. Die pi-Elektronen können sich also im gesamten System frei bewegen.
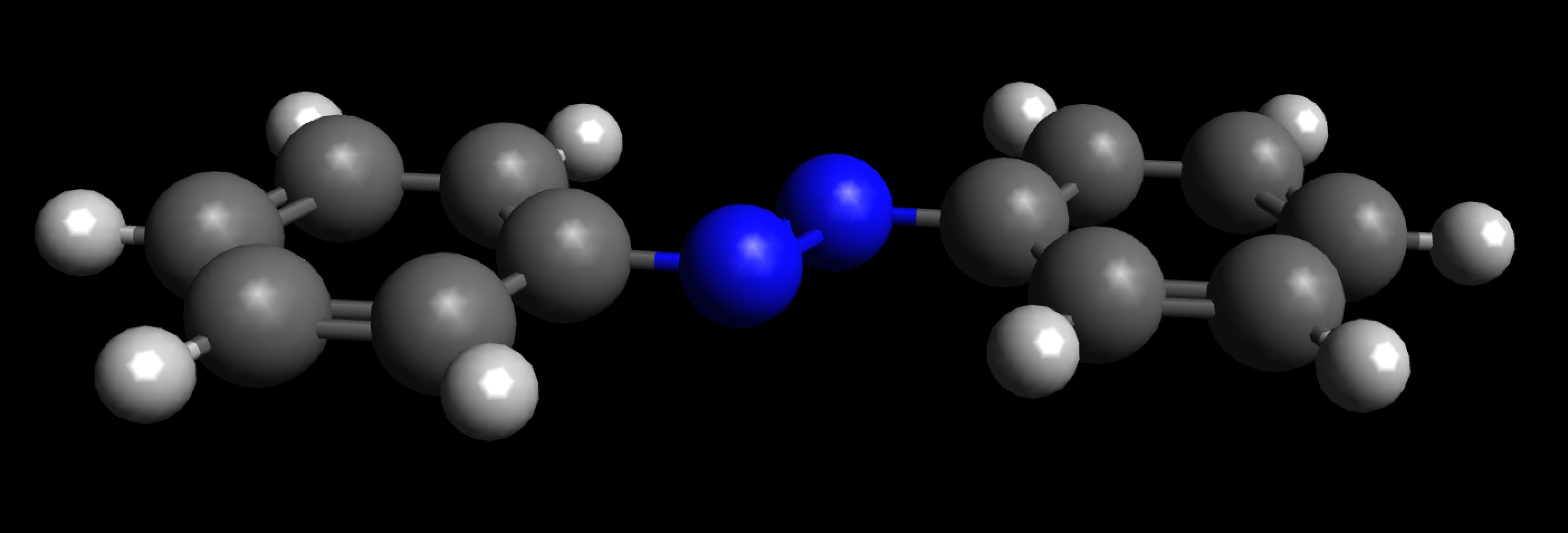
Molekülmodell von Azobenzol, Seitenansicht
Autor: Ulrich Helmich, Lizenz: Public domain
In diesem Wikipedia-Artikel erfahren Sie alle Einzelheiten zu diesem einfachsten Azofarbstoff, der bereits im 19. Jahrhundert entdeckt bzw. synthetisiert wurde.
Die Azofarbstoffe haben nicht nur eine interessante chemische Struktur, sondern auch vielfältige Anwendungen, die von Textilfärbung über Lebensmittel bis hin zu biologischen und medizinischen Bereichen reichen.
Farbigkeit
Die Farbigkeit eines Azofarbstoffs kann durch die Art der Substituenten, die an die Aromaten gebunden sind, sowie durch die chemische Umgebung beeinflusst werden. Diese Substituenten können Elektronen ziehend oder Elektronen schiebend wirken und somit die Wellenlänge des absorbierten Lichts verändern.
Synthese
Die Synthese von Azofarbstoffen erfolgt in der Regel durch eine Diazotierung, gefolgt von einer Kupplungsreaktion.
Schritt 1: Diazotierung
Bei der Diazotierung wird ein aromatisches Amin (wie Anilin) in eine Diazonium-Verbindung umgewandelt.
Zunächst wird das Amin mit salpetriger Säure HNO2 versetzt. Die salpetrige Säure erhält man aus Natriumnitrit NaNO2 und ca. 4 molarer Salzsäure HCl.
Bei der Diazotierung bildet sich ein recht instabiles Diazonium-Kation. Die Temperatur muss während der Reaktion unterhalb von 5 ºC gehalten werden, sonst zerfällt das Diazonium-Kation sofort.
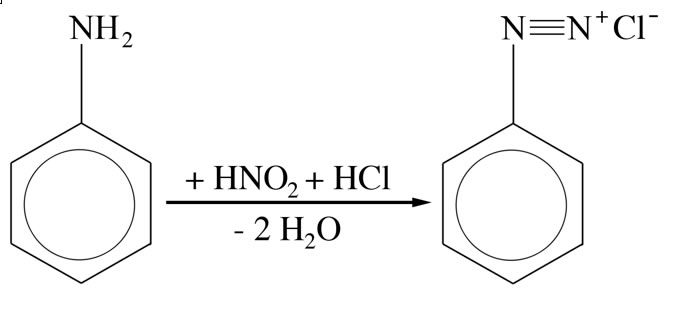
Diazotierung von Anilin
Autor: Ulrich Helmich, Lizenz: Public domain
Schritt 2: Kupplung
Anschließend wird die Diazoniumverbindung in der Kupplungsreaktion mit einer anderen aromatischen Verbindung (wie Benzol, Phenol oder Naphthol) gekoppelt, um den Azofarbstoff zu bilden:
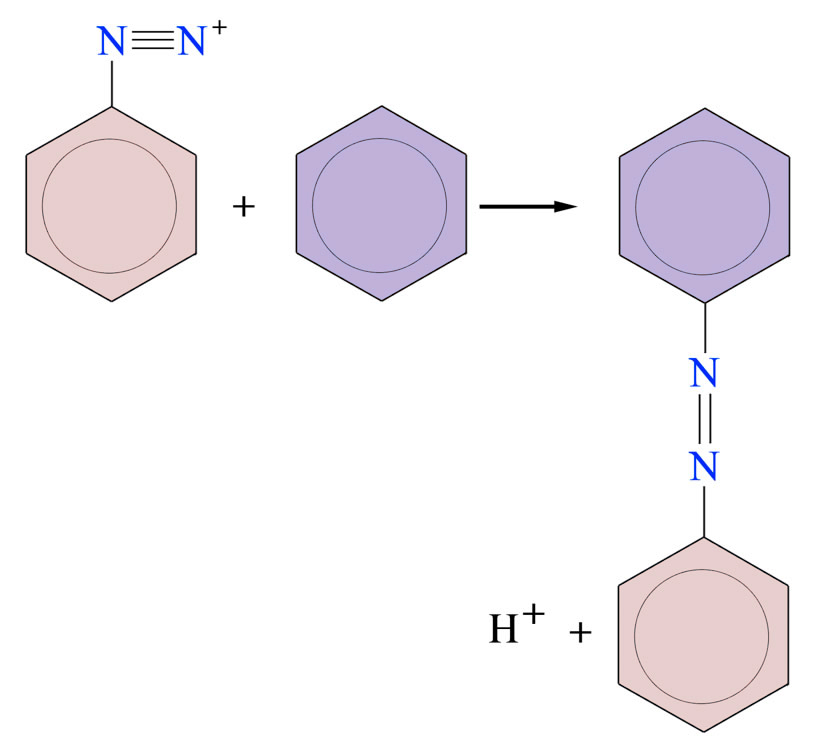
Kupplung mit Benzol
Autor: Ulrich Helmich, Lizenz: Public domain
Diese Kopplungsreaktion ist nichts anderes als die bekannte elektrophile Substitution an einem Aromaten, das Diazonium-Kation R-N≡N+ spielt dabei die Rolle des Elektrophils. Die Aromatizität des "unteren" Benzolrings wird dabei durch Abspaltung eines Protons wieder hergestellt.
Haben Sie aufgepasst?
Die obige Abbildung enthält noch einen kleinen Fehler in der Struktur einer der Moleküle. Haben Sie aufgepasst und können diesen Fehler benennen?
Lösung:
Die N-Atome der N=N-Bindung sind sp2-hybridisiert, die Bindungswinkel C-N=N-C betragen daher 120 Grad und nicht wie in der Abbildung 180 Grad.
Am Beispiel des Azofarbstoffs Naphtholorange wird die Synthese eines solchen Farbstoffs ausführlich in Einelschritten erläutert.
Geschichte der Azofarbstoffe
In der Wikipedia können wir zur Geschichte der Azofarbstoffe folgendes lesen:
Geschichte der Azofarbstoffe
"Mitte des 19. Jahrhunderts hatte sich die Industrialisierung ausgehend von England auf ganz West- und Mitteleuropa ausgebreitet. Durch die Technisierung des Spinn- und Webvorgangs erhielt die Textilindustrie einen Aufschwung, der auch die Nachfrage nach Farbstoffen erhöhte. Diesen neuen Anforderungen kam die Produktion natürlich gewonnener Farbstoffe nicht nach, was die Farbforschung und die rasche Entwicklung der chemischen Industrie förderte.
1844 wagte Justus von Liebig die Prognose, man werde schon bald Methoden entdecken, um aus Steinkohlenteer Farb- und Arzneistoffe synthetisch herzustellen.
1856 schließlich gelang dem Engländer William H. Perkin beim Experimentieren mit Steinkohlenteer die Synthese des ersten künstlichen Teerfarbstoffs Mauvein, der jedoch kein Azofarbstoff ist.
Auf der Londoner Weltausstellung erregte er aber Aufsehen, auch dies förderte die weitere Forschung.
Die Diazotierung wurde dann 1857 von Peter Grieß, einem Schüler von August Wilhelm von Hofmann gefunden. Chemiker entdeckten überall in Europa Herstellungswege für eine ganze Palette solcher Teerfarbstoffe, von Hofmann-Violett über Fuchsin, von Anilingelb (1861) bis hin zu Bismarckbraun, wobei die beiden letztgenannten wichtige Vertreter der Gruppe der Azofarbstoffe sind. Ausgangsstoff war das Anilin, das aus Kohlenteer gewonnen wurde, daher wurde diese Gruppe auch Teerfarbstoffe genannt. ...
Azofarbstoffe wurden schon frühzeitig als Lebensmittelfarbstoffe eingesetzt, beispielsweise Buttergelb ... zum Färben von Butter und Margarine. Die Verwendung von Buttergelb zur Margarinefärbung wurde jedoch 1938 verboten, nachdem man erkannt hatte, dass es bei Ratten Leberkarzinome erzeugen kann. Darüber hinaus gab es noch um 1949 nur wenige Einschränkungen, Azofarbstoffe Nahrungsmitteln zur "Verschönerung" zuzusetzen."