Inhaltliche Schwerpunkte
Auf dieser Seite werden folgende inhaltliche Schwerpunkte* berücksichtigt:
-
funktionelle Gruppen verschiedener Stoffklassen und ihre Nachweise:
Hydroxy-Gruppe,Carbonyl-Gruppe, Carboxy-Gruppeund Ester-Gruppe
*nach dem Kernlehrplan des Landes NRW 2022
Di- und Tricarbonsäuren
Unter Dicarbonsäuren versteht man Carbonsäuren mit zwei COOH-Gruppen, entsprechend werden Carbonsäuren mit drei COOH-Gruppen Tricarbonsäuren genannt. Tricarbonsäuren sind recht selten, die Zitronensäure ist die berühmte Ausnahme. Dicarbonsäuren dagegen kommen recht häufig in der Natur vor und spielen auch in der Lebensmittelchemie und industriellen Chemie eine wichtige Rolle.
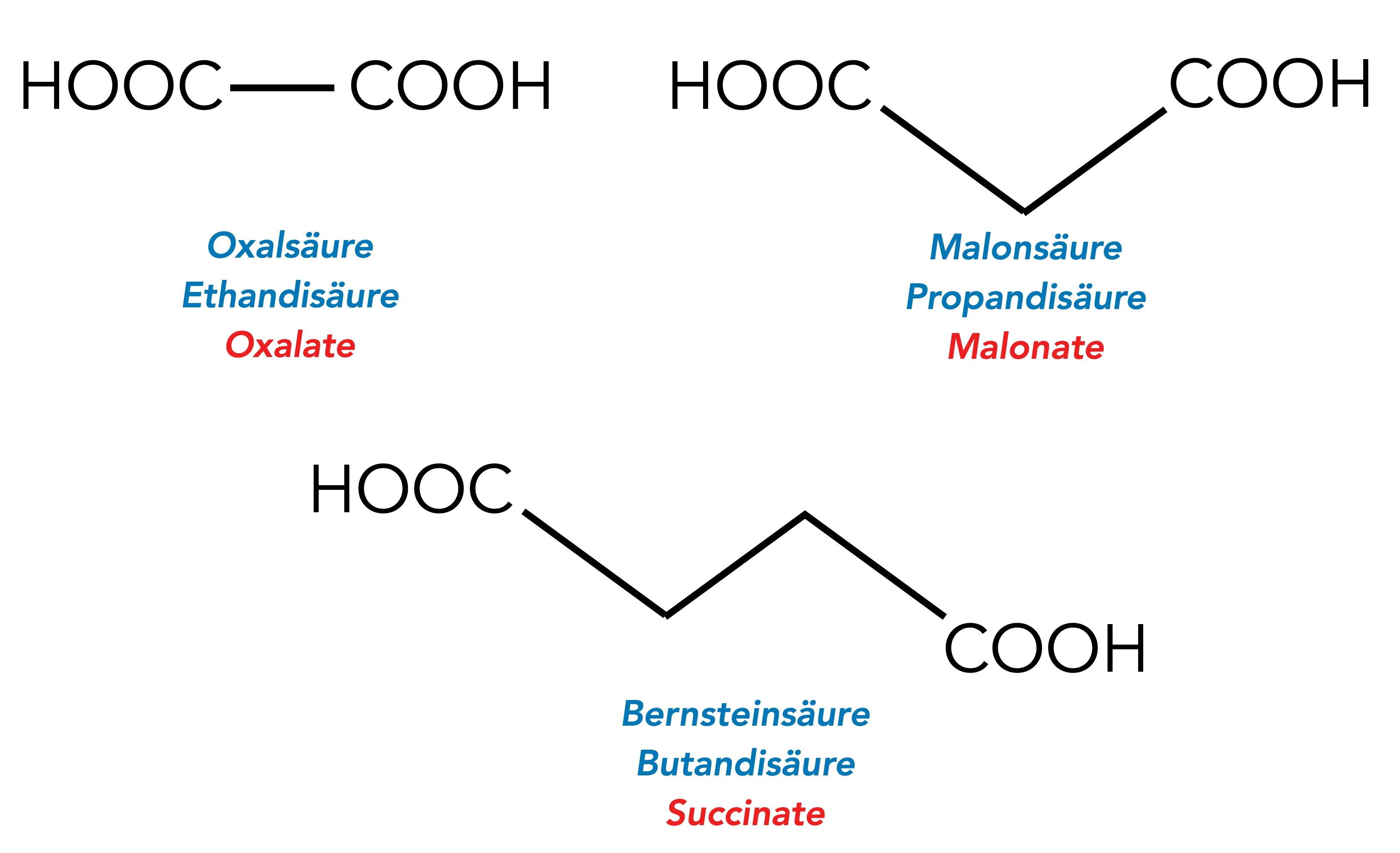
Drei Dicarbonsäuren: Oxal-, Malon- und Bernsteinsäure
Autor: Ulrich Helmich 02/2025, Lizenz: Public domain
Dieses Bild zeigt drei wichtige Dicarbonsäuren, die Oxalsäure, die Malonsäure und die Bernsteinsäure.
Oxalsäure
Die einfachste Dicarbonsäure ist die Oxalsäure, auch als Ethandisäure bezeichnet. Oxalsäure besteht quasi nur aus zwei miteinander verbundenen COOH-Gruppen und ist daher recht sauer - saurer zumindest als Ameisen- oder Essigsäure. Oxalsäure kommt bei unseren heimischen Gewächsen vor allem in in Rhabarber, Spinat und Sauerampfer vor - und für Kühe vielleicht interessant - in Sauerklee, der bekanntlich von Kühen nicht gefressen wird, weil er so sauer ist.
Malonsäure
Die Propandisäure kommt im Saft der Zuckerrübe vor, hat aber für die Lebensmitteltechnologie und die industrielle Chemie nur eine geringe Bedeutung. Nur 10 bis 100 Tonnen dieser Verbindung werden jährlich nach Europa importiert, für chemische Synthesen. Im Fettstoffwechsel des Menschen ist Malonsäure allerdings ein wichtiger Ausgangsstoff.
Bernsteinsäure
Bernsteinsäure oder Butandisäure ist die dritte Verbindung in der homologen Reihe der Dicarbonsäuren. Bernsteinsäure spielt eine wichtige Rolle im sogenannten Citratzyklus, einem zentralen Stoffwechselprozess in nahezu allen Lebewesen, mit dem Sie sich auch im Biologie-Unterricht beschäftigen werden.
In Europa ist Bernsteinsäure als Lebensmittelzusatzstoff (E 363) zugelassen, sie dient als Geschmacksverstärker für Desserts, Trockensuppen und Getränkepulver. In der chemischen Industrie ist sie ein wichtiger Ausgangsstoff für Synthesen - im Jahr werden laut Wikipedia ca. 15.000 Tonnen Bernsteinsäure verbraucht, vor allem zur Herstellung von Polymeren.
Zitronensäure
Zitronensäure ist eine Tricarbonsäure, enthält also drei COOH-Gruppen und ist daher so sauer, dass sie sogar in Haushaltsreinigern verwendet wird. Die IUPAC-Name der Zitronensäure ist 2-Hydroxy-1,2,3-propantricarbonsäure.
Stellen Sie sich ein Propan-Molekül vor, bei dem an jedem C-Atom noch eine COOH-Gruppe sitzt. Am mittleren C-Atom befindet sich zusätzlich noch eine OH-Gruppe.
Zitronensäure ist sogar eine der in Pflanzen am weitesten verbreiteten Säuren. Und nicht nur in Pflanzen, sogar in allen Zellen kommt Zitronensäure als essentieller und namensgebender Bestandteil des Zitronensäurezyklus (Citratzyklus) vor.
Zitronensäure wird in der Lebensmittelindustrie vielfältig eingesetzt, weil sie für den Menschen völlig harmlos ist und leicht aus Pflanzen gewonnen werden kann. In Limonaden, Gelees, Wein, Eiscreme, Marmeladen, Torten und so weiter findet sich Zitronensäure als Säuerungs- und Konservierungsmittel.
Aufgabe 1
Wenn man Oxalsäure erhitzt, entstehen zunächst Kohlendioxid und Ameisensäure. Erhitzt man weiter, bekommt man schließlich Kohlenmonoxid und Wasser.
a) Erstellen Sie die Reaktionsgleichungen für die beiden genannten Reaktionsschritte.
b) Begründen Sie, wieso Oxalsäure eine stärkere Säure ist als Essigsäure.
Eine Lösung dazu finden Sie hier...
Aufgabe 2*
*Nur für Schüler(innen), die sich bereits mit dem Citratzyklus auskennen (Biologie-Unterricht).
Erkläre die Rolle der Bernsteinsäure im Citratzyklus. Warum ist sie für den Energiestoffwechsel in Lebewesen so wichtig?
Hier finden Sie eine Lösung dieser Aufgabe ...
Hydroxycarbonsäuren
Wenn eine Carbonsäure zusätzlich zur COOH-Gruppe noch eine oder mehrere OH-Gruppen besitzt, bezeichnet man sie als Hydroxycarbonsäure. Die einfachste Hydroxycarbonsäure ist die Milchsäure bzw. 2-Hydroxypropansäure. Also eine Propansäure mit einer OH-Gruppe am mittleren C-Atom.
Milchsäure
Viele Milchprodukte enthalten Milchsäure. Durch Milchsäure-Gärung können dann Sauermilchprodukte wie Joghurt, Kefir und Buttermilch hergestellt werden. Auch Sauerkraut und Salzgurken werden durch Milchsäure-Gärung hergestellt.
Milchsäure ist auch ein beliebtes (weil relativ harmloses) Konservierungsmittel für Backwaren, Fertigsalate etc.
Äpfelsäure
Äpfelsäure gehört sowohl zu den Dicarbonsäuren wie auch zu den Hydroxycarbonsäuren, ihre Moleküle besitzen nämlich zwei COOH-Gruppen und eine OH-Gruppe.
Die 2-Hydroxybutandisäure kommt in unreifen Früchten vor, vor allem in Äpfeln, Weintrauben und Stachelbeeren. Sie wird aber auch als Lebensmittelzusatzstoff verwendet, ist aber recht teuer und daher als Säuerungs- oder Konservierungsmittel nicht allzu verbreitet.
Weinsäure
Bei der Weinsäure handelt es sich um eine Dicarbonsäure mit zwei zusätzlichen OH-Gruppen. Der IUPAC-Name der Weinsäure ist 2,3-Dihydroxy-Butandisäure.
Weinsäure findet sich in den Trauben (und Blättern) der Weinpflanze, aber auch in vielen anderen Pflanzen wie zum Beispiel Löwenzahn. In der Lebensmittelindustrie wird Weinsäure bei der Herstellung von Speiseeis, Kunsthonig, Obst, Limonaden und Erfrischungsgetränken verwendet.
Aufgabe 3
Erstellen Sie eine Tabelle, in der die abgekürzten Strukturformeln und die IUPAC-Namen von Milchsäure, Äpfelsäure und Weinsäure gegenübergestellt werden.
Aufgabe 4
Recherchieren Sie, in welchen Lebensmitteln Hydroxycarbonsäuren als Zusatzstoffe verwendet werden und welche Funktionen sie dort übernehmen.
Zwei Lösungsvorschlänge von DeepSeek und ChatGPT finden Sie auf dieser Seite...
Aminosäuren
Diese wichtigen Verbindungen kennen Sie sicherlich aus dem Biologie-Unterricht. Aminosäuren sind die Bausteine aller Peptide und Proteine. Peptide bestehen aus wenigen Aminosäuren (2 bis 100), Proteine aus mehr als 100 bis einigen 1000 Aminosäuren.
Aminosäuren sind Carbonsäuren, die eine oder zwei zusätzliche Amino-Gruppen enthalten - NH2-Gruppen also.
Die einfachste Aminosäure ist das Glycin - ein Essigsäure-Molekül, bei dem ein H-Atom der CH3-Gruppe durch eine NH2-Gruppe ersetzt wurde.
In der Biologie-Abteilung dieser Homepage gibt es ein ganzes Kapitel zu diesem Thema. Hier werden alle 20 Aminosäuren eingehend vorgestellt, die eine wichtige Rolle in Lebewesen spielen.
Während die COOH-Gruppe einer Aminosäure saure Eigenschaften im Sinne von Brönsted besitzt (also ein Protonen-Donator) ist, hat die NH2-Gruppe einer Aminosäure basische Eigenschaften im Sinne von Brönsted (ist also ein Protonen-Akezptor).
Aufgabe 5
a) Recherchieren und zeichnen Sie die Strukturformel der Aminosäure Alanin. Kennzeichnen Sie die funktionellen Gruppen der Aminosäure und markieren Sie den sogenannten Aminosäure-Rest bzw. die Aminosäure-Seitenkette.
b) Bei einem bestimmten pH-Wert liegen die Moleküle einer Aminosäuren als sogenanntes Zwitterion vor. Recherchieren Sie, was das bedeutet, und stellen Sie graphisch mit zwei Strukturformeln da, wie aus der Aminosäure Glycin ein Zwitterion wird. Erläutern Sie Ihre Abbildung kurz.
Auch für diese Aufgabe gibt es einen Lösungsvorschlag...