Inhaltliche Schwerpunkte
Auf dieser Seite werden folgende inhaltliche Schwerpunkte* berücksichtigt:
- funktionelle Gruppen verschiedener Stoffklassen und ihre Nachweise:
Hydroxy-Gruppe, Carbonyl-Gruppe,Carboxy-Gruppe und Ester-Gruppe - Oxidationsreihe der Alkanole:
Oxidationszahlen
*nach dem Kernlehrplan des Landes NRW 2022
Aldehyde sind oxidierbar, denn das H-Atom der Aldehyd-Gruppe kann durch eine Hydroxy-Gruppe ersetzt werden, dann entsteht eine Carbonsäure. Ketone dagegen haben kein H-Atom an der Carbonyl-Gruppe, so dass hier auch keine weitere Oxidation stattfinden kann (es sei denn durch Verbrennung, wobei dann Kohlendioxid und Wasser entstehen).
Die Nachweismethoden für Aldehyde beruhen in der Regel auf dieser Oxidierbarkeit der Aldehydgruppe. Als Oxidationsmittel werden dabei meistens Metall-Ionen eingesetzt, die während der Reaktion reduziert werden. Drei dieser Nachweismethoden sind besonders bekannt.
Eine einfache "Nachweisreaktion" haben wir bereits kennengelernt, als wir primäre und sekundäre Alkohole mit Kupferoxid oxidiert haben. Das schwarze mit CuO überzogene Kupferblech wurde sofort nach dem Eintauchen in den flüssigen Alkohol wieder blank, weil das CuO zu elementarem Kupfer reduziert wurde.
Im Folgenden wollen wir uns mit "richtigen" Nachweisreaktionen für Aldehyde beschäftigen, die auch für Fächer wie Biologie oder Ernährungslehre interessant sind, denn viele Kohlenhydrate sind ebenfalls Aldehyde (oder Ketone).
Die FEHLING-Probe
Die wohl bekannteste Nachweisreaktion für die Aldehyd-Gruppe ist die Fehling-Probe.
Bei dieser Fehling-Probe werden die Aldehyde mit Hilfe von zweiwertigen Kupfer-Ionen oxidiert, die ihrerseits zu einwertigen Kupfer-Ionen reduziert werden.
Auf dieser Seite wird der Versuch zur Fehling-Probe beschrieben (nur die Durchführung).
Erläuterungen zum Versuch
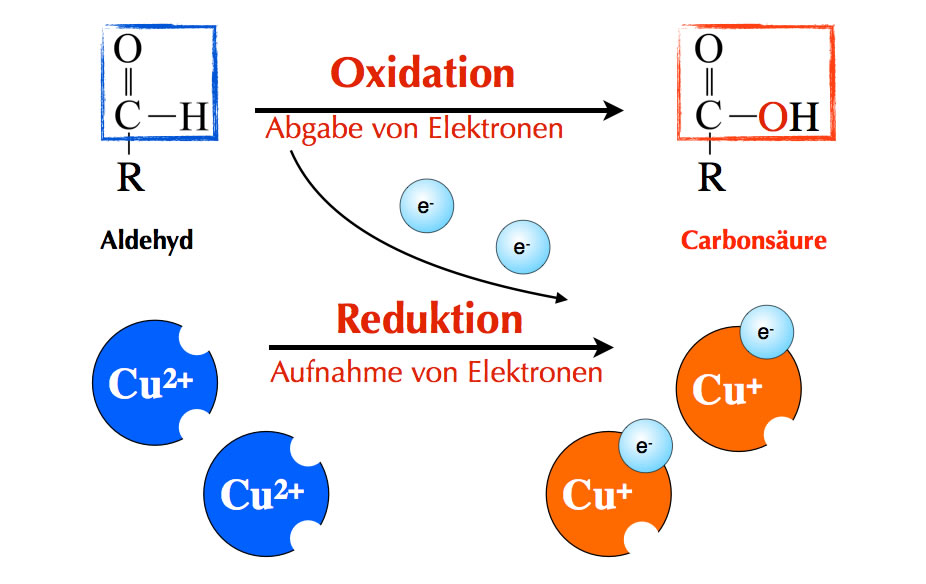
Reaktionsschema für die Fehling-Probe mit einem Aldehyd und Cu2+-Ionen
(C) Ulrich Helmich 2018, Lizenz: Public domain
Die zweiwertigen Kupfer-Ionen haben eine blaue Farbe, die einwertigen Kupfer-Ionen dagegen eine rote Farbe, so dass man am Farbumschlag von tiefblau nach orangerot gut erkennen kann, ob die Probe positiv verlaufen ist.
Die TOLLENS-Probe
Eine andere bekannte Nachweismethode ist die Tollens-Probe, auch als Silberspiegelprobe bekannt. Bei dieser Redoxreaktion werden einwertige Silber-Ionen zu metallischem Silber reduziert. Wenn man den Versuch korrekt in einem Reagenzglas durchführt, erhält man einen wunderschönen Silberspiegel auf der Innenwand des Glases:

Ein Silberspiegel an der Innenwand eines Reagenzglases
Tmv23, CC BY-SA 3.0, via Wikimedia Commons
Hier sehen wir einen solchen Silberspiegel. Schauen wir uns nun die entsprechende Reaktion an:
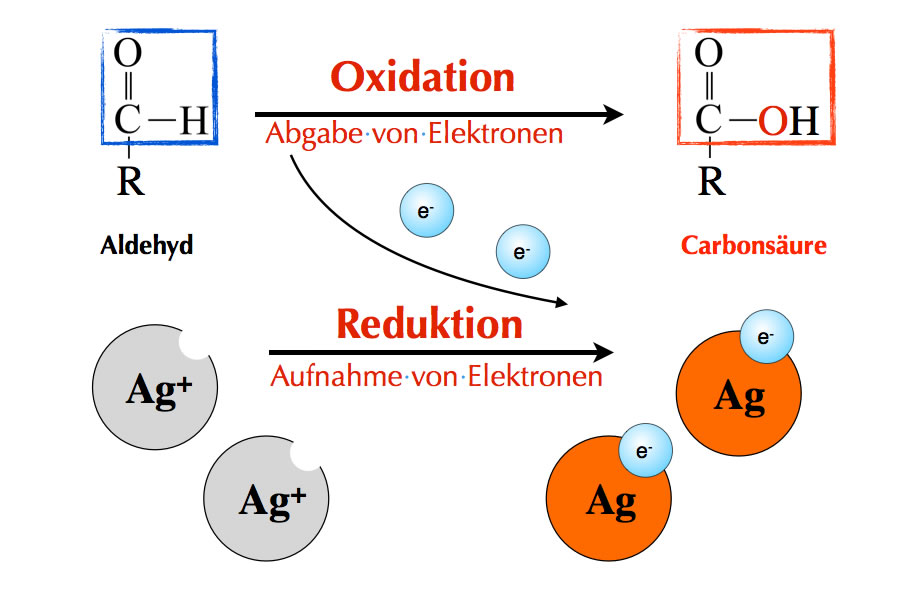
Die Tollens-Probe beruht auf der Reduktion von Ag+-Ionen zu Ag-Atomen
(C) Ulrich Helmich 2018, Lizenz: Public domain
Aufgabe 1
In die Abbildungen 1 und 3 hat sich noch ein "kleiner" Fehler eingeschlichen. Können Sie feststellen, was hier noch nicht ganz korrekt ist?
Lösung
Wo kommen die Sauerstoff-Atome der sich bildenden Carboxy-Gruppe -COOH her? Das kann man aus den beiden Reaktionsschemata für die Fehling- und die Tollens-Probe noch nicht entnehmen.
Aufgabe 2
Damit die "Gleichung" bei der Tollens-Probe aufgeht, müssen auf der linken Seite noch zwei Hydroxid-Ionen zugefügt werden.
Stellen Sie mit Hilfe dieser neuen Information nun die korrekte und vollständige Reaktionsgleichung für die Tollens-Probe auf.
Eine Lösung finden Sie auf der entsprechenden Seite der Wikipedia.
Aufgabe 3
Recherchieren Sie nun die korrekte und vollständige Reaktionsgleichung für die Fehling-Probe.
Eine Lösungshilfe finden Sie auf der entsprechenden Seite im Chemie-Lexikon auf dieser Homepage
Die SCHIFF-Probe
Diese Probe ist ein Nachweisverfahren speziell für Aldehyde. Sie zu erklären, wäre an dieser Stelle etwas zu aufwändig. Die Probe beruht nicht auf der Oxidation der Aldehyd-Gruppe. Bei der SCHIFF-Probe wird der rote Farbstoff Fuchsin mit Schwefelsäure versetzt, wobei sich ein komplexeres farbloses Molekül bildet, das Schwefel enthält. Gibt man nun einen Aldehyd zu diesem farblosen Stoff, verbinden sich zwei Aldehyd-Moleküle mit diesem farblosen Molekül. Es finden dann weitere komplexe Reaktionsschritte statt, die schließlich zu einem rot-violetten Molekül führen. Einzelheiten finden sich in der Wikipedia, in dem Praktikumsprotokoll auf www.chids.de oder auf der Seite der Uni Bayreuth.
Wie ich gerade auf der Seilnacht-Seite lese, sollte diese Probe an Schulen "aufgrund des krebserzeugenden Potenzials von Fuchsin" nicht mehr durchgeführt werden.