Die Reaktion
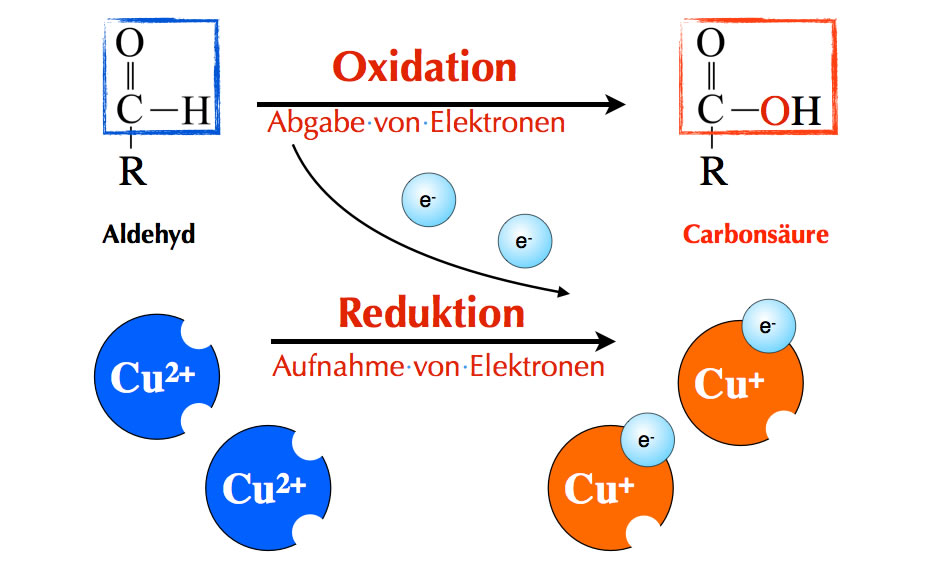
Die Fehling-Probe ist ein Nachweis auf die Aldehyd-Gruppe und beruht auf der Tatsache, dass die Aldehyd-Gruppe einer organischen Verbindung oxidiert werden kann, während beispielsweise eine Keto-Gruppe oder eine Carboxy-Gruppe nicht mehr weiter oxidiert werden kann.
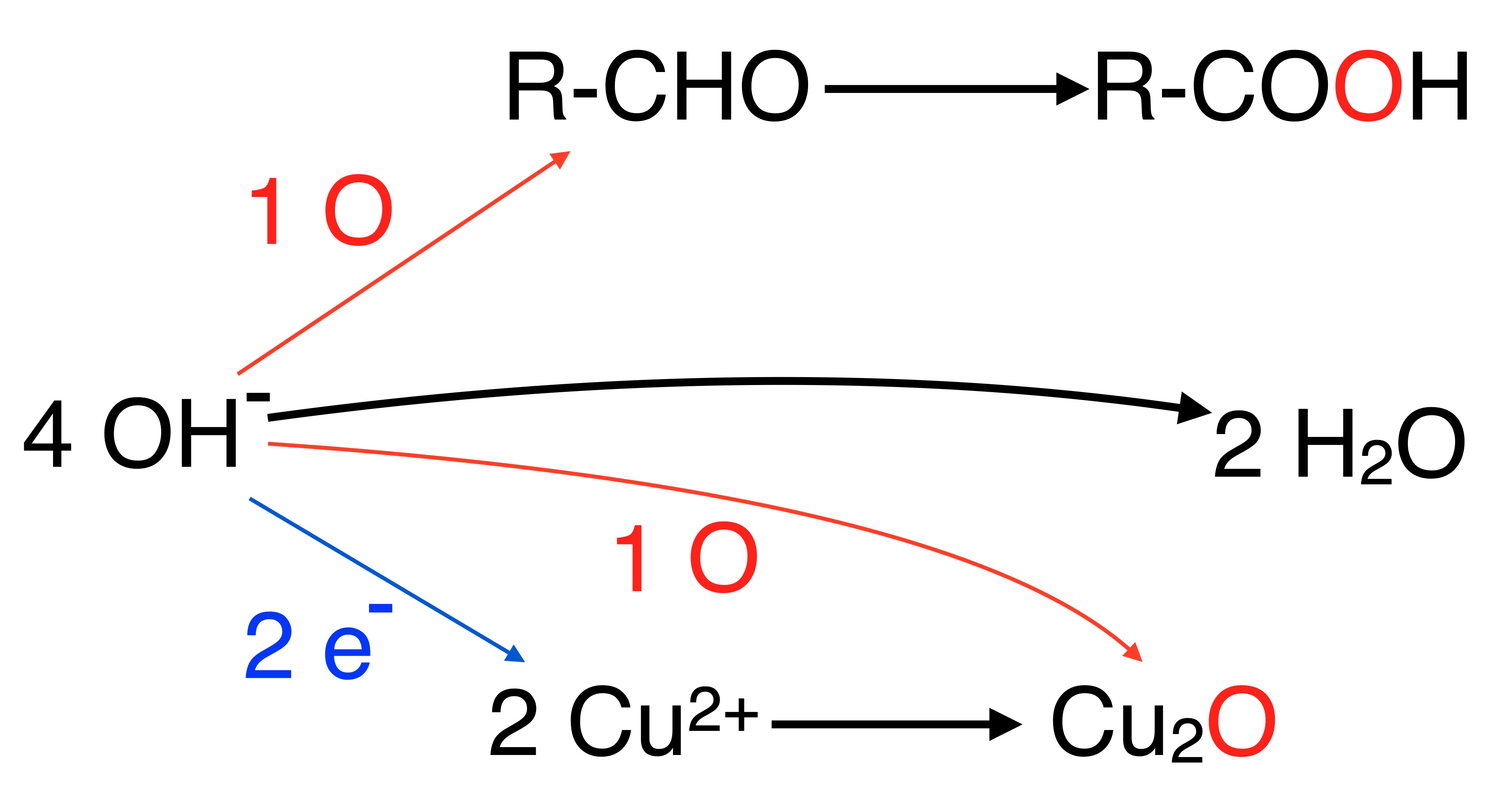
Die Fehling 1 - Lösung enthält Natriumhydroxid. Welche Rolle die Hydroxid-Ionen bei der Fehling-Reaktion spielen, kann man diesem Schema entnehmen. Insgesamt werden 4 OH- benötigt. Von den vier O-Atomen wird eins in die Aldehyd-Gruppe -CHO eingefügt, die dann zur Carboxy-Gruppe -COOH oxidiert wird. Ein zweites O-Atom reagiert mit den Kupfer(II)-Kationen zum Cu2O mit Kupfer(I)-Kationen. Die beiden übrig gebliebenen O-Atome reagieren mit den vier H-Atomen zu zwei H2O-Molekülen.
Durchführung
Bei der Fehling-Probe gibt man die zu analysierende Substanz in flüssiger oder in Wasser gelöster Form in ein Reagenzglas. Anschließend gibt man gleiche Mengen der beiden Fehling-Lösungen Fehling 1 und Fehling 2 dazu. Bei Fehling 1 handelt es sich um nichts anderes als um eine Kupfersulfat-Lösung, während Fehling 2 eine mit Natronlauge angereicherte Kaliumnatriumtartrat-Lösung ist. Kaliumnatriumtartrat ist das Kalium-Natrium-Salz der Weinsäure.
Auf dieser Seite wird die Durchführung der Fehling-Probe genau beschrieben, allerdings in einer sehr allgemeinen Form.
Bei der Fehling-Reaktion gibt die Aldehyd-Gruppe zwei Elektronen ab, die dann von den zweiwertigen Kupfer-Ionen (blau) aufgenommen werden. Allerdings nimmt jedes Cu2+-Ion nur ein Elektron auf. Bei dieser Reduktion entstehen dann die rotbraunen Cu+-Ionen. Diese roten Ionen sind dann für die Rotfärbung im Reagenzglas verantwortlich, wenn die Fehling-Probe positiv ausfällt. Lässt man die Reaktion noch länger laufen, bildet sich auch metallisches Kupfer.
Nachweis von Glucose mit der Fehling-Probe
Die Glucose-Nachweis mit Cu2+-Ionen wurde ursprünglich von Herrmann Fehling im Jahre 1848 veröffentlicht. Er entwickelte die Nachweisreaktion zur Diagnose der Zuckerkrankheit, wahrscheinlich weil er keine Lust mehr hatte, den Urin seiner Patienten mit seinem Mund auf hohen Zuckergehalt zu überprüfen, wie es damals durchaus üblich war.
Die Erklärung für die Reaktion der Glucose, die man in vielen Schulbüchern heute findet, ist allerdings falsch. Die Glucose wird bei der Reaktion nicht zu Gluconsäure oxidiert, sondern zu 2-Ketoglucose. Die Aldehyd-Gruppe am ersten C-Atom bleibt also erhalten, aber am zweiten C-Atom bildet sich eine Keto-Gruppe. Im weiteren Verlauf der Reaktion kann sich dieses Reaktionsprodukt zu anderen Verbindungen umlagern oder noch weiter oxidiert werden.
Die Cu2+-Ionen werden zunächst zu Cu+ reduziert, erhitzt man die Probe aber länger, entsteht auch metallisches Kupfer Cu(s).
Alternativen zur Fehling-Probe
In fast jedem bekannten Chemiebuch der Mittelstufe und Oberstufe wird die Fehling-Probe behandelt und teils sogar als Schülerversuch dargestellt. Nun ist die Fehling-II-Lösung aber stark alkalisch, so dass hier ein hohes Sicherheitsrisiko für die Schüler(innen) vorliegt. Es empfiehlt sich daher, die Fehling-Probe durch eine gleich gute, aber deutlich sichere Nachweismethode zu ersetzen.
Empfohlen wird hier in der Regel die Benedict-Reaktion, die 1908 von Stanley Benedict erfunden wurde und ebenfalls auf der Reduktion von Cu2+-Ionen basiert. Der Vorteil bei der Benedict-Probe ist ein doppelter: Erstens wird nur ein Reagenz benötigt (und nicht zwei wie bei der Fehling-Probe), und zweitens ist das Reagenz nur sehr schwach alkalisch, da statt Natriumhydroxid das weniger gefährliche Natriumcarbonat verwendet wird.
Diese Wikipedia-Seite erläutert die Zusammensetzung und die Anwendung des Benedict-Reagenz.
Ein sehr schöner und übersichtlicher Artikel von Klaus Ruppersberg et al. mit einer Darstellung vieler verschiedener Nachweismethoden für Kohlenhydrate.