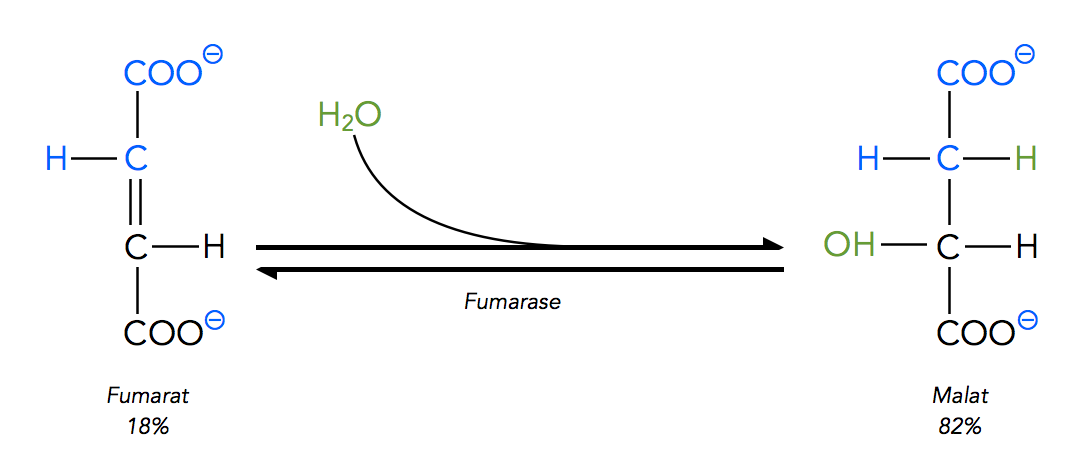
Schritt 8: Fumarat + H2O → Malat
Autor: Ulrich Helmich 2017, Lizenz: siehe Seitenende.
Im Schritt 7 verlor das Succinat-Molekül zwei H-Atome an das Coenzym FAD. Dadurch bildete sich eine C=C-Doppelbindung im Fumarat-Molekül.
Durch die Anlagerung eines Wasser-Moleküls an diese C=C-Doppelbindung entsteht eine OH-Gruppe im Malat-Molekül, die im nächsten Schritt leicht oxidiert werden kann, wobei dann noch einmal Wasserstoff freigesetzt wird.
Das Enzym, welches diesen Schritt katalysiert, heißt Fumarase.
Für Chemie-Profis:
Bei dieser Reaktion handelt es sich um nucleophile Addition. Aus dem Chemie-Unterricht kennen Sie sicherlich die Addition von Wasser an ein Alken. Hier greift zunächst ein Proton H+ die C=C-Doppelbindung an und bildet ein Carbenium-Ion als Zwischenprodukt. An dieses Carbenium-Ion setzt sich dann ein Hydroxid-Ion, und fertig ist die Addition.
Bei der Bildung von Malat greift dagegen zuerst das Hydroxid-Ion die C=C-Doppelbindung an. Durch die beiden COO--Gruppen, die ja stark elektronenziehend sind, ist die C=C-Doppelbindung im Fumarat recht elektronenarm. Daher ist sie ein Angriffsziel für Nucleophile wie zum Beispiel das OH--Ion. Als Zwischenprodukt bildet sich dann ein Carbanion (negativ geladenes C-Atom mit einem freien Elektronenpaar). An dieses Carbanion lagert sich dann ein Proton an [1].
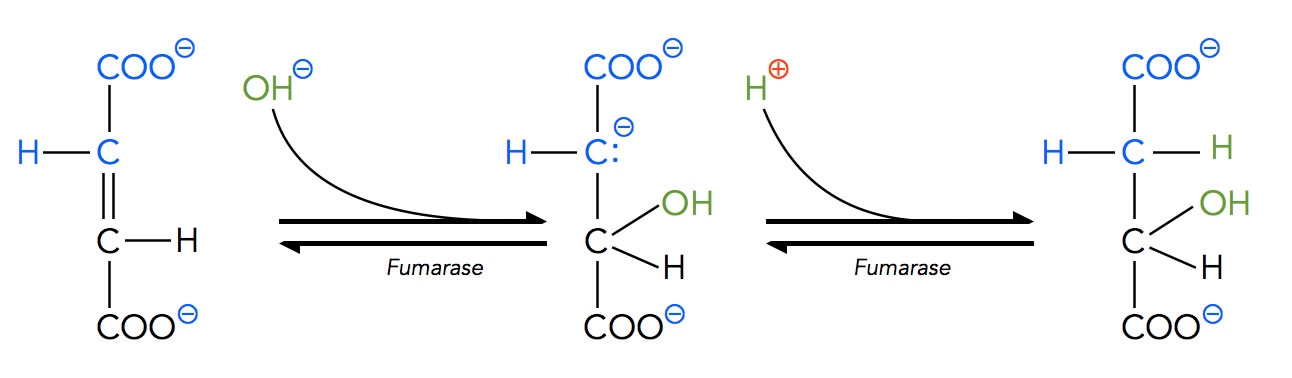
Der Schritt 8 als nucleophile Addition
Autor: Ulrich Helmich 2022, Lizenz: siehe Seitenende
Die Umkehrreaktion wäre dann eine basenkatalysierte Eliminierung nach dem E2-Mechanismus: Eine starke Base zieht ein Proton aus dem Malat-Molekül heraus, dabei entsteht das Carbanion als Zwischenprodukt, und schließlich spaltet sich ein Hydroxid-Ion ab, und fertig ist das Fumarat. In einer lebenden Zelle liegt das Gleichgewicht dieser Umsetzung auf Seiten des Malats (zu 82%) [4]. Die freie Energie ΔG dieser Reaktion liegt bei -3,8 kJ/mol [1].
Quellen:
- Nelson, Cox. LEHNINGER Principles of Biochemistry. Macmillan Learning, New York 2021.
- Berg, Tymoczko, Gatto jr., Stryer: Stryer Biochemie, 8. Auflage, Springer Berlin Heidelberg 2018.
- engl. Wikipedia, Artikel "Fumarase".
- Chemgapedia, Artikel "Fumarat-Hydratase".
Seitenanfang -
Weiter mit Schritt 9 ...
Zurück zur Übersicht ...