Addition von H2O an Alkene
An einfache Alkene kann Wasser mit wenig Aufwand addiert werden, eine Ansäuerung der Reaktionslösung mit Schwefelsäure reicht dazu meistens aus.
Gehen Sie auf diese Seite, um etwas über die Grundlagen der Wasser-Addition an Alkene zu erfahren.
Will man einen Alkohol aus einem komplexeren Alken herstellen, wendet man oft das Verfahren der Oxymercurierung an. Dazu wird Quecksilberacetat (CH3COO)Hg eingesetzt.
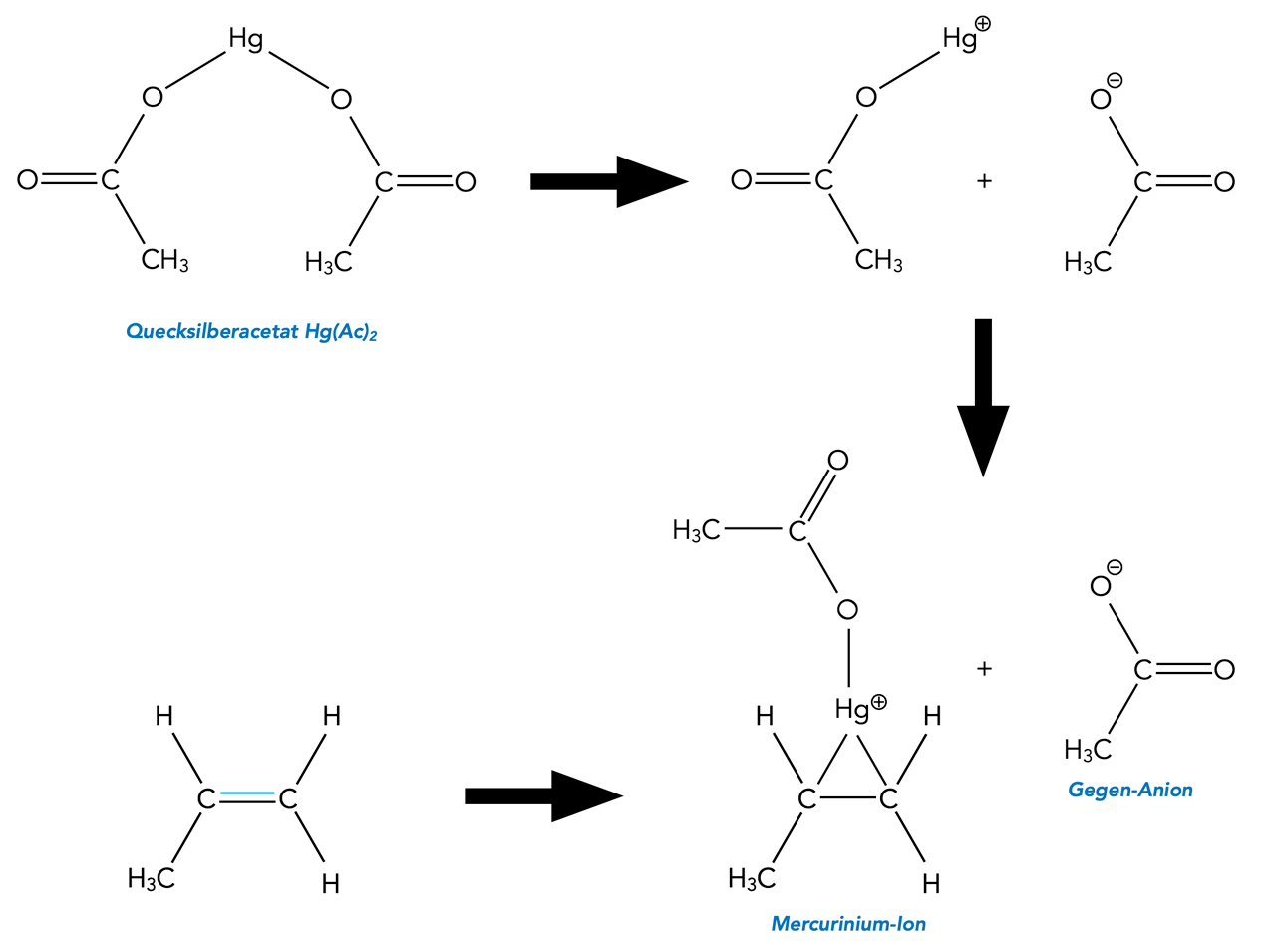
Bildung der Mercurinium-Ions
Autor: Ulrich Helmich 2022, Lizenz: Public domain
Das Quecksilberacetat zerfällt in ein Acetat-Ion Ac- und ein HgAc+-Kation. Das HgAc+-Kation setzt sich nun - ähnlich wie ein Br+-Kation bei der Bromierung - an die C=C-Doppelbindung. Es entsteht das Mercurinium-Ion (in Analogie zum Bromonium-Ion). In der Lösung ist dieses Kation mit dem Gegen-Anion assoziiert, dem Acetat-Ion.
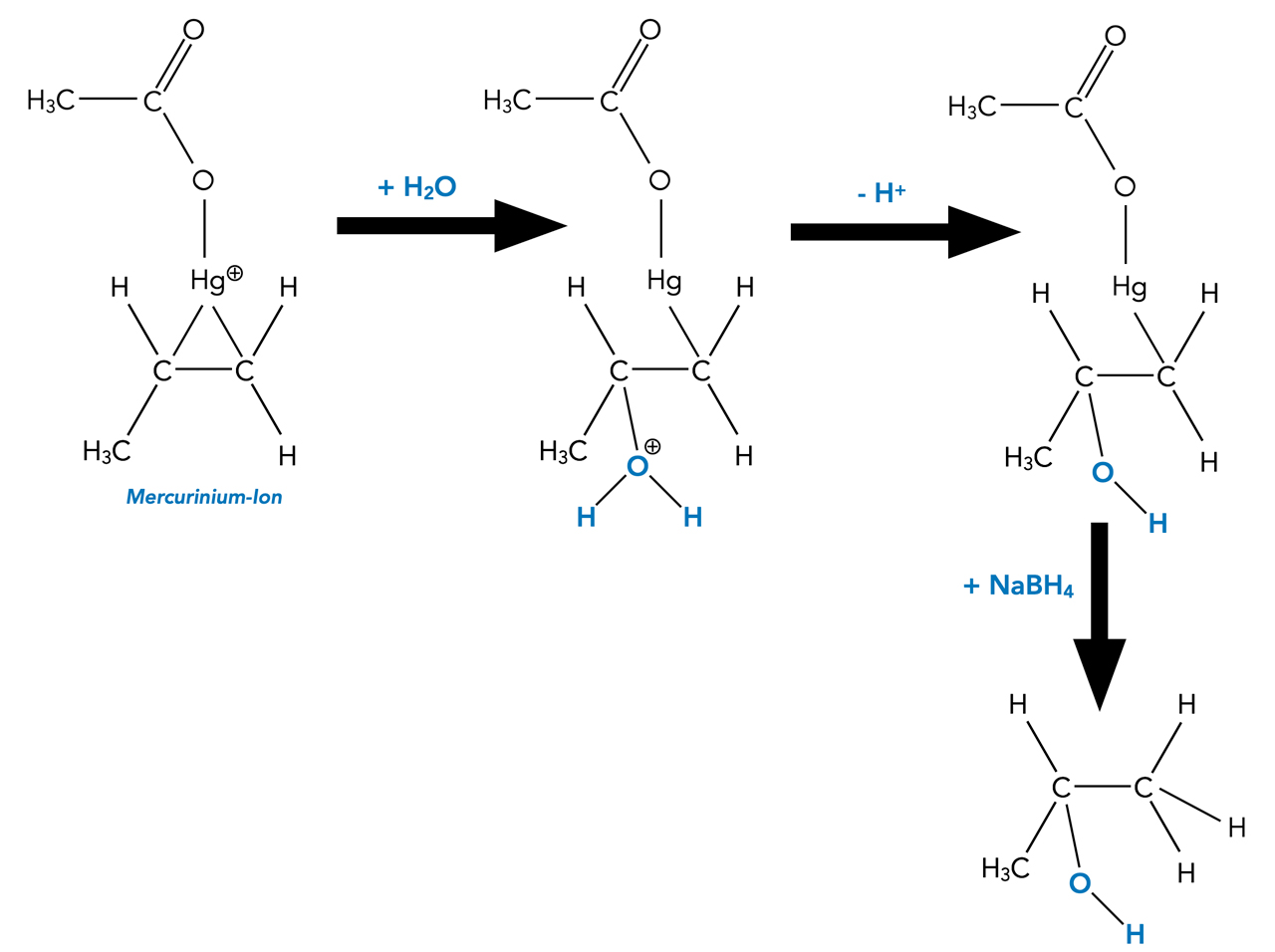
Bildung des Alkohols und Demercurierung mit NaBH4
Autor: Ulrich Helmich 2022, Lizenz: Public domain
Es erfolgt nun ein Rückseitenangriff von Wasser, dabei wird das C-Atom der ehemaligen Doppelbindung angegriffen, das durch +I-Effekte am stärksten stabilisiert wird. In unserem Fall handelt es sich um das "linke" C-Atom der C=C-Doppelbindung; dieses C-Atom wird durch die Methylgruppe stabilisiert.
Es bildet sich eine Art Oxonium-Ion ROH2+, durch Abspaltung eines Protons entsteht dann der Alkohol und wir sind fast fertig. Der Alkohol ist aber noch mit dem Quecksilber/Acetat-Rest verbunden. Hier führt man dann eine Reduktion mit NaBH4 (Natriumborhydrid) durch, und fertig ist der Alkohol. Diesen letzten Reaktionsschritt bezeichnet man übrigens als Demercurierung.
In dem hier gezeigten Beispiel ergibt die Oxymercurierung den so genannten Markovnikov-Alkohol, also denjenigen Alkohol, den man nach der Markovnikov-Regel erwarten würde.
Bei der Demercurierung bildet sich elementares Quecksilber, das dann in Form von kleinen Kügelchen im Reaktionsgefäß vorliegt. Weil Quecksilber ein hochgiftiges Schwermetall ist, ist die Oxymercurierung nicht für den industriellen Maßstab geeignet, sondern findet nur gelegentlich im Labor Anwendung, und auch das nur mit höchster Vorsicht.
Quellen und weiterführende Bücher und Artikel, die über allgemeines Schulbuchwissen hinausgehen:
- M. A. Fox, J. K. Whitesell: Organische Chemie - Grundlagen, Mechanismen, bioorganische Anwendungen. 1. Auflage, Heidelberg 1995.
- K. P. C. Vollhard, N.E. Schore: Organische Chemie. 6. Auflage, Weinheim 2020.
- J. Clayden, N. Greeves, S. Warren: Organische Chemie. Berlin 2013.
- R. T. Morrison, R. N. Boyd, S. K. Bhattacharjee: Organic Chemistry. 7. Auflage, Dorling Kindersley 2011.
- Reinhard Brückner, Reaktionsmechanismen, 3. Auflage, Springer-Verlag 2014.
- Organikum, 22. Auflage, Weinheim 2004.
- J. Falbe, M. Regitz (Herausgeber): Römpp Chemie Lexikon in 6 Bänden. 9. Auflage, Stuttgart, New York 1989-1992.
- Dyker-Vorlesung "Organische Chemie 1", Folge 32 (auf Tib AV - Portal verfügbar).