Betrachten Sie die Strukturformeln folgender vier Butene:
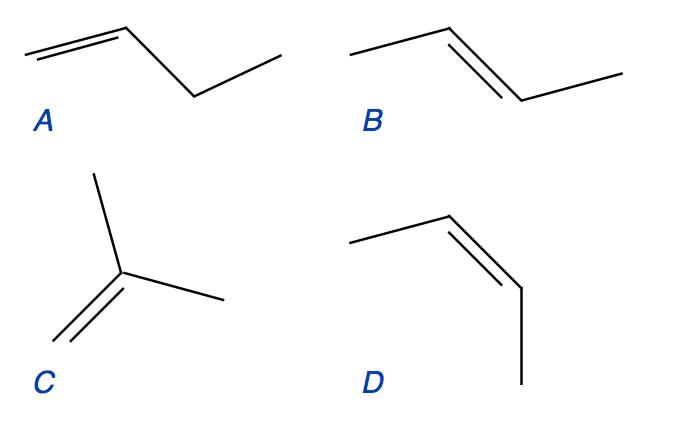
-
Geben Sie die korrekten IUPAC-Namen dieser vier Butene an.
- Erläutern Sie an diesem Beispiel, welche Art von Isomerie hier jeweils vorliegt.
- Die vier Butene haben unterschiedliche Siedepunkte. Geben Sie eine mögliche Reihenfolge dieser Siedepunkt an und begründen Sie Ihre Wahl.
Lösung
1. Namen der vier Butene
A) 1-Buten oder But-1-en, B) trans-2-Buten oder trans-But-2-en, C) 2-Methylpropen, D) cis-2-Buten oder cis-But-2-en.
2- Isomerie
Unter Isomerie versteht man allgemein, dass es von einer Verbindung mit einer bestimmten Summenformel mehrere unterschiedliche Strukturen gibt. Die Summenformel aller vier Butene ist C4H8.
Konstitutions-Isomere besitzen die gleiche Summenformel, haben aber eine unterschiedliche chemische Struktur, in der die Atome anderes miteinander verknüpft sind. Die Butene A, B und D haben das gleiche Grundgerüst, bei dem vier C-Atome zu einer linearen Kette verknüpft sind. Das Buten C hat ein völlig anderes Grundgerüst, hier sind nur drei C-Atome zu einer Kette verknüpft, am mittleren C-Atom ist eine Verzweigung zu finden, die dann zum vierten C-Atom führt. Diese Art von Konstitutions-Isomerie wird übrigens als Rumpfisomerie, Skelettisomerie oder Strukturisomerie bezeichnet.
Als Stellungsisomerie oder Positionsisomerie bezeichnet man Konstitutions-Isomere, die zwar das gleiche Grundgerüst haben, bei denen sich aber die funktionelle Gruppe an einer anderen Position befindet. Das könnte hier bei den Butenen A und B/C der Fall sein. Bei A befindet sich die C=C-Doppelbindung an der Position 1, bei B/C an der Position 2. Allerdings ist eine C=C-Doppelbindung keine "richtige" funktionelle Gruppe. Der Begriff Bindungsisomerie wäre hier etwas genauer. Bei der Bindungsisomerie ist das Kohlenstoff-Grundgerüst das gleiche, auch die funktionellen Gruppen sind identisch. Bindungsisomere unterscheiden sich aber in der Lage von Doppel- und Dreifachbindungen.
Kommen wir nun zu den beiden Strukturen B und D. Beide Butene haben das gleiche Grundgerüst, und auch die Stellung der Doppelbindung ist gleich. Trotzdem unterscheiden sich die beiden Moleküle, wie man leicht mit Hilfe eines Molekülbaukastens nachvollziehen kann. Wir haben es hier mit einer Stereoisomerie zu tun. Bei der Stereoisomerie handelt es sich um eine Art der Isomerie, bei der die Isomere die gleiche Konstitution (Struktur, Art und Weise, in der die Atome miteinander verknüpft sind) besitzen, sich aber in der räumlichen Anordnung der Atome unterscheiden. B und D verhalten sich nicht wie Bild und Spiegelbild, sind also keine Enantiomere. Vielmehr handelt es sich um die cis-trans-Isomerie, die übrigens nicht nur bei C=C-Doppelbindungen auftritt, sondern auch bei zyklischen Verbindungen wie 1,2-Dibromcyclohexan, also immer dann, wenn die freie Drehbarkeit um C-C-Bindungen aufgehoben ist.
3. Siedepunkte
Den niedrigsten Siedepunkt sollte die Struktur C haben. Das Molekül C hat eine nahezu "kugelförmige" Gestalt, das heißt, die Kontaktfläche zwischen den Molekülen von C ist sehr gering, was dann zu schwachen van-der-Waals-Bindungen führt.
Den höchsten Siedepunkt sollte die Struktur D haben. Die beiden Methylgruppen befinden sich hier auf der gleichen Seite der Doppelbindung, wo sie Elektronen "hinschieben". Alkylgruppen haben nämlich einen +I-Effekt. Die beiden Methylgruppen "schieben" die Elektronen in die gleiche Richtung, somit verstärken sich die so erzeugten Dipolmomente gegenseitig, und das ganze Molekül ist ein stärkerer Dipol als beispielsweise Struktur D, wo sich die Effekte der beiden Methylgruppen aufheben. Diese stärkere Dipoleigenschaft sollte dann zu einem relativ hohen Siedepunkt führen.
Die Siedepunkte der beiden anderen Strukuren sind schlecht abzuschätzen. Der Siedepunkt von B ist auf jeden Fall niedriger als der von D, und der Siedepunkt von A ist auf jeden Fall höher als der von C. Somit ergibt sich die Reihenfolge
D > A/B > C
Faktencheck
Die tatsächlichen Siedepunkte sind:
A) -6,2 ºC, B) 0,9 ºC, C) -7,1 ºC, D) 3,7 ºC
also gilt
D > B > A > C