Lernziele
Wenn Sie diese Seite durchgearbeitet haben, sollten Sie wissen
- dass der HOMO-LUMO-Abstand mit zunehmender Anzahl konjugierter C=C-Doppelbindung im Polyen immer kleiner wird,
- dass daher immer energieärmeres und langwelligeres Licht für den HOMO->LUMO-Übergang benötigt wird,
- dass bei 9 konjugierten C=C-Doppelbindungen Polyene zum ersten Mal sichtbares Licht absorbieren und dem menschlichen Auge daher farbig erscheinen (schwach gelb).
Absorption von UV-Licht
Hexatrien ist eine Verbindung mit sechs hintereinander liegenden sp2-hybridisierten C-Atomen, daher gibt es sechs pz-Orbitale, die überlappen können. Folglich existieren auch sechs verschiedene π-Molekülorbitale, drei bindende und drei anti-bindende. Im Normalzustand (also im nicht-angeregten Grundzustand) sind die drei bindenden Molekülorbitale mit den sechs π-Elektronen besetzt, während die drei anti-bindenden Molekülorbitale leer sind.
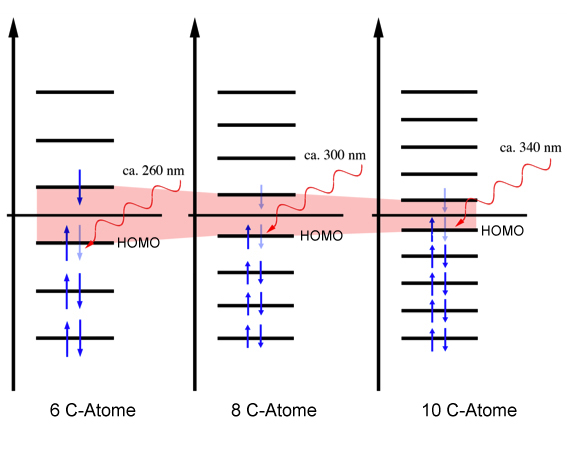
Energiediagramm der Molekülorbitale des Hexatriens sowie der beiden folgenden Polyene mit 8 und 10 C-Atomen.
Wurde für den HOMO -> LUMO-Übergang des Butadiens noch kurzwelliges UV-Licht der Wellenlänge 217 nm benötigt, so sind beim Hexatrien "nur" 260 nm Wellenlänge erforderlich. Der Abstand zwischen HOMO und LUMO ist beim Hexatrien etwas geringer als beim Butadien.
Und wie man auf Abbildung 1 gut erkennen kann, setzt sich diese Tendenz fort, je länger die Kette der C-Atome wird - konjugierte Doppelbindungen vorausgesetzt.
Bei 9 konjugierten Doppelbindungen (also 18 sp2-hybridisierten C-Atomen) wird zum ersten Mal sichtbares Licht absorbiert.
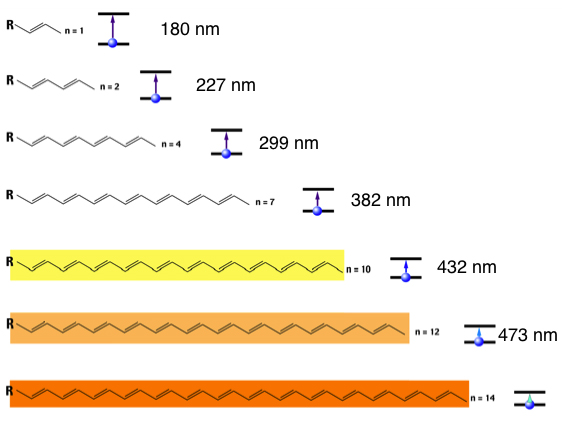
HOMO-LUMO-Abstand bei verschiedenen Polyenen mit bis zu 14 Doppelbindungen
Diese Graphik zeigt den gleichen Sachverhalt noch einmal aus einer etwas anderen Perspektive. Dargestellt sind die Strukturformeln einiger Polyene der Art H3C-(CH=CH)n-CH3, angefangen mit But-2-en (n = 1) über Hexa-2,4-dien und so weiter, wenn man R = CH3 setzt. Polyene mit 10 konjugierten C=C-Doppelbindungen absorbieren sichtbares Licht der Wellenlänge 432 nm, das ist violettes Licht. Die Komplementärfarbe ist gelb, daher erscheinen uns solche Polyene gelb. Wir haben mit n = 10 das erste farbige Polyen vor uns.
Exkurs: Carotinoide
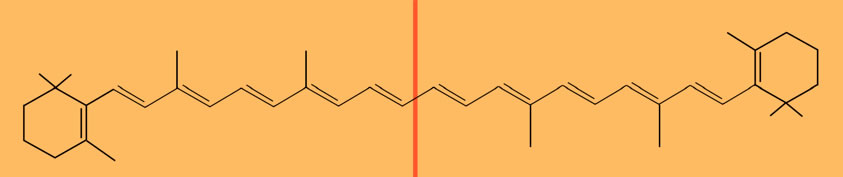
Das ß-Carotin-Molekül
Das ß-Carotin-Molekül ist symmetrisch aufgebaut. Es besitzt 12 konjugierte Doppelbindungen und absorbiert blaues Licht. Daher erscheint ß-Carotin orangerot.
In der Natur kommen ca. 600 Farbstoffe mit ähnlicher Struktur vor, sie werden zur Gruppe der Carotinoide zusammengefasst.
Viele Früchte und Beeren enthalten Carotinoide, aber auch in den grünen Blättern sind sie enthalten. Bestimmte Carotinoide schützen die Pflanzen vor UV-Licht, in dem sie dieses absorbieren.
Einige Carotinoide werden vom menschlichen Körper zur Produktion des Sehfarbstoffs Retinal benötigt. Sie müssen mit der Nahrung als Vitamin A aufgenommen werden.
Seitenanfang -
Weiter mit Beeinflussung der Lichtabsorption durch Substituenten…