Autoprotolyse
Die geringe, aber nachweisbare elektrische Leitfähigkeit von dest. Wasser kann mit der Autoprotolyse der Wasser-Moleküle erklärt werden.
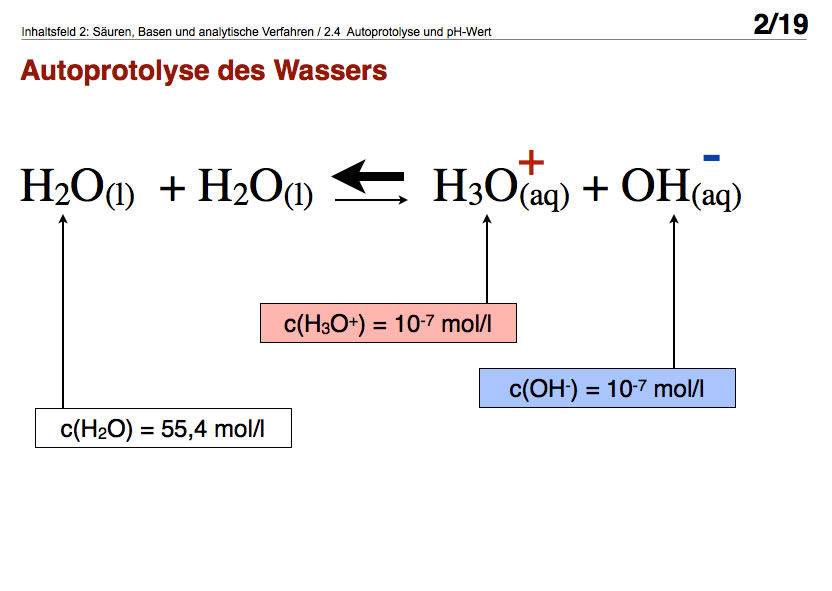
Hier sehen Sie das Bild 2 aus meiner Präsentation zum Thema "Autoprotolyse und pH-Wert". Gezeigt ist die Reaktionsgleichung der Autoprotolyse. Ein Wasser-Molekül gibt ein Proton an ein anderes Wasser-Molekül ab. Es bilden sich dabei ein Oxonium-Ion und ein Hydroxid-Ion. Das eine Wasser-Molekül fungiert also als Säure, das andere als Base.
Das Gleichgewicht dieser Autoprotolyse liegt weit auf der linken Seite, wie man an den Konzentrationen der Teilchen gut erkennen kann.
Diese wenigen Ionen sind dann für die geringe elektrische Leitfähigkeit von dest. Wasser verantwortlich.