Struktur
Thiazol gehört zu den fünfgliedrigen aromatischen Heterocyclen.

Thiazol ist ein Verwandter des Imidazols
Autor: Ulrich Helmich 05/2023, Lizenz: Public domain
Das Thiazol-Molekül ist mit dem Imidazol-Molekül verwandt, allerdings ist das H-Atom tragende N-Atom durch ein S-Atom ersetzt.
Aromatizität
Das pi-System des Thiazols besteht aus sechs Elektronen: drei werden von den drei C-Atomen geliefert, zwei von dem S-Atom und eins von dem N-Atom. Damit ist die (4n+2)-Regel von Hückel erfüllt. Der Ring ist außerdem planar.
Das freie Elektronenpaar des N-Atoms sowie das eine freie Elektronenpaar des S-Atoms gehören nicht zum aromatischen System.
Aber selbst, wenn sie es täten, wäre die (4n+2)-Regel erfüllt, denn dann hätten wir 10 pi-Elektronen (n=2).
Diese wichtige Regel wurde von Erich Hückel (1896-1980) um 1930 aufgestellt. Mit dieser Regel kann man beurteilen, ob eine cyclische Verbindung mit Doppelbindungen aromatisch ist oder nicht.
Biologische Bedeutung
Der Thiazol-Ring oder Derivate von ihm kommen in einigen biologisch wichtigen Verbindungen vor wie zum Beispiel Vitamin B1(Thiamin).
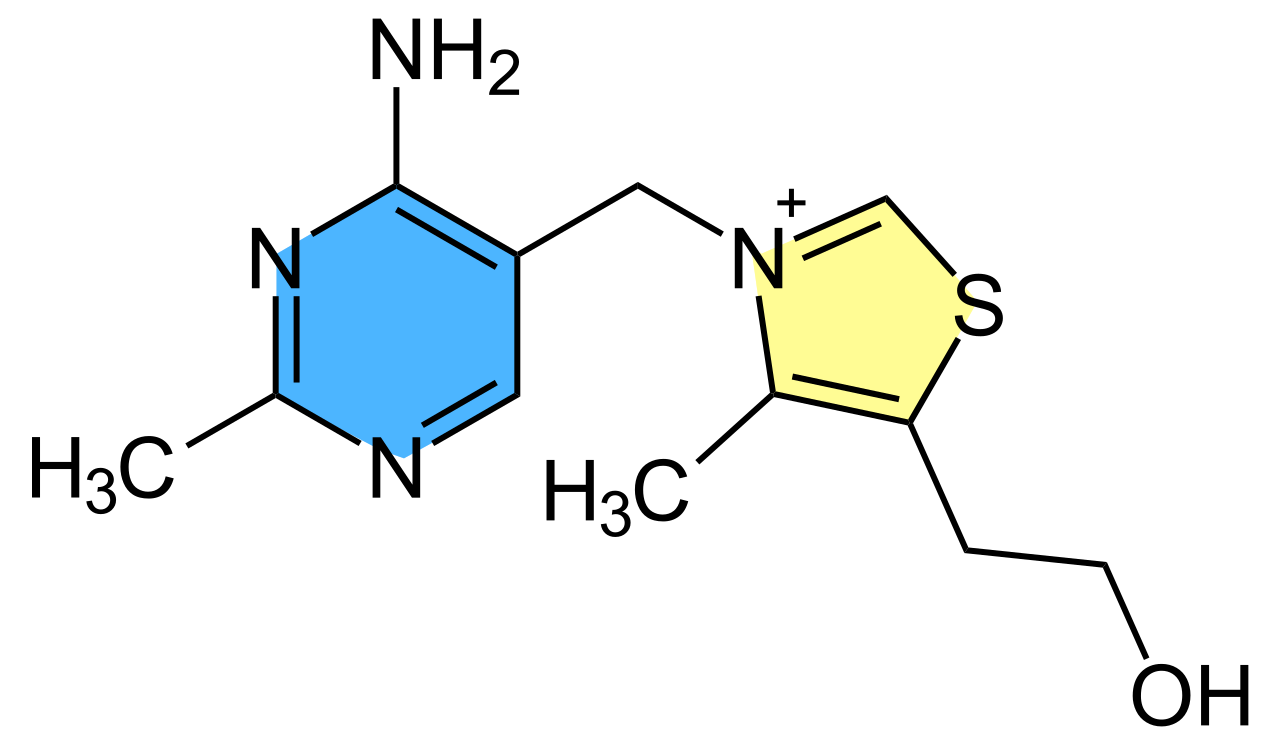
Strukturformel des Thiamin-Kations
NEUROtiker, Public domain, via Wikimedia Commons
Medizinische Bedeutung
Laut Römpp (1992) dienen einige Thiazol-Derivate als Zwischenprodukte für die Synthese von Sulfonamiden, andere werden als Chemotherapeutika eingesetzt. Auch Antibiotika wie Penicilline enthalten einen (reduzierten) Thiazol-Ring als Baustein:

Text
Yikrazuul, Public domain, via Wikimedia Commons. Einfärbung des Thiazol-Rings durch U. Helmich
Eigenschaften
Thiazol ist eine farblose bis blassgelbe Flüssigkeit von faulig-fischigem Geruch mit einer Dichte von 1,20 g/cm3 , einem Schmelzpunkt von -33 ºC und einem Siedepunkt von 117 bis 118 ºC. Die Wasserlöslichkeit ist mäßig.
Weitere Einzelheiten zum Thiazol finden sich in diesem Wikipedia-Artikel.