Offizielle Formulierung
Die Schülerinnen und Schüler
- stellen den Aufbau der Moleküle (Konstitutions-Isomerie, Stereoisomerie, Molekülgeometrie, Chiralität am asymmetrischen C-Atom) von Vertretern der Stoffklassen der Alkane, Halogenalkane, Alkene, Alkine Alkanole, Alkanale, Alkanone, Carbonsäuren, Ester und Amine auch mit digitalen Werkzeugen dar.
Aufbau und Darstellung organischer Moleküle
Organische Moleküle haben ein Grundgerüst aus miteinander verbundenen Kohlenstoff-Atomen, die im Falle der Kohlenwasserstoffe (Alkane, Alkene, Alkine etc.) nur von Wasserstoff-Atomen umgeben sind, im Falle anderer organischer Stoffgruppen aber zusätzliche funktionelle Gruppen tragen, von denen wohl die Hydroxygruppe (-OH), die Aldehydgruppe (-CHO), die Ketogruppe (-CO-), die Carboxygruppe (-COOH), die Aminogruppe (-NH2) sowie Halogenatome (-F, -Cl, -Br und -I) die wichtigsten für den Chemieunterricht der Oberstufe sind. Gelegentlich werden auch die C=C-Doppelbindung und die C-C-Dreifachbindung als funktionelle Gruppen bezeichnet. Diese funktionellen Gruppen verleihen den organischen Verbindungen ihre typischen physikalischen und chemischen Eigenschaften.
Auf dieser Seite im Organik-Kurs erfahren Sie, wie man organische Moleküle auf verschiedene Weisen zeichnerisch und mit Hilfe von Molekülbaukästen bzw. digitalen Werkzeugen darstellen kann.
Konstitutions-Isomerie am Beispiel der Alkane
Dazu betrachten wir einfach mal die Verbindung Butan mit der Summenformel C4H10.

Zwei Konstitutions-Isomere des Butans, in der unteren Reihe als Skelettformeln.
Autor: Ulrich Helmich 2022, Lizenz: Public domain
Das "normale" Butan, auch als n-Butan bezeichnet, besteht aus einer durchgehenden Kette von vier C-Atomen, während das Konstitutions-Isomer Methyl-propan nur eine Kette mit drei C-Atomen besitzt (daher der Name "Propan"). Allerdings hängt an dem mittleren C-Atom der Propankette eine Methylgruppe. Das Molekül besitzt also ebenfalls vier C-Atome und zehn H-Atome, genau wie das n-Butan.
Die Formulierung "Methyl-propan gehört zu den Butanen" ist also völlig korrekt, denn das Molekül hat vier C-Atome. Dagegen wäre die Formulierung "Methyl-propan ist ein Propan" falsch, denn Propan hat drei C-Atome und nicht vier.
Über das Phänomen der Isomerie erfahren Sie mehr auf dieser Seite im Chemie-Lexikon. Von dieser einführenden Seite führen dann Querverweise auf die konkreten Isomerie-Arten.
Wenn Sie mehr über die Konstitutions-Isomerie wissen wollen, gehen Sie auf diese Lexikonseite in dem Chemie-Lexikon.
Stereoisomerie am Beispiel der Alkane
Bei der Stereoisomerie gibt es zwei Formen, die für das Chemie-Abitur eine Rolle spielen könnten, die Enantiomerie und die Diastereoisomerie.
Enantiomerie
Betrachten wir zunächst die Enantiomerie am Beispiel von Butan-2-ol:
Zwei Konstitutions-Isomere des Butans
Autor: Ulrich Helmich 2022, Lizenz: Public domain
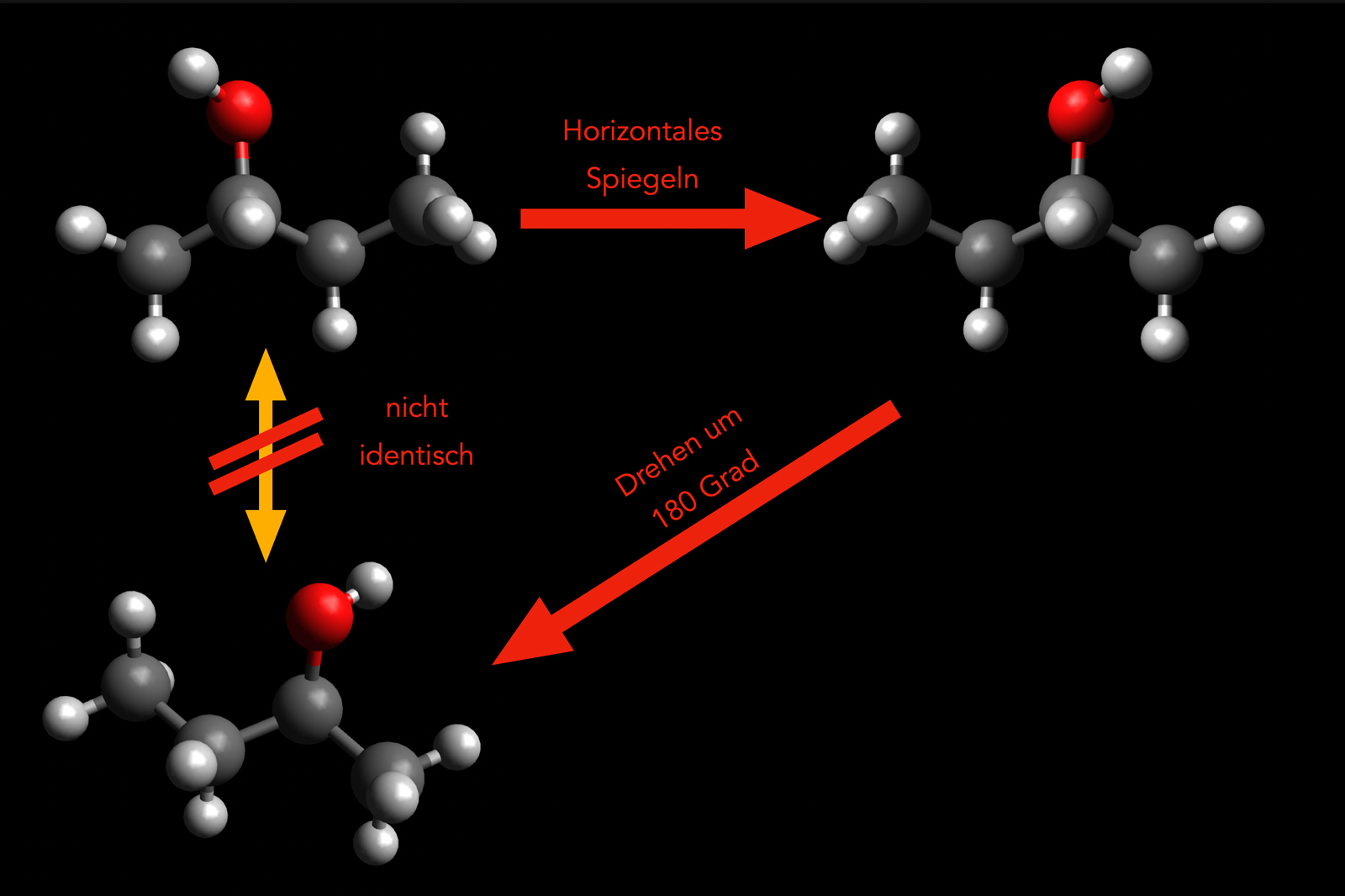
Das Bild zeigt oben links ein Butan-2-ol-Molekül. Durch horizontales Spiegeln mit Photoshop erhält man das exakte Spiegelbild des Moleküls. Die Frage ist jetzt, ob Bild und Spiegelbild identisch sind. Kann man das Spiegelbild durch einfaches Drehen zurück in das Bild verwandeln?
Mann kann nicht! Wenn Sie es versuchen, zum Beispiel durch Drehen des Spiegelbildes um 180 Grad (unten links), dann werden Sie feststellen, dass das gedrehte Spiegelbild und das Original nicht identisch sind. Es handelt sich um zwei verschiedene Moleküle, die aber nicht nur die gleiche Summenformel haben, sondern zudem auch noch die gleiche Konstitution: Kette aus vier C-Atomen mit einer OH-Gruppe am zweiten C-Atom.
Über Enantiomerie oder Spiegelbild-Isomerie können Sie mehr auf dieser Lexikonseite lesen.
Diastereomerie
Die Definition von Diastereomerie ist eigentlich ganz einfach:
Diastereomere sind unterscheidbare Moleküle mit der selben Konstitution (also Stereoisomere), die sich aber nicht wie Bild und Spiegelbild verhalten, also keine Enantiomere sind.
Oder formelmäßig:
Hier ein einfaches Beispiel:
2-Brom-3-Chlor-pentan
Autor: Ulrich Helmich 2022, Lizenz: Public domain
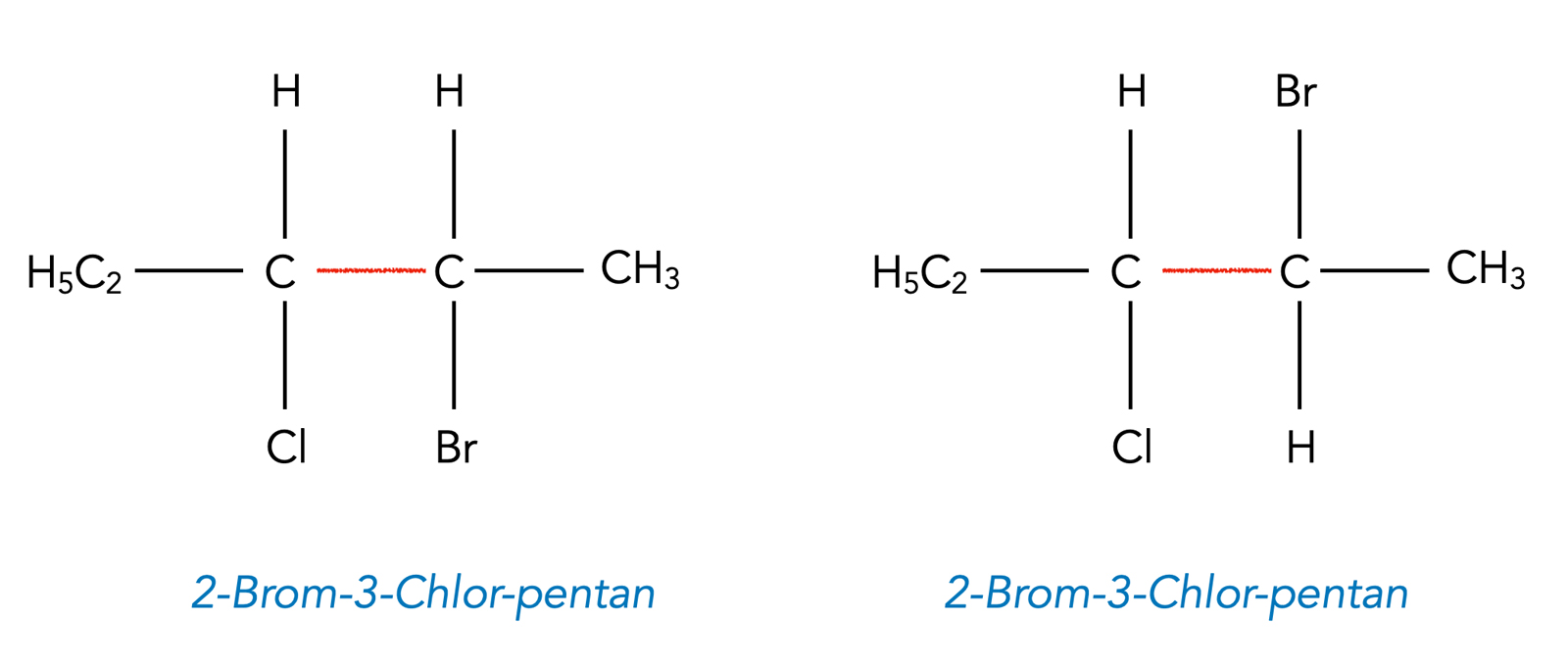
Sind diese beiden Moleküle identisch oder nicht? Auf den ersten Blick könnte man denken: Drehen wir doch einfach das C-Atom, an dem das Br-Atom hängt, um 180 Grad um die rot eingezeichnete C-C-Einfachbindung.
Ein guter Gedanke! Allerdings berücksichtigt dieser Gedanke nicht die Tatsache, dass die obigen Strukturformeln nicht die Raumstruktur der Moleküle wiedergeben, sondern nur die Konstitution in Form einer planaren Projektion. Wenn wir uns die beiden Moleküle dagegen mit einem Molekülbaukasten zusammenbauen, dann sehen wir, dass es sich tatsächlich um zwei verschiedene Moleküle handelt.

2-Brom-3-Chlor-pentan als Modelle
Autor: Ulrich Helmich 2022, Lizenz: Public domain
In der oberen Reihe sehen wir die Molekülmodelle A und B für die beiden Verbindungen aus der Abbildung 3.
Die untere Reihe zeigt, was passiert, wenn man beim Modell B das C-Atom mit dem Brom um 180 Grad dreht. Zwar zeigt jetzt das Brom-Atom nach unten, genau wie bei Modell A, aber achten Sie mal auf die Position des H-Atoms am gleichen C-Atom. Bei Modell A zeigt dieses H-Atom nach hinten, beim gedrehten Modell B (also bei B') jedoch nach vorne. Die beiden Moleküle sind also nicht identisch, obwohl sie die gleiche Konstitution haben. Es handelt sich um Stereoisomere, die sich nicht spiegelbildlich zueinander verhalten. Also sind es zwei Diastereomere.
cis-trans-Isomerie
Eine spezielle Form der Diastereomerie ist die cis-trans-Isomerie, die bei Alkenen oder cyclischen Verbindungen auftritt.
cis-trans-Isomerie
Autor: Ulrich Helmich 2022, Lizenz: Public domain
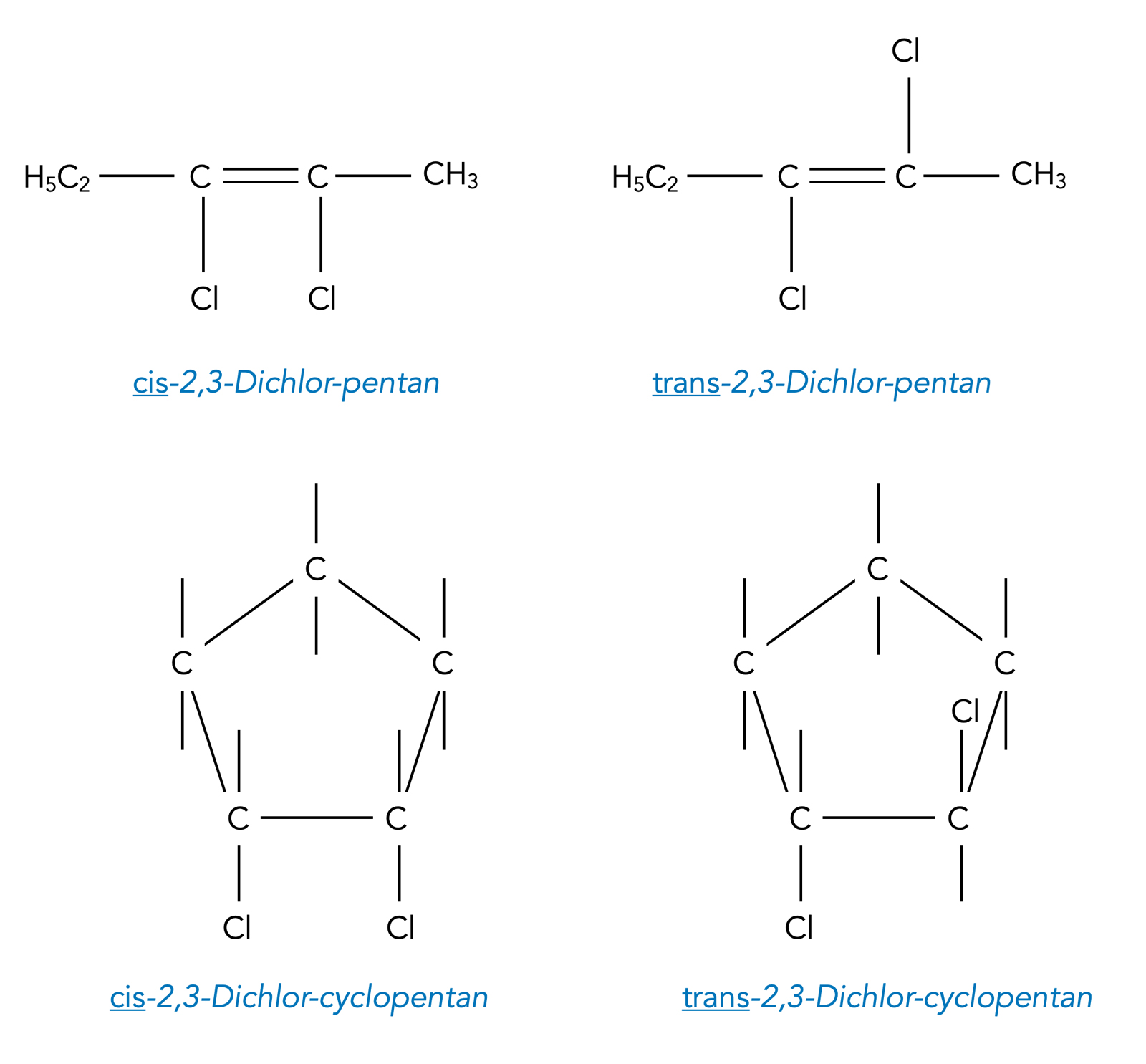
Hier sehen wir zwei Beispiele für cis-trans-Isomerie, oben bei einem Halogen-Alken, unten bei einem cyclischen Halogen-Alkan. Die H-Atome sind in dem unteren Beispiel nicht mit eingezeichnet worden, um die Zeichnung übersichtlich zu halten.
Wenn Sie mehr über Diastereomerie wissen möchten, sind Sie auf diese Lexikon-Seite richtig.
Hier erfahren Sie mehr über die spezielle Form der Diastereomerie, die cis-trans-Isomerie.