Lernziele
Wenn Sie diese Seite durchgearbeitet haben, sollten Sie wissen
- was der Unterschied zwischen syn-Addition und anti-Addition ist
- wie sterische Effekte den Angriff von Wasserstoff auf die C=C-Doppelbindung beeinflussen
Ein Beispiel für eine syn-Addition
Bei einer elektrophilen Addition an eine C=C-Doppelbindung kann eine Verbindung X-Y auf zwei verschiedene Weisen addiert werden:
- X und Y greifen auf der gleichen Seite der Doppelbindung an: syn-Addition.
- X und Y greifen auf unterschiedlichen Seiten der Doppelbindung an: anti-Addition.
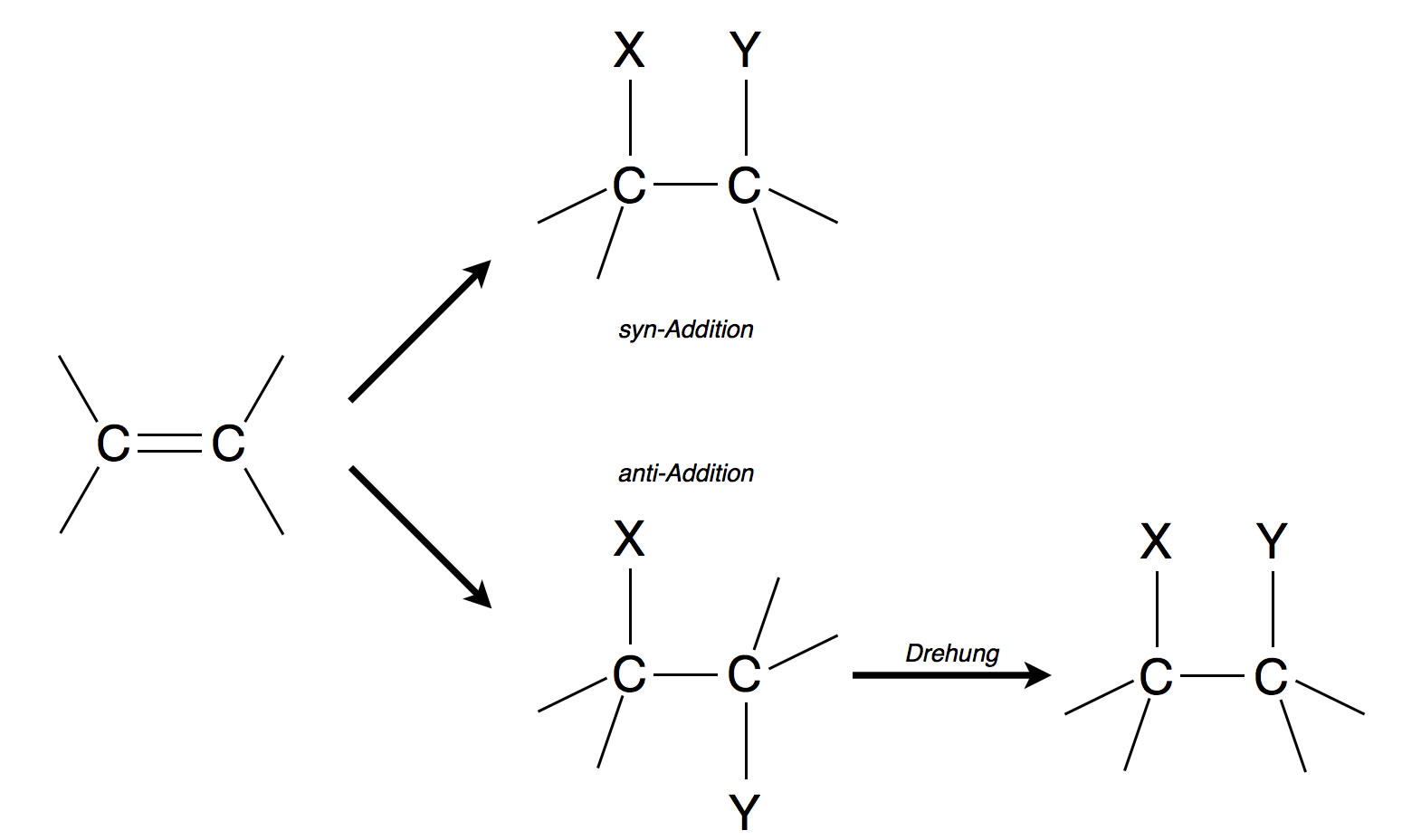
syn- und anti-Addition im Schema
Bei kettenförmigen Kohlenwasserstoffen spielt dieser Unterschied normalerweise keine Rolle, das Endprodukt besitzt statt der C=C-Doppelbindung jetzt eine C-C-Einfachbindung mit freier Drehbarkeit. Das Produkt der syn-Addition ist dann das gleiche wie das Produkt einer anti-Addition.
Ist die freie Drehbarkeit jedoch sterisch gehemmt, wie es beispielsweise in zyklischen Verbindungen der Fall ist, so können tatsächlich zwei verschiedene Produkte entstehen, ein cis-Produkt bei der syn-Addition und ein trans-Produkt bei der anti-Addition.
Wichtig ist die syn-Addition bei der elektrophilen Addition von Wasserstoff an eine C=C-Doppelbindung. Wegen der hohen Bindungsdissoziationsenergie der H-H-Bindung gelingt diese Hydrierung nur mit Hilfe von Katalysatoren. Das H2-Molekül bindet an der Oberfläche des Katalysators, wodurch die H-H-Bindung geschwächt wird. Dann verbindet sich erst das eine H-Atom mit einem C-Atom der C=C-Doppelbindung, dann das andere H-Atom. Einzelheiten dazu siehe Wikipedia-Artikel "Hydrierung". Ergebnis dieser katalysierten Hydrierung ist immer eine syn-Addition des Wasserstoffs.
In der Video-Vorlesung "Organische Chemie 1" von Prof. Dyker von der Ruhr-Universität Bochum wird in der Folge 1.31 bei Zeitindex 37:00 ein interessantes Beispiel vorgestellt, nämlich die Addition von Wasserstoff an die zyklische Verbindung Caren.
Caren ist ein bicyclisches Monoterpen. Es besteht aus einem Cyclohexen-Ring, an den ein Cyclopropan-Ring angekoppelt ist, daher "bicyclisch". Die genaue Strukturformel ist aus der folgenden Abbildung ersichtlich, die ich in Anlehnung an das Tafelbild von Prof. Dyker selbst erstellt habe:
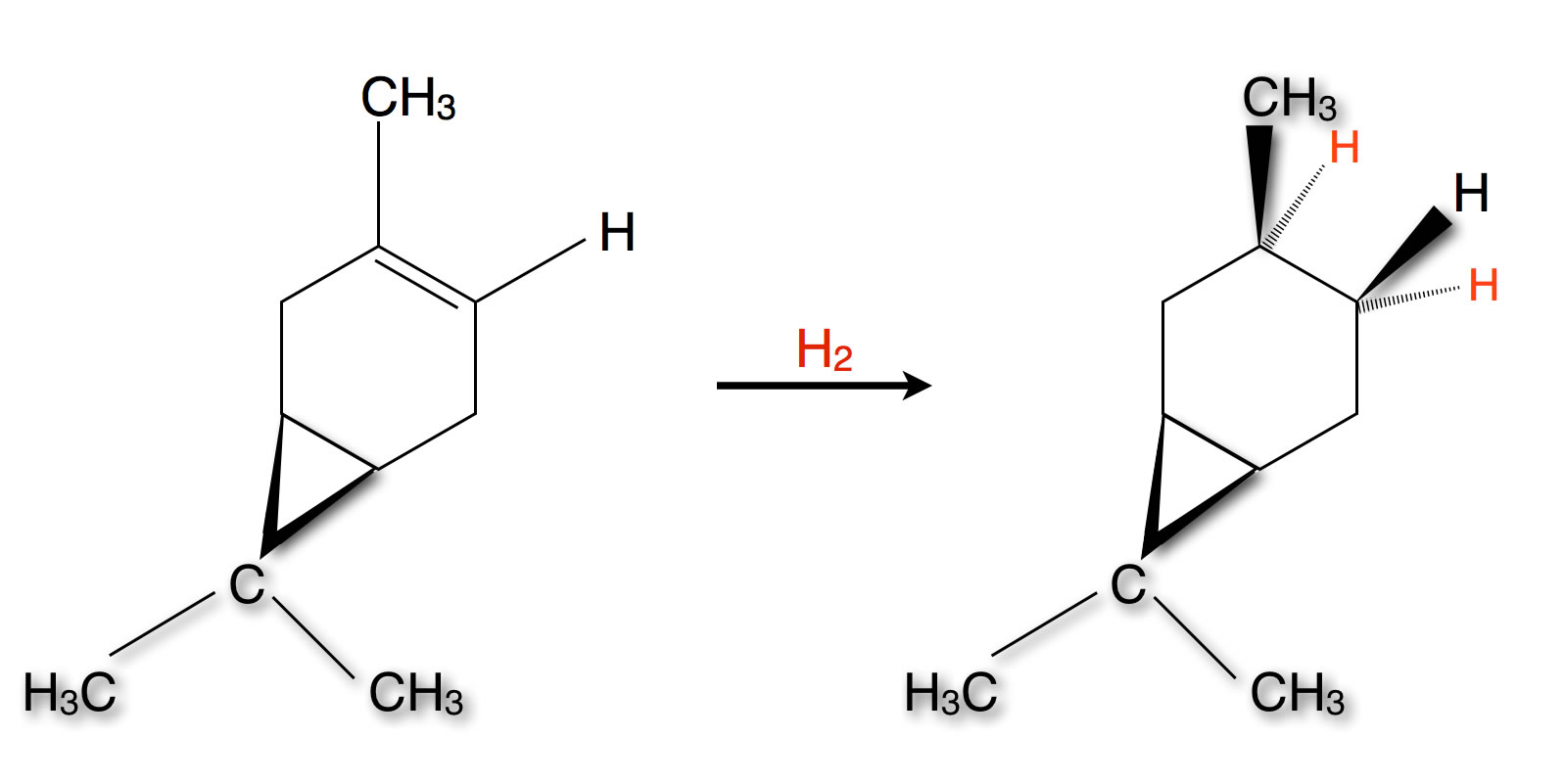
Die syn-Addition von Wasserstoff an die Doppelbindung von Caren
Der Cyclopropan-Ring des Carens (links) ragt nach vorne aus der Zeichenebene heraus. Das Wasserstoff-Molekül greift die Doppelbindung "von hinten" an. Ein Angriff von vorne wird durch den nach vorne herausragenden Cyclopropan-Ring sterisch behindert.
Und jetzt wird es interessant: An sich wäre es energetisch günstiger, wenn das alternative Reaktionsprodukt entstünde, durch einen syn-Angriff von der "Vorderseite". Dann würde nämlich die CH3-Gruppe oben in der Abbildung nach "hinten" zeigen, abgewandt von dem Cyclopropan-Ring.
Wegen der sterischen Hinderung greift der Wasserstoff jedoch von der "Unterseite" an, so dass das energetisch ungünstigere Produkt entsteht.
In diesem Beispiel sehen wir wieder einmal den Einfluss der kinetischen Kontrolle gegenüber der thermodynamischen Kontrolle:
- Thermodynamische Kontrolle: Es wird der Reaktionsweg eingeschlagen, bei dem die meiste Reaktionsenthalpie freigesetzt wird.
- Kinetische Kontrolle: Es wird der Reaktionsweg eingeschlagen, bei dem die Aktivierungsenergie am geringsten ist.
In unserem Beispiel hat die kinetische Kontrolle einen größeren Einfluss als die thermodynamische Kontrolle.
Ein Beispiel für anti-Addition
Ein Beispiel für eine anti-Addition haben wir mit der Bromierung von Hexen bzw. Ethen bereits kennengelernt. Das positiv geladene Brom-Kation bildet ein Bromonium-Ion mit delokalisierter positiver Ladung. Ein Bromid-Anion wird nun angezogen, kann aber nur von der Rückseite her angreifen, wegen der sterischen Behinderung durch das Bromonium-Ion. Das Ergebnis dieses Rückseitenangriffs ist dann eine anti-Addition.