Das Grove-Element ist ein historisches galvanisches Element, das man heute aus Zink-Platin-Zelle bezeichnen würde.
Aufbau
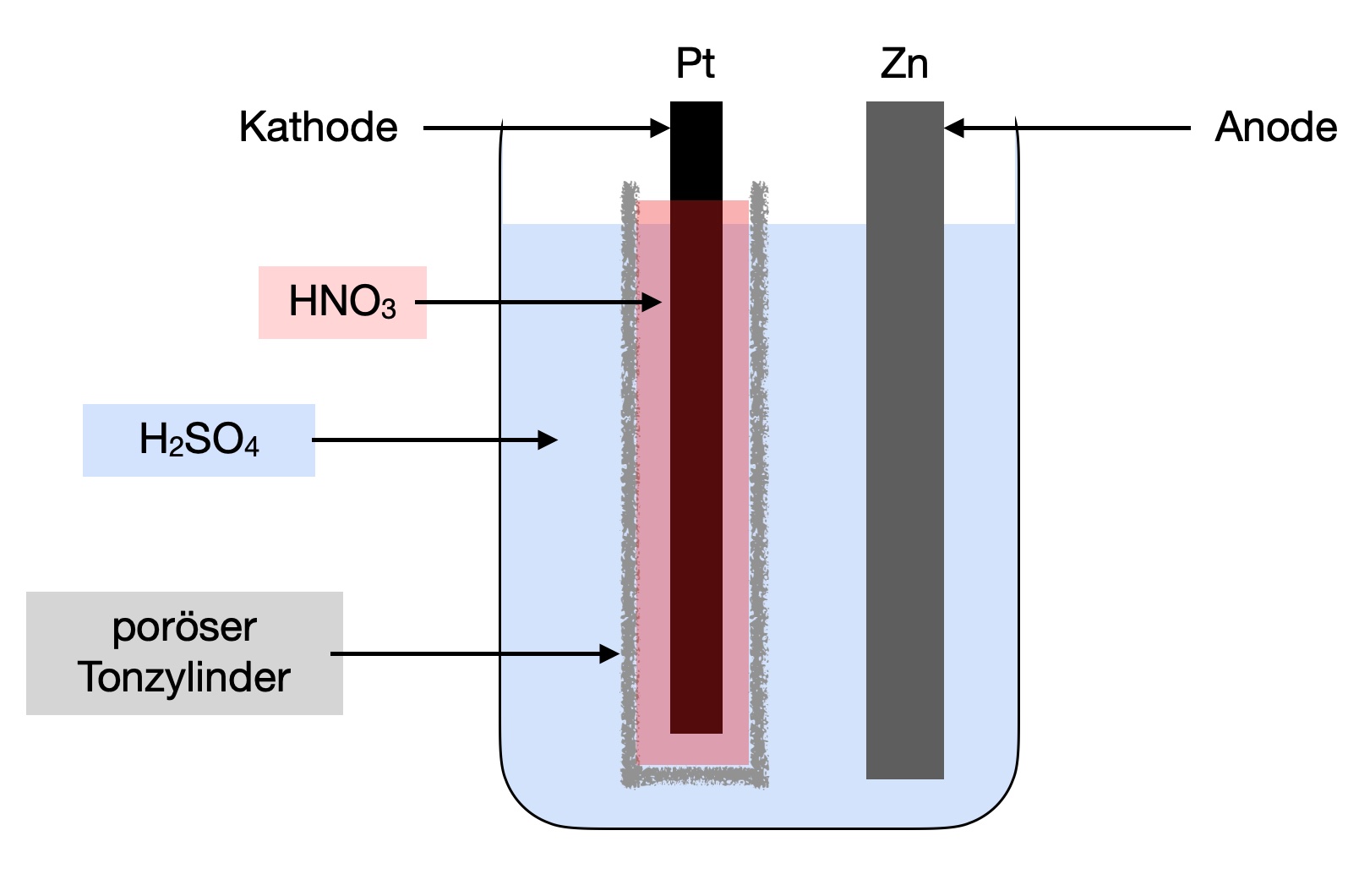
Aufbau des Grove-Elements
Autor: Ulrich Helmich 05/2024, Lizenz: Public domain
In einem porösen Tonzylinder befindet sich eine Platin-Elektrode in verdünnter Salpetersäure HNO3.
Dieser Tonzylinder steht dann in einem Becherglas, das mit verdünnter Schwefelsäure H2SO4 gefüllt ist, außerdem befindet sich eine Zink-Elektrode in dem Becherglas mit der Schwefelsäure.
Reaktionen
Zink-Halbzelle
$Zn \to Zn^{2+} + 2 \ e^{-}$
Zink-Atome werden zu Zn2+-Ionen oxidiert.
Falls der Browser die Formeln auf dieser Seite nicht richtig darstellt, wurde die Erweiterung MathJax nicht korrekt geladen. Entweder ist der Browser veraltet, oder es besteht im Augenblick keine Internetverbindung.
Platin-Halbzelle
$NO_3^{-} + 2 \ H_3O^{+} + e^{-}\to NO_2 + 3 \ H_2O$
Nitrat-Ionen und Oxonium-Ionen, die Bestandteil des Elektrolyten HNO3 sind, werden an der Platin-Elektrode zu Stickstoffdioxid NO2 und Wasser H2O reduziert.
Gesamtreaktion
$Zn + 2 \ NO_3^{-} + 4 \ H_3O^{+} \to Zn^{2+} + 2 \ NO_2 + 6 \ H_2O$
Spannung
Unter Standardbedingungen
Das Standardredoxpotenzial für das System NO2, H2O / NO3-, H3O+ beträgt +0,80 Volt.
Das Standardredoxpotenzial für das System Zn / Zn2+ beträgt -0,76 Volt.
Daraus ergibt sich eine theoretische Spannung von 1,56 Volt unter Standardbedingungen.
Tatsächliche Spannung
Die tatsächlich verwendeten Grove-Elemente lieferten sogar Spannungen bis 1,9 V, was deutlich mehr ist als die Spannung von 1,1 V, die das Daniell-Element lieferte.
Wegen dieser hohen Spannung wurde das Grove-Element in Nordamerika bei den ersten Telegrafieverbindungen als Stromquelle eingesetzt. Gegen den kommerziellen Einsatz sprechen allerdings zwei Gründe: Erstens der hohe Preis für die Platin-Elektroden, und zweitens die schädlichen Stickoxide, die beim Betrieb freigesetzt werden.
Modernere Versionen
In der Abituraufgabe "Das Grove-Element" aus dem Jahre 2021 (NRW) wird eine modernere Version dieses historischen Elements vorgestellt. Das moderne Grove-Element weicht in drei wichtigen Punkten von klassischen Vorbild ab:
- Die Zink-Elektrode befindet sich wie beim klassischen Vorbild in verdünnter Schwefelsäure, die Platin-Elektrode wird aber durch eine einfache Kohle-Elektrode ersetzt.
- Die Kohle-Elektrode befindet sich nicht in Salpetersäure, sondern in einer schwefelsauren Lösung von Kaliumperoxodisulfat K2S2O8.
- Der poröse Tonzylinder, der für Kationen und Anionen jeglicher Art durchlässig ist, wird durch eine Membran ersetzt, die ausschließlich Kationen durchlässt.
Diese moderne Version hat gegenüber der historischen Version mehrere Vorteile:
- Es ist wesentlich billiger, da die teure Platin-Elektrode durch eine preiswerte Kohle-Elektrode ersetzt wird.
- Der Elektrolyt (schwefelsaure Lösung von Kaliumperoxodisulfat K2S2O8) hat ein geringeres Gefahrenpotenzial für die Umwelt als die ursprünglich verwendete Salpetersäure, weil hier die Bildung von giftigem Stickstoffdioxid vermieden wird.
- Die kationensensitive Membran verringert die Störanfälligkeit
- Das moderne Grove-Element liefert eine höhere Spannung.