Schritt 1: Nucleophiler Angriff des Alkohols
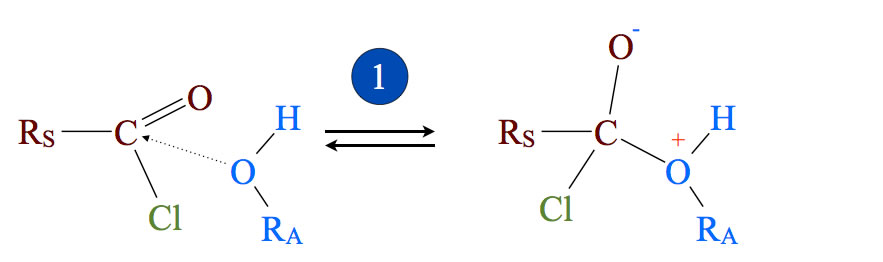
Säurechlorid sind wesentlich reaktiver als Carbonsäuren. Das C-Atom der COOH-Gruppe ist durch das stark elektronegative Chlor-Atom recht stark positiv polarisiert. Daher stellt es ein ideales Angriffsziel für ein Nucleophil dar.
Schritt 2: Umlagerung eines Protons
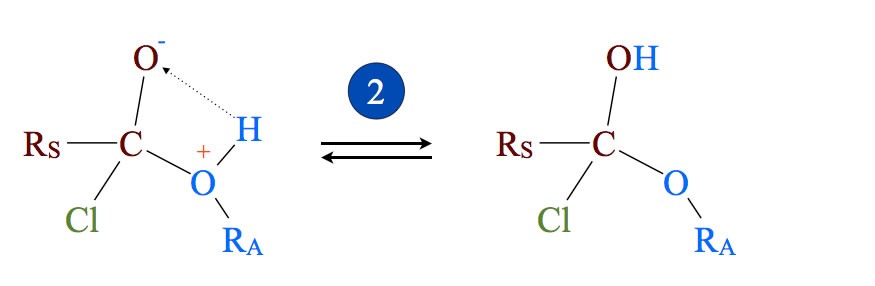
Dieser Schritt verläuft ähnlich wie bei der säurekatalysierten Veresterung einer Carbonsäure. Das Proton "wandert" vom Alkohol-O-Atom zur Hydroxygruppe der Carbonsäure. Allerdings bildet sich eine stabile OH-Gruppe. Bei der säurekatalysierten Veresterung bildete sich in Schritt 3 ja ein Oxonium-Ion, dass im nächsten Schritt dann leicht als Wasser-Molekül abgespalten werden konnte.
Schritt 3: Abspaltung von Chlorid
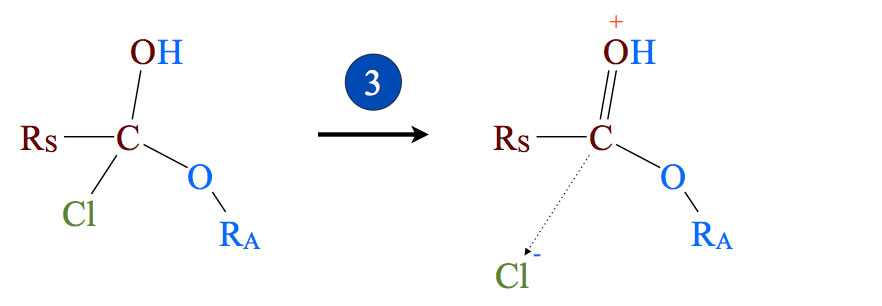
Das Chlor-Atom wird nun als Chlorid-Ion abgespalten; es bleibt ein positiv geladenes organisches Ion zurück. Die positive Ladung "wandert" vom C-Atom zur OH-Gruppe, was nicht gerade sehr stabil aussieht.
Schritt 4: Abspaltung eines Protons
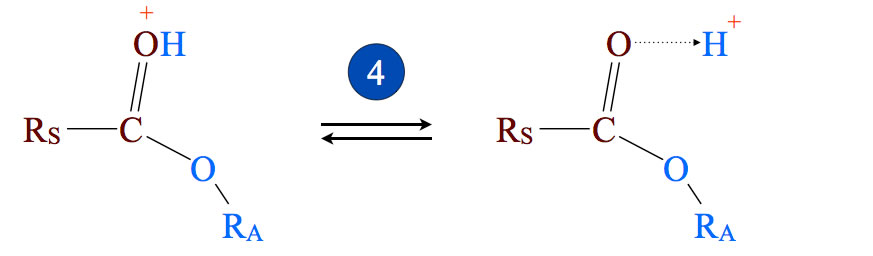
Im letzten Schritt der Veresterung wird ein Proton abgespalten und das Endprodukt Ester liegt vor.