Reduktion zu Alkoholen Q1
Im Chemieunterricht lernt man normalerweise, dass man Alkohole zu Aldehyden und Ketonen oxidieren kann, und dass sich die Aldehyde weiter zu Carbonsäuren oxidieren lassen. Viele komplexere Carbonsäuren werden auch tatsächlich auf diese Weise synthetisiert.
Es gibt aber auch Fälle, in denen die Carbonsäure leichter gewonnen werden kann als der entsprechende Alkohol, das ist zum Beispiel bei den langkettigen Fettsäuren der Fall, die man leicht aus Fetten oder Ölen gewinnen kann, oder bei den Fruchtsäuren, die man aus Früchten wie Äpfeln oder Weintrauben herstellen kann.
Das beliebteste Reduktionsmittel, mit dem man aus einer Carbonsäure einen primären Alkohol herstellen kann, ist das Lithiumaluminiumhydrid LiAlH4[1,4]. Der genaue Verlauf der Reduktion ist hier jetzt nicht relevant, auf jeden Fall entsteht dann unter recht milden Bedingungen der passende primäre Alkohol in hoher Ausbeute aus der Carbonsäure. Allerdings ist das Lithiumaluminiumhydrid recht teuer, daher wird es nur bei der Synthese von Arzneimitteln oder Hormonen eingesetzt[1].
Billiger ist die zweistufige Reduktion: Zunächst wird die Carbonsäure verestert, und dann wird der Ester zu zwei Alkoholen reduziert.
Halogenierung am alpha-C-Atom Q1
Kommen wir nun zu einer ganz anderen Reaktion, bei der die Carboxygruppe zwar eine Rolle spielt, aber nicht an der Reaktion teilnimmt. Das der Carboxygruppe direkt benachbarte C-Atom der Carbonsäure wird als alpha-C-Atom bezeichnet. Die H-Atome, die an diesem C-Atom sitzen, heißen dann entsprechende alpha-H-Atome.
Diese α-H-Atome können nun recht leicht durch Halogen-Atome ersetzt werden, vor allem durch Brom oder Chlor. Kleine Mengen an Phosphor dienen dabei als Katalysator. Auf diese Reaktion soll aber an dieser Stelle nicht weiter eingegangen werden. Es sei nur gesagt, dass sie sehr spezifisch und sehr schnell verläuft und damit eine große Bedeutung für die organische industrielle Synthese hat[4].
Decarboxylierung Q1
Manche Carbonsäuren geben ihre Carboxygruppe recht leicht in Form von Kohlendioxid ab, man spricht dann von einer Decarboxylierung. Das Ergebnis einer solchen Decarboxylierung ist dann ein einfaches Alkan. Jedenfalls dann, wenn eine Monocarbonsäure decarboxyliert wurde.
Ganz einfach ist diese Decarboxylierung bei Monocarbonsäuren wie Essigsäure oder Buttersäure allerdings nicht. Viel besser eigenen sich beta-Ketosäuren und 1,3-Dicarbonsäuren zur Decarboxylierung[4].
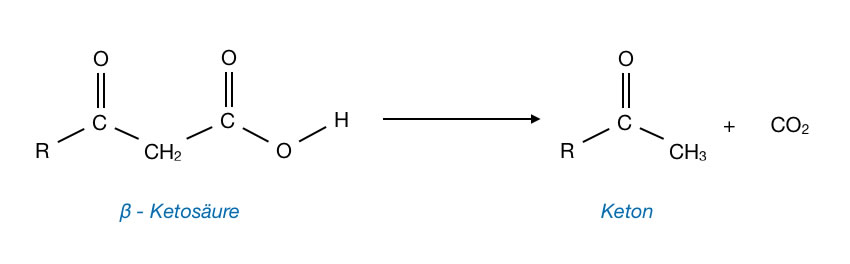
Decarboxylierung einer beta-Ketosäure zu einem Keton
Eine beta-Ketosäure ist eine Carbonsäure mit einer Keto-Gruppe am beta-C-Atom, und eine 1,3-Dicarbonsäure ist eine Carbonsäure mit zwei COOH-Gruppen, die durch eine CH2-Gruppe getrennt sind.
Eine bekannte 1,3-Dicarbonsäure ist die Malonsäure. Malonsäure lässt sich in wässriger Lösung bereits bei 70 ºC decarboxylieren[5].
In der Biochemie spielen Decarboxylierungen eine sehr wichtige Rolle. Denken Sie mal an den Citratzyklus, den Sie vielleicht aus dem Biologie-Unterricht kennen. Am Ende der Glycolyse wird der gewonnene C3-Körper Pyruvat decarboxyliert, der so gebildete C2-Körper wird an den C4-Körper Oxalacetat gebunden, wobei der C6-Körper Citrat entsteht. Dieser C6-Körper wird dann zweimal decarboxyliert, so dass sich schließlich wieder ein C4-Körper bildet, der erneut einen C2-Körper aus der Glycolyse anlagern kann. Das dabei freigesetzte CO2 atmen wir dann über die Lunge aus.
Weiterführende Seiten
Wenn Sie vorhaben, nach Ihrem Abitur Chemie, Biologie oder Medizin zu studieren, dann sollten Sie sich vielleicht ein paar der folgenden Seiten anschauen, die ich extra für Studieninteressierte und auch für Leute, die bereits eines dieser Fächer studieren, geschrieben habe.
Hier erfahren Sie weitere Einzelheiten zu diesem Thema.
Auf dieser Seite wird das Thema allgemein dargestellt, auf die Reaktionen im Citratzyklus wird nicht eingegangen.
Denn zu diesem Thema gibt es hier eine eigene Seite!
Quellen:
- Morrison, Boyd, Organic Chemistry, 7th Edition 2011
- Römpp Chemie-Lexikon, 9. Auflage 1992
- Wikipedia, Artikel zu den einzelnen Säuren
- Chemgapedia, Artikel "Reaktion von Carbonsäuren" (nicht mehr zugänglich!)
- Wikipedia, Artikel "Malonsäure"