Neubildung von Glucose
Unter der Gluconeogenese versteht man die Synthese von Glucose aus Verbindungen, die nicht zu den Kohlenhydraten gehören [2]. Die Hydrolyse von Stärke oder Glycogen zu Glucose ist also keine Gluconeogenese, sondern einfach eine Hydrolyse von Polysacchariden. Eine Neubildung von Glucose aus Nicht-Kohlenhydraten findet im menschlichen Körper immer dann statt, wenn nicht genügend Glucose aus der Nahrung oder den gespeicherten Glycogen-Reserven zur Verfügung steht. Bei einer kohlenhydratarmen Ernährung oder sogar -freien Ernährung kann das der Fall sein[4]. Wichtige Schlüsselenzyme der Gluconeogenese finden sich beim Menschen nur in der Lebe und der Niere.
Das Gehirn des Menschen benötigt täglich ca. 120 g Glucose [2], das ist ganz schön viel. Normalerweise reichen die Glucosereserven des Körpers aus, um diesen Bedarf zu decken. Wenn der Körper aber keine Nahrung bekommt oder nur sehr wenige Kohlenhydrate aufnimmt, wird Glucose aus der niedermolekularen Verbindung Pyruvat hergestellt. Pyruvat haben wir als Endprodukt der Glycolyse kennengelernt.
"Bereits nach einer nächtlichen Hungerphase steigt die Gluconeogenese beträchtlich an" [5].
Pyruvat kann aber auch aus Lactat, Aminosäuren und Glycerin hergestellt werden [2]. Das heißt mit anderen Worten, der Körper kann aus den mit der Nahrung aufgenommenen Proteinen (→ Aminosäuren) und Fetten (→ Fettsäuren + Glycerin) über das Pyruvat den wichtigen Nährstoff Glucose herstellen.
Glucose aus Pyruvat
Man könnte nun denken, die Glucose-Synthese aus Pyruvat ist einfach eine Umkehrung der Glycolyse. Das ist chemisch allerdings nicht möglich, denn drei der Reaktionen der Glycolyse sind irreversibel, also nicht umkehrbar. Die Glucose-Neubildung aus Pyruvat ist ein eigener Stoffwechselweg, bei dem an Anfang das Biotin eine wesentliche Rolle spielt. Wir haben ja bereits einige wichtige Coenzyme kennengelernt:
- ATP ist für den Transport von Phosphatgruppen verantwortlich.
- NADH und FADH2 sind für den Transport von Wasserstoff zuständig.
- Acetyl-CoA ist für den Transport von Acetyl-Gruppen verantwortlich.
Nun lernen wir ein neues Coenzym kennen, das Biotin, das auch als Vitamin B7 bekannt ist.
- Biotin ist für den Transport von CO2 bzw. Carboxygruppen zuständig.
Schritt 1: Pyruvat → PEP
Schritt 1.1: Pyruvat → Oxalacetat
Im ersten Schritt der Gluconeogenese wird in der Mitochondrien-Matrix das Pyruvat zu Phosphoenolpyruvat (PEP) umgebaut. Formal ist dies eine Umkehrung des letzten Schrittes der Glycolyse, verläuft chemisch allerdings völlig anders.
Zunächst wird das Pyruvat von der Pyruvat-Carboxylase zu Oxalacetat carboxyliert. Das Coenzym Biotin-CO2 liefert die erforderliche Carboxygruppe für diesen Schritt.
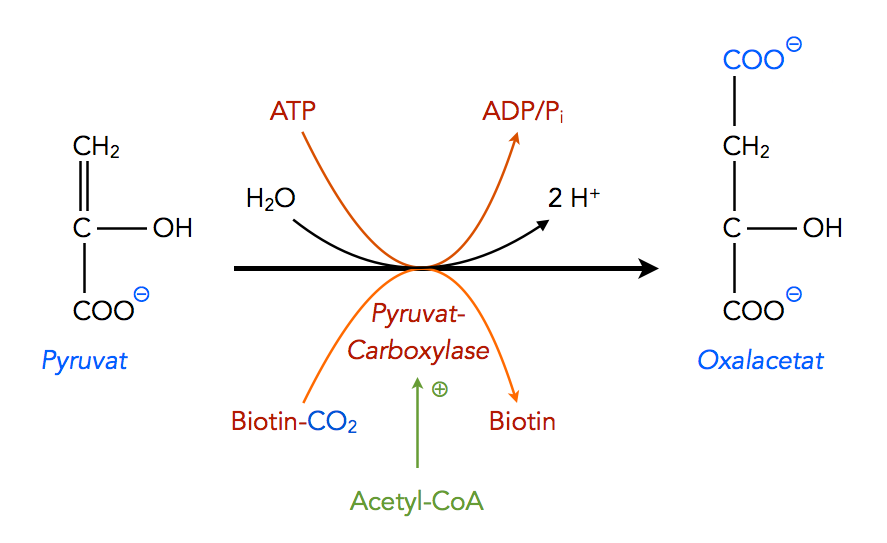
Die Carboxylierung von Pyruvat
Autor: Ulrich Helmich 2022, Lizenz: Public domain
In Wirklichkeit ist diese Reaktion etwas komplexer als in der Abbildung dargestellt, sie läuft in mehreren Schritten ab. Die Pyruvat-Decarboxylase ist auch für die Bildung des Carboxy-Biotins (Biotin-CO2) zuständig. Das geht allerdings nur in Anwesenheit von Acetyl-CoA, das allerdings nicht als Kohlendioxid-Spender fungiert, sondern als allosterischer Aktivator des Enzyms[2]. Das Kohlendioxid wird tatsächlich formal als CO2 an das Biotin gebunden, allerdings liegt CO2 in wässriger Lösung als Hydrogencarbonat-Ion HCO3- vor.
Schritt 1.2: Oxalacetat → Malat
Im zweiten Teil des ersten Schrittes wird das Oxalacetat in den Mitochondrien zu Malat reduziert:
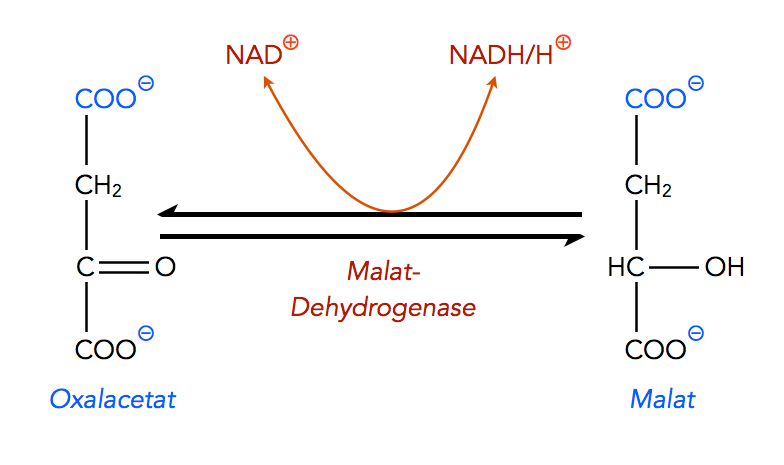
Umwandlung von Oxalacetat zu Malat
Autor: Ulrich Helmich 2022, Lizenz: Public domain
Diese Reaktion ist reversibel. Das zuständige Enzyme ist die Malat-Dehydrogenase, die wir bereits aus dem Citratzyklus kennen, der ja ebenfalls in der Matrix des Mitochondriums abläuft. Im Citratzyklus, Schritt 9, katalysiert die Malat-Dehydrogenase exakt die gleiche Reaktion.
Schritt 1.3 Malat → Oxalacetat
Aus irgendeinem Grund kann Oxalacetat nicht die Membranen des Mitochondriums passieren. Daher wird das Oxalacetat in der Mitochondrien-Matrix zunächst in Malat umgewandelt. Das Malat kann dann die Membranen passieren und gelangt ins Cytoplasma, dort wo auch die Glycolyse abläuft. Im Cytoplasma angekommen, wird das Malat wieder in Oxalacetat umgewandelt. Die Reaktion läuft genau so ab wie in der Abbildung 2, die man jetzt aber von rechts nach links lesen muss. Es wird also NADH/H+ verbraucht und NAD+ erzeugt.
Schritt 1.4 Oxalacetat → Phosphoenolpyruvat (PEP)
Jetzt endlich kann das erste "Zielprodukt" Phosphoenolpyruvat hergestellt werden. Das zuständige Enzym ist die Phosphoenolpyruvat-Carboxykinase. Das Enzym hat diesen komplizierten Namen, weil es zwei Dinge gleichzeitig macht:
- Decarboxylierung
- Phosphorylierung
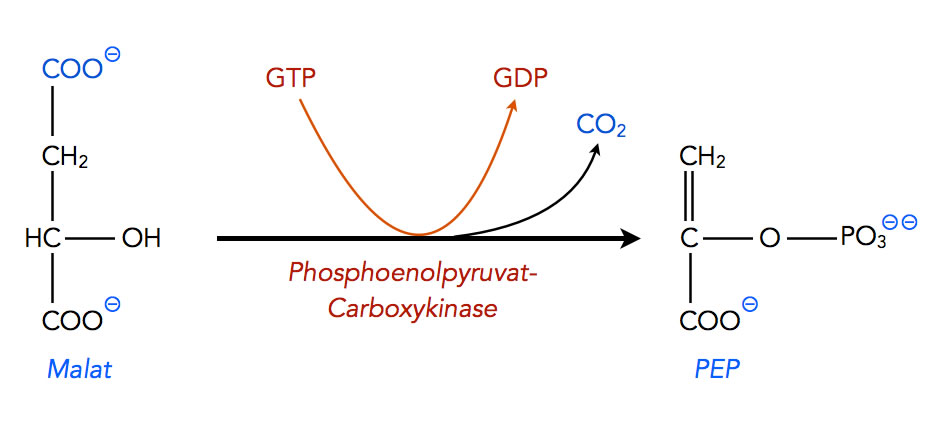
Beschreibung
Autor: Ulrich Helmich 2021, Lizenz: Public domain
GTP ist hier der Spender der Phosphatgruppe.
Damit wäre der erste Schritt der Gluconeogenese beendet. Hier noch einmal eine kurze Zusammenfassung:
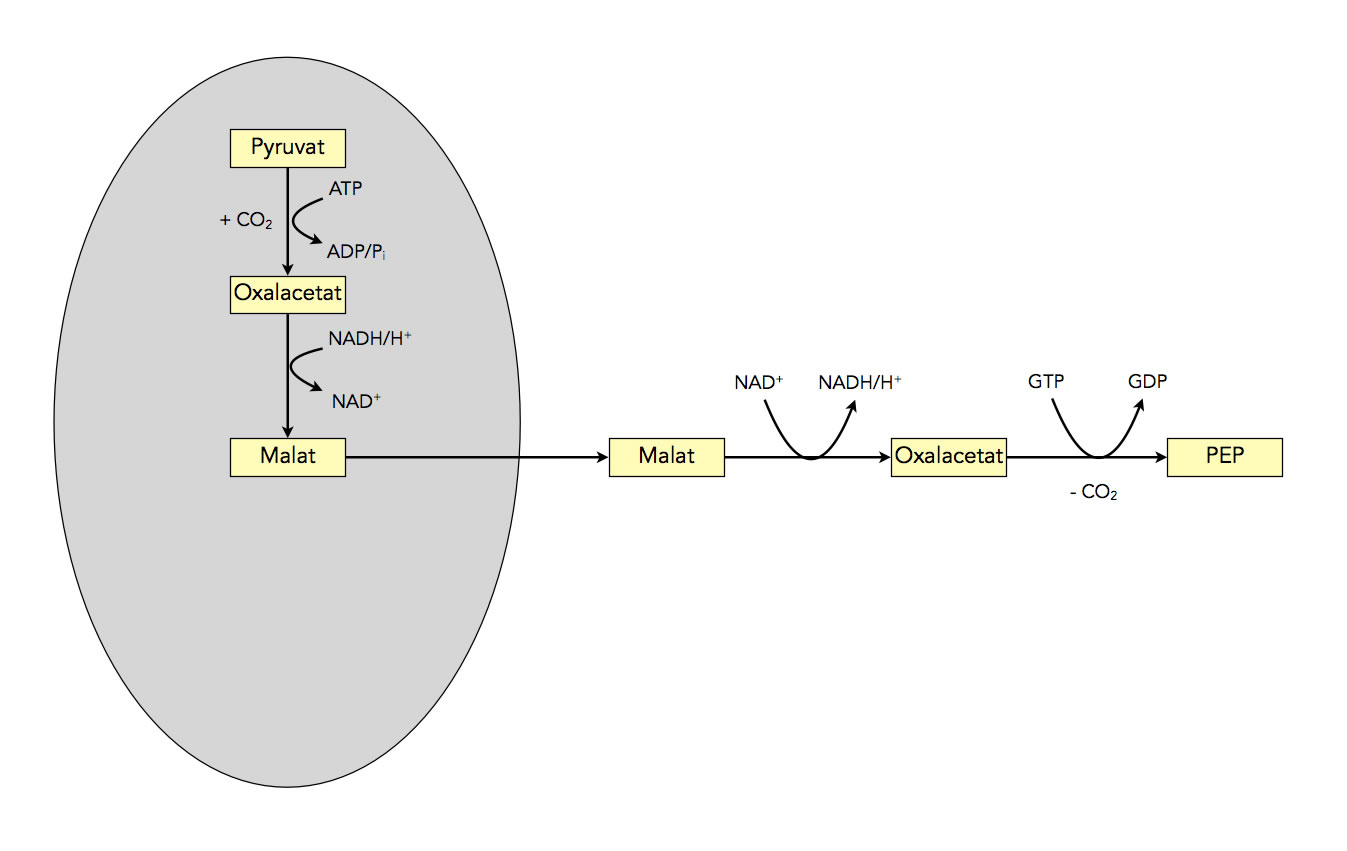
Zusammenfassung des ersten Schrittes der Gluconeogenese
Autor: Ulrich Helmich 2022, Lizenz: Public domain
Folgeschritte 2 bis 7
Jetzt können wir uns die Sache sehr einfach machen. Das Phosphoenolpyruvat durchläuft eine umgekehrte Glycolyse, bis zum Fructose-1,6-bisphosphat. Die Enzyme der Glycolyse, die an diesen Schritten beteiligt sind, katalysieren sowohl die Hin- wie auch die Rück-Reaktion (Hin-Reaktion = Glycolyse, Rück-Reaktion = Gluconeogenese):

Die Folgeschritte der Gluconeogenese bis zum Fructose-1,2-bisphosphat
Autor: Ulrich Helmich 2022, Lizenz: Public domain
Schritt 8
Bei der Glycolyse entsteht das Fructose-1,6-bisphosphat durch Phosphorylierung von Fructose-6-phosphat, das hierfür verantwortliche Enzym ist die Phosphofructokinase. Bei der Gluconeogenese wird der umgekehrte Weg beschritten:
Fructose-1,6-bisphosphat + H2O → Fructose-6-phosphat + Pi
Allerdings ist ein anderes Enzym für die Reaktion zuständig, nämlich die Fructose-1,6-bisphosphatase. Dieses Enzym kommt nur in der Leber und der Niere des menschlichen Körpers vor, also kann auch nur hier die Gluconeogenese vollständig ablaufen.
Schritt 9
Die Glucose-6-phosphat-Isomerase der Glycolyse ist auch für den 9. Schritt der Gluconeogenese verantwortlich:
Fructose-6-phosphat → Glucose-6-phosphat
Schritt 10
Der letzte Schritt der Gluconeogenese, die Herstellung des Endprodukts Glucose, wird nicht von der Hexokinase katalysiert, dem ersten Enzym der Glycolyse. Stattdessen führt das Enzym Glucose-6-phosphatase diesen Schritt durch. Auch dieses Enzym kommt nur in der Leber und in der Niere vor.
Glucose-6-phosphat + H2O → Glucose + Pi
Gesamtreaktion
Fasst man alle 10 Schritte der Gluconeogenese zusammen, so erhält man [1]:
2 Pyruvat + 4 ATP + 2 GTP + 2 NADH/H+ + 4 H2O →
Glucose + 4 ADP + 2 GDP + 6 Pi + 2 NAD+
Wie man leicht sieht, ist die Gluconeogenese sehr energieaufwändig, um ein Molekül Glucose herzustellen, werden sechs Energieträger verbraucht, 4 ATP und 2 GTP. Insofern kann man sagen, dass die Gluconeogenese nur eine Art "Notprogramm" für den Organismus ist, das durchgeführt wird, wenn dem Körper, vor allem dem Gehirn, keine Glucose mehr zur Verfügung steht.
Energetische Aspekte
An sich ist die "nackte" Gluconeogenese eine sehr endotherme Reaktion. Durch die Hydrolyse von sechs Energieträgern allerdings wird mehr Energie freigesetzt, als für die Bildung von Glucose benötigt wird. Daher ist die Gluconeogenese insgesamt exotherm bzw. exergonisch: ΔG = -48 kJ/mol.
Würde man es irgendwie schaffen, die Glycolyse vollständig rückwärts ablaufen zu lassen, sähe die Energiebilanz wesentlich schlechter aus: ΔG = +90 kJ/mol.
Daher ist es quasi unmöglich, dass die Glycolyse komplett in umgekehrter Richtung abläuft. Viele Schritte der Glycolyse sind reversibel, das haben wir ja auch bei der Betrachtung der Schritte 2 bis 7 der Gluconeogenese gesehen. Aber drei Schritte der Glycolyse, nämlich die Phosphorylierungen, sind de facto nicht reversibel, da die Rückreaktion energetisch extrem ungünstig wäre. Auch wenn nur ein einziger Schritt einer solchen Reaktionskette nicht reversibel wäre, könnte die gesamte Kette nicht rückwärts ablaufen. Und bei der Glycolyse sind gleich drei solcher Schritte irreversibel.
Weitere Einzelheiten
Laut [2] endet die Gluconeogenese in den meisten Geweben beim Glucose-6-phosphat, Glucose selbst wird oft also gar nicht hergestellt. Das Glucose-6-phosphat wird dann zum Aufbau von Glycogen, dem tierischen Glucosespeicher, verwendet.
Ein nützlicher Nebeneffekt besteht darin, dass Glucose-6-phosphat als ionische Verbindung die Membran der Zellen nicht ohne weiteres passieren kann, während Glucose die Zelle ohne Probleme verlassen kann.
Freisetzung von Glucose
Die Aufgabe der Leber ist es, nach Möglichkeit den Blutzuckerspiegel (also die Glucose-Konzentration) aufrecht zu erhalten (Homöostase). Sinkt der Blutzuckerspiegel unter ein bestimmtes Maß, bauen die Leberzellen den Kohlenhydrat-Speicher Glycogen ab und geben Glucose in das Blut ab.
Allerdings findet der letzte Schritt der Gluconeogenese, also die Produktion von Glucose, nicht im Cytoplasma der Leberzellen statt, sondern im Lumen des endoplasmatischen Reticulums.
Die Glucose-6-phosphatase, die den letzten Schritt katalysiert, sitzt in der Membran des endoplasmatischen Reticulums. Das Enzym ist mit drei Transportproteinen assoziiert, die kurz als T1, T2 und T3 bezeichnet werden. T1 ist für den Transport des Glucose-6-phosphats in das ER zuständig. Das Enzym wandelt dann Glucose-6-phosphat in Glucose und anorganisches Phosphat Pi um. Das Protein T2 transportiert dann Pi in das Cytoplasma, während T3 die Glucose in das Cytoplasma befördert [2].
Regulation der Gluconeogenese und der Glycolyse
Beide Reaktionen sind exergonisch und könnten daher in der gleichen Zelle nebeneinander ablaufen, was natürlich völliger Unsinn wäre, nicht nur aus energetischer Sicht, sondern allgemein aus ökonomischer Sicht. Durch ausgefeilte Regulationsmechanismen (allosterische Enzyme an Schlüsselpositionen der Stoffwechselketten) wird gewährleistet, dass stets entweder die Glycolyse oder die Gluconeogenese abläuft.
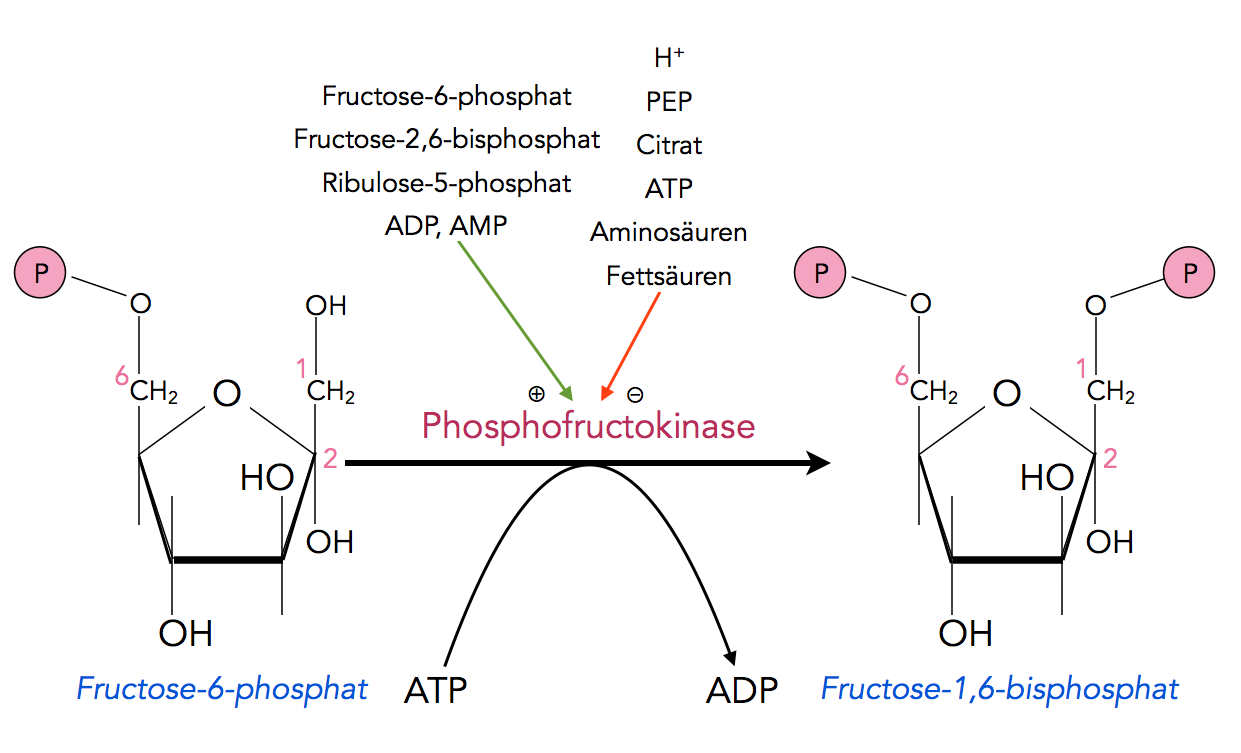
Regulation der Fructose-6-phosphat / Fructose-1,6-bisphospat-Umwandung
Ein solches Schlüsselenzym haben wir bereits bei der Glycolyse kennengelernt, nämlich die Phosphofructokinase:
Ist ein Überschuss an Fructose-6-phosphat vorhanden, erfolgt eine allosterische Substratinduktion dieses dritten Glycolyse-Schrittes. Auch wenn gerade viel Energie benötigt wird und daher viel ATP verbraucht wurde (und somit viel ADP vorliegt), wird die Glycolyse an dieser Stelle aktiviert, umgekehrt wird das entsprechende Enzym der Gluconeogenese, die Fructose-1,6-bisphosphatase, durch ADP und vor allem AMP gehemmt.
Bei der Gluconeogenese können Glycerin und Aminosäuren über die Bildung von Pyruvat zur Neubildung von Glucose verwertet werden. Daher hemmt eine hohe Konzentration an Aminosäuren die Glycolyse an dieser Stelle. Fette bestehen bekanntlich aus Glycerin und drei Fettsäuren. Liegt also eine hohe Fettsäure-Konzentration vor, ist gleichzeitig auch die Glycerin-Konzentration hoch, und Glycerin kann wiederum für die Gluconeogenese verwertet werden. Daher ist es sinnvoll, wenn die Glycolyse an dieser Stelle gehemmt wird.
Citrat, eine Schlüsselverbindung des Citratzyklus, hemmt die Glycolyse und fördert die Gluconeogenese. Liegt viel Citrat in der Zelle vor, ist das ja ein Zeichen dafür, dass viel Glucose abgebaut wurde. Daher macht die Hemmung der Glycolyse und die Förderung der Gluconeogenese durch Citrat Sinn.
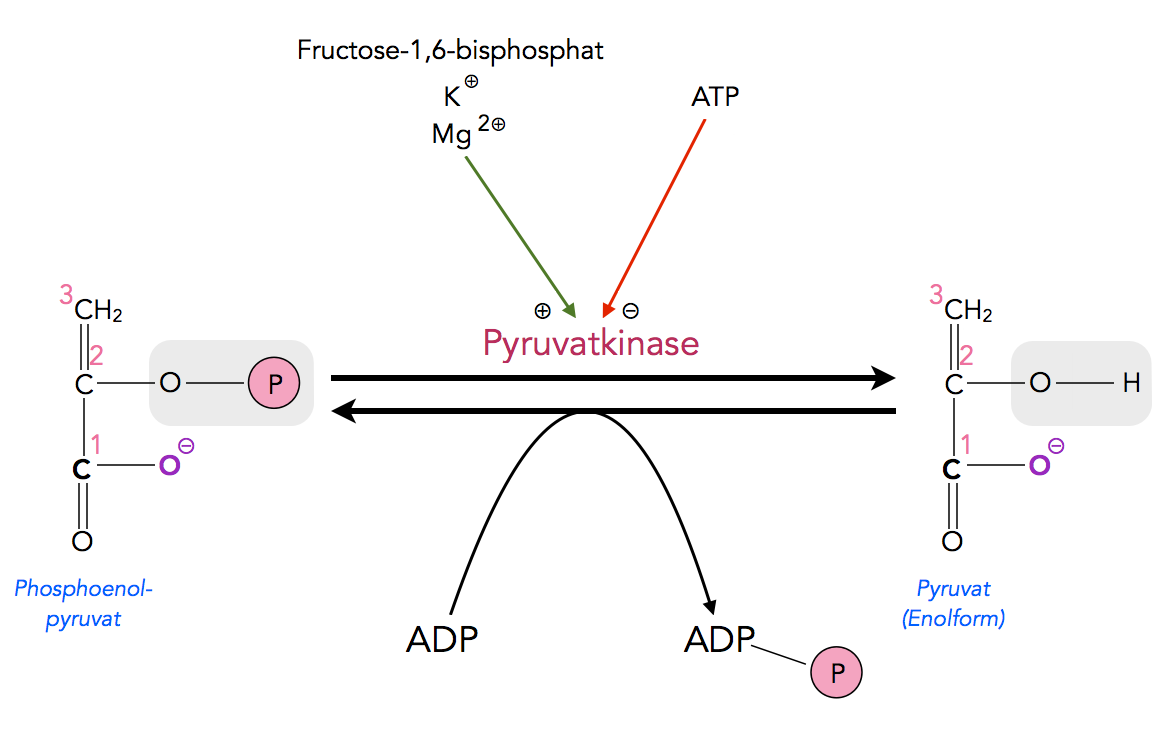
Regulation der Pyruvat / PEP - Umwandlung
Eine zweite Schlüsselstelle zur Regulation der Glycolyse und Gluconeogenese ist die Umwandlung von PEP in Pyruvat bei der Glycolyse bzw. die Umwandlung von Pyruvat in PEP bei der Gluconeogenese.
ATP hemmt diesen Schritt der Glycolyse, während ADP den entsprechenden Schritt der Gluconeogenese hemmt. Acetyl-CoA, das ja aus dem Pyruvat gebildet wird, das das Endprodukt der Glycolyse ist, aktiviert die Gluconeogenese an dieser Stelle. Eine hohe Acetyl-A-Konzentration bedeutet ja, dass viel Glucose verbraucht wurde. Also macht es Sinn, die Neusynthese von Glucose aus anderen Stoffen zu aktivieren.
Quellen:
- Nelson, Cox. Lehninger Principles of Biochemistry. Macmillan Learning, New York 2021.
- Berg, Tymoczko, Gatto jr., Stryer: Stryer Biochemie, 8. Auflage, Springer Berlin Heidelberg 2018.
- Alberts, Bruce et al. Molekularbiologie der Zelle, 6. Auflage, Weinheim 2017.
- Schlieper, Grundfragen der Ernährung, 21. Auflage, Hamburg 2014.
- Hahn, Ströhle, Wolters, Ernährung, 3. Auflage, Stuttgart 2016.