Eine Gruppe von künstlichen Makromolekülen (Kunststoffen, Copolymeren), die vor allem in der Textilindustrie Anwendung finden, wie folgendes Zitat aus dem Spiegel vom 18. Februar 2017 zeigt:
"Knitterfrei, formstabil und vor allem billig: Inzwischen enthalten rund 60 Prozent der Kleidung Polyester. Die Kunstfaser ist der große Treiber der Fast-Fashion-Industrie – und entpuppt sich als Recycling-Desaster."
Struktur
Ein Ester besteht in der Regel aus einem Alkohol, der unter Abspaltung von Wasser mit einer Carbonsäure reagiert hat. Das einfachste Beispiel für einen solchen Ester ist der Ameisensäure-methylester aus Methansäure (Ameisensäure) und Methanol (Methylalkohol).
Wenn ein Alkohol-Molekül zwei OH-Gruppen hat, wie zum Beispiel Ethylenglycol HO-CH2-CH2-OH, dann kann ein solcher Alkohol mit zwei Säure-Molekülen verestert werden:
Säure - Alkohol - Säure
Ein Alkohol mit drei OH-Gruppen kann sogar mit drei Säuren verestert werden, das kennt man ja beispielsweise von den Neutralfetten (Glycerin + 3 Fettsäuren).
Umgekehrt kann eine Carbonsäure mit zwei COOH-Gruppen gleichzeitig mit zwei Alkohol-Molekülen eine Ester-Bindung eingehen:
Alkohol - Säure - Alkohol
Was passiert nun, wenn man einen Alkohol mit zwei OH-Gruppen und eine Carbonsäure mit zwei COOH-Gruppen unter geeigneten Bedingungen zusammenrührt?
Jedes Alkohol-Molekül verbindet sich unter Wasser-Abgabe mit zwei Säure-Molekülen, und jedes Säure-Molekül wiederum geht mit je zwei Alkohol-Molekülen eine Ester-Bindung ein. Es entsteht ein langes Moleküle mit folgendem Aufbau:
Säure - Alkohol - Säure - Alkohol - Säure - Alkohol - ... Säure - Alkohol
Eine solche Verbindung bezeichnet man dann als Polyester.
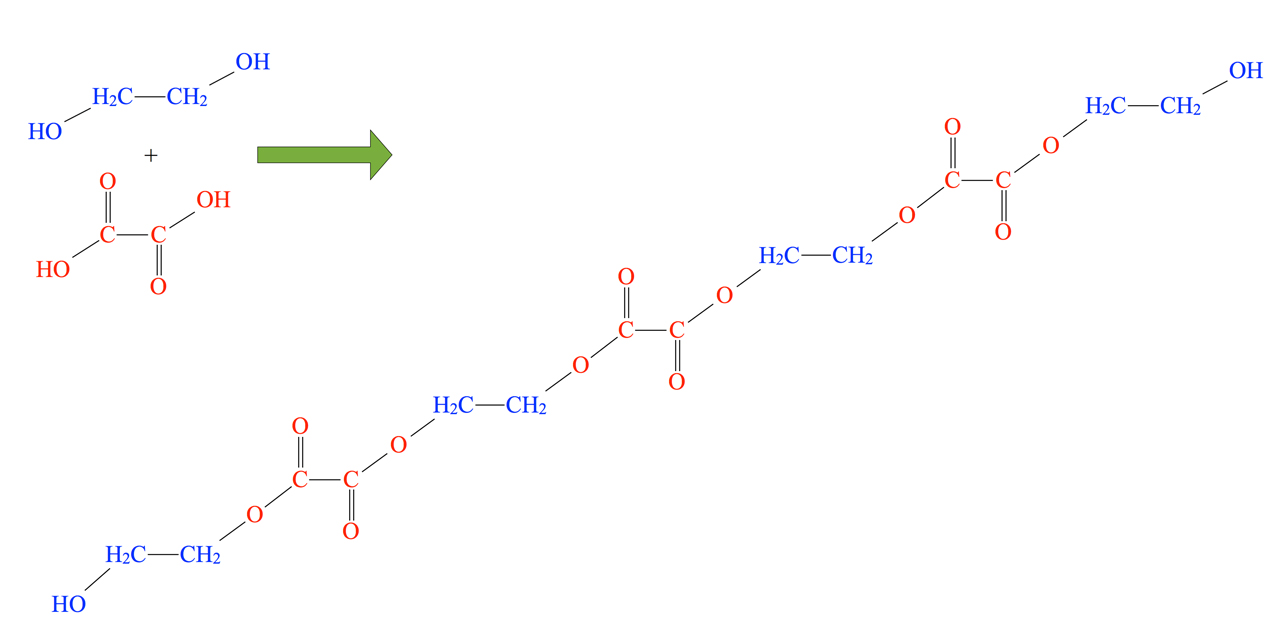
Hier sieht man einen "Mini-Polyester" bestehend aus vier Molekülen Ethylenglycol und drei Molekülen Oxalsäure. Echte Polyester bestehen natürlich aus Tausenden solcher Bausteine.
Weitere Einzelheiten zu Polyestern finden Sie auf meiner Seite "Polykondensation" in der Q2-Abteilung und natürlich auf der Polyester-Seite in der Wikipedia.