Entdeckung
Das Element Fluor wurde 1886 von Henri Moissan isoliert, als er eine Lösung von Kaliumhydrogendifluorid in flüssigem Fluorwasserstoff bei tiefen Temperaturen elektrolysierte. An sich war das Element Fluor schon länger bekannt, aber aufgrund seiner extrem hohen Reaktivität konnte es nicht isoliert werden. 1906 bekam Moissan den Chemie-Nobelpreis für die Isolierung von Fluor.
Vorkommen
Das sehr reaktive Halogen kommt als freies Element nicht vor. In gebundener Form findet es sich dagegen in vielen Salzen, vor allem in den Fluoriden. Das wichtigste Fluorid ist wohl das Calciumfluorid, auch Fluorit oder Flussspat genannt. Ein anderes relativ häufiges Mineral ist der Fluorapatit Ca5(PO4)3F, der auch die Hauptquelle für die Fluorgewinnung ist. Schließlich wäre hier das Mineral Kryolith Na3AlF6 zu nennen, das vor allem auf Grönland vorkam, aber heute fast ausgebeutet ist. In der Häufigkeitsliste der Elemente steht Fluor an der 14. Stelle, es kommt also relativ häufig vor.
Darstellung
Im Labor wird Fluor meistens durch thermische Zersetzung von Manganfluorid MnF4 gewonnen.
Herstellung
In der Industrie wird zunächst Fluorwasserstoff HF durch Reaktion von konz. Schwefelsäure mit Calciumfluorid gewonnen.
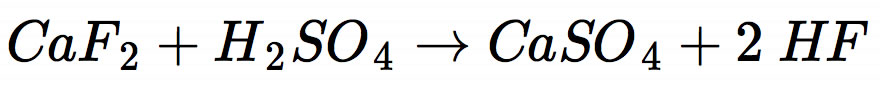
Dieser Fluorwasserstoff wird dann elektrochemisch in Wasserstoff und Fluor zerlegt:
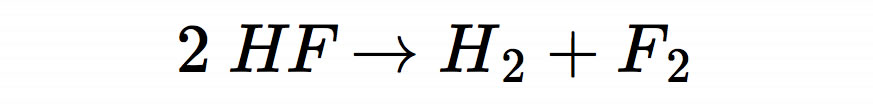
Die Einzelheiten dieses Verfahrens sind in dem Wikipedia-Artikel über Fluor genau erläutert.
Eigenschaften
physikalische Eigenschaften
Fluor ist bei Zimmertemperatur ein farbloses bis hellgelbes, beißend riechendes Gas. Der Siedepunkt beträgt -188 ºC, das kondensierte flüssige Fluor ist sehr gelb, es wird oft von "kanariengelber Farbe" gesprochen. Der Schmelzpunkt liegt bei -220 ºC.
chemische Eigenschaften
Fluor ist noch reaktiver als Chlor, es reagiert mit den meisten Elementen und mit vielen Verbindungen, auch mit organischen Verbindungen. Wie reaktiv Fluor ist, sieht man an der Reaktion mit Wasserstoff. Während ein Chlor-Wasserstoff-Gemisch belichtet oder anderes aktiviert werden muss, damit es zur explosionsartigen Reaktion kommt, reagiert Fluor mit Wasserstoff sofort, also ohne Belichtung oder sonstige Aktivierung. Selbst als Feststoff reagiert Fluor bei -200 ºC heftig mit Wasserstoff. Und jetzt kommt es noch extremer: Fluor reagiert auch mit Edelgasen! Mit Xenon bildet es zum Beispiel Xenon(II)-fluorid XeF2. Und das will schon wirklich etwas heißen!
Glas ist zunächst resistent gegen Fluor, bei höheren Temperaturen reagiert das Fluor aber auch mit Glas. Selbst Kunststoffe, die ja als recht stabil gegenüber Halogenen gelten, reagieren mit Fluor.
Verwendung
Wegen seiner extremen Reaktivität wird Fluor nicht sehr oft in der Industrie oder Technik eingesetzt. Zu den bekannteren Ausnahmen gehört die Herstellung von Uranhexafluorid UF6. Diese Verbindung spielt bei der Gewinnung bzw. Anreicherung des Uran-Isotops 235U in Gaszentrifugen eine wichtige Rolle.
Kunststoffe werden mit Fluor behandelt, die Oberfläche des Kunststoff-Gegenstandes reagiert mit Fluor und bildet dann eine stabile Schutzschicht. Es muss nur dafür gesorgt werden, dass das Fluor nicht weiter in den Gegenstand eindringt. Bei den Benzintanks von Autos spielt dies zum Beispiel eine Rolle. Die fluorierte Innenschicht verhindert ein Eindringen des Benzins in den Kunststoff.
Erwähnt werden muss hier noch unbedingt das Teflon, ein hochwertiger Kunststoff mit dem richtigen Namen Polytetrafluorethylen. Teflon ist beständig gegen starke Säuren und starke Laugen, und es wird von so gut wie keinem Lösemittel aufgelöst. Selbst Königswasser, mit dem man Gold auflösen kann, greift Teflon nicht an. Außerdem ist Teflon extrem hitzebeständig, es hat einen Schmelzpunkt von 327 ºC. Bei Temperaturen über 400 ºC zersetzt sich Teflon, wobei giftige Fluor-Gase freigesetzt werden. Weitere Einzelheiten siehe Lexikon-Artikel "Teflon" auf meiner Homepage.
Biologische Bedeutung
Das Element Fluor ist bekannt aus der Zahnpasta-Werbung. Fluor ist ein wichtiges Spurenelement, unser Körper enthält etwa 5 g Fluor, der größte Teil findet sich in den Knochen und Zähnen. Bekanntlich schützt Fluor vor Karies und härtet den Zahnschmelz. In einigen Ländern - nicht in Deutschland - wird daher sogar dem Trinkwasser Fluor hinzugefügt.