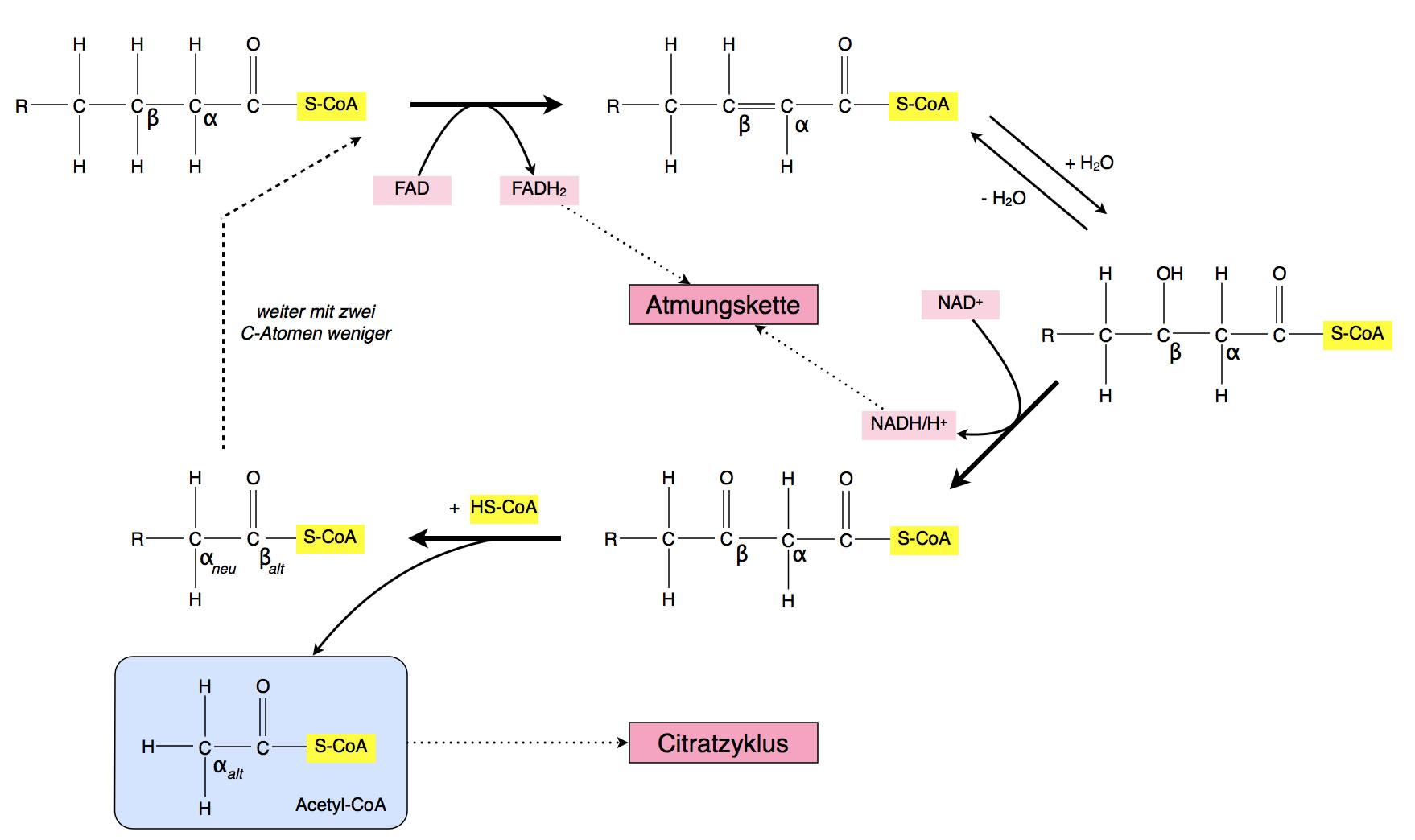
Die Versuche von Knoop
Im Jahre 1904 machte der deutsche Chemiker F. Knoop einen interessanten Versuch, der sehr entscheidende Erkenntnisse über den Abbau von Fettsäuren in den Zellen der Säugetiere erbrachte. Eine Reihe von Hunden bekam Fett zu essen - aber kein gewöhnliches Fett, sondern Fett, in dem die Fettsäuren am Omega-Ende auf besondere Weise markiert waren. Radioaktive Markierungen oder Markierungen mit Fluoreszenzfarbstoffen waren zu der damaligen Zeit noch nicht erfunden, aber chemische Markierungen konnten schon eingesetzt werden. Knoop verwendete Fettsäuren, an deren Omega-Ende ein H-Atom durch einen Benzolring ersetzt wurde.
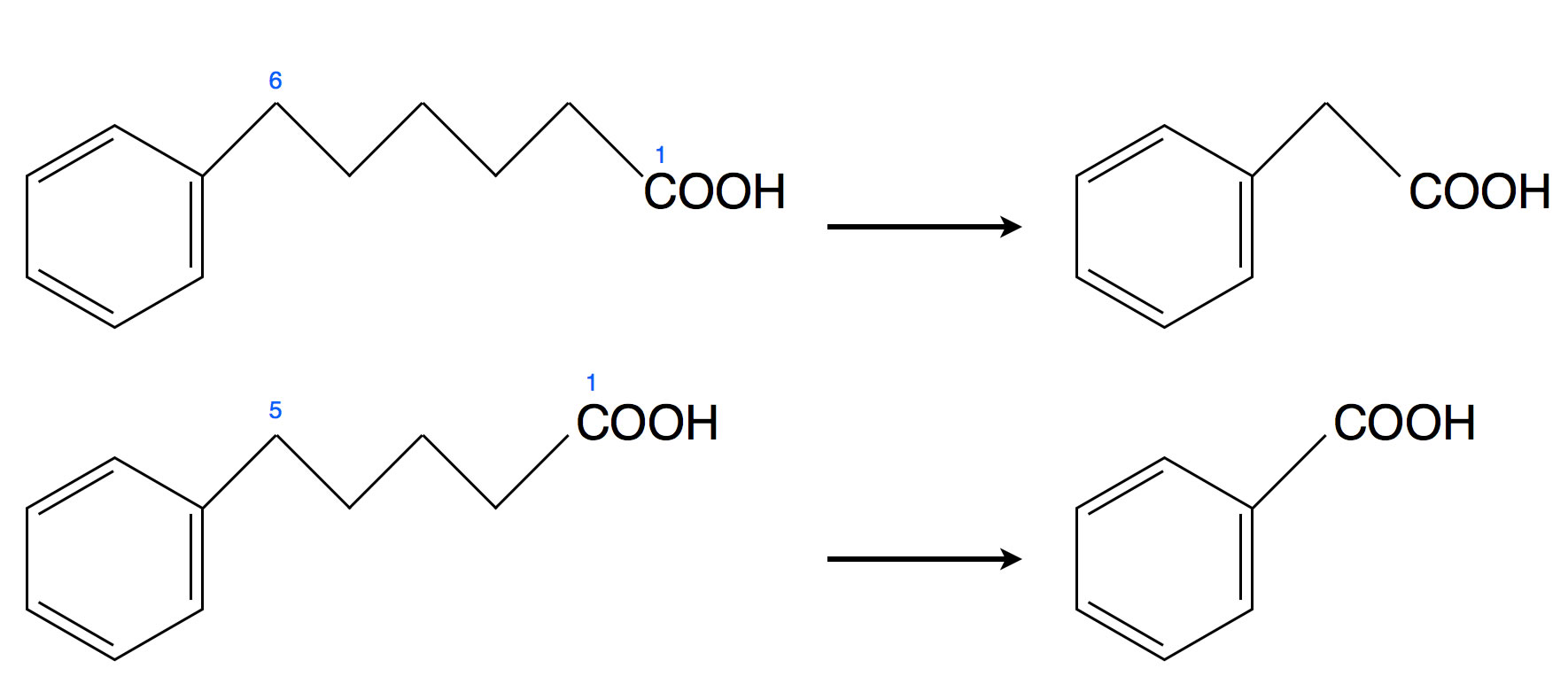
Die Versuche von F. Knoop
Ein Teil der Fettsäuren bestand aus einer geraden Anzahl von C-Atomen (obere Reihe), ein anderer Teil der Fettsäuren hatte eine ungerade Zahl von C-Atomen.
Die Abbauprodukte der Fettsäuren konnte Knoop dann im Urin der Hunde nachweisen. Im oberen Beispiel der Abbildung 1 hat sich die Zahl der Fettsäure-C-Atome von 6 auf 2 reduziert, im unteren Beispiel von 5 auf 1. Das heißt, es wurden immer genau vier C-Atome abgebaut. Bei ähnlich präparierten Fettsäuren mit 7 und 8 C-Atomen wurden immer genau sechs C-Atome abgebaut und so weiter.
Knoops Erkenntis aus diesen Versuchen lässt sich in einem Satz formulieren: Beim Abbau von Fettsäuren werden die C-Atome stets in Zweiergruppen entfernt.
Auf dem Bild sieht man, dass die COOH-Gruppe am alpha-Ende der Fettsäure erhalten bleibt. Das ist nicht ganz korrekt. Die COOH-Gruppe der Fettsäure wird zusammen mit dem zweiten C-Atom entfernt. Das dritte C-Atom, das sogenannte beta-C-Atom, wird dann wieder oxidiert, so dass sich eine neue COOH-Gruppe bildet.
Ablauf der beta-Oxidation[1][4]
Die beta-Oxidation "erleichtert" die Fettsäure um zwei C-Atome und gewinnt dadurch quasi ein Molekül Essigsäure. Auch dieser Vorgang verläuft wie so oft in der Biochemie in mehreren Schritten.
Oxidation durch FAD
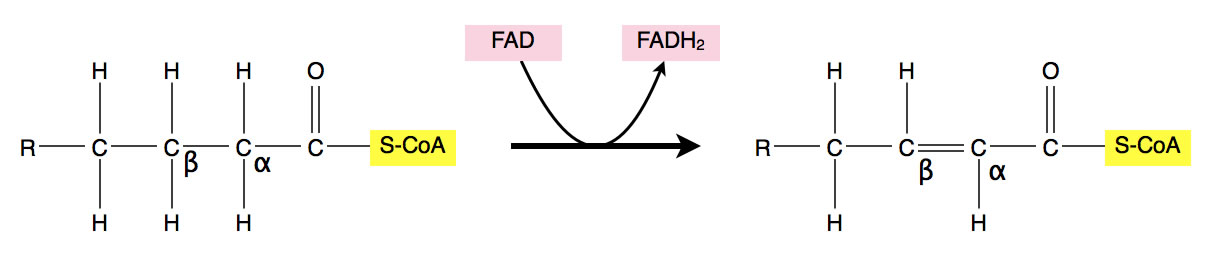
Oxidation einer Fettsäure durch FAD
Kurz zur Terminologie der C-Atome: Wenn man mit dem C-Atom der ehemaligen COOH-Gruppe beginnt, wird das direkt benachbarte zweite C-Atome das alpha-C-Atom genannt. Das dritte C-Atom ist dann das beta-C-Atom.
Im ersten Schritt der beta-Oxidation werden das alpha- und das beta-C-Atom oxidiert, indem Wasserstoff entzogen wird (Dehydrierung). Als Wasserstoff-Akzeptor tritt dabei das Coenzym FAD auf, das dabei zu FADH2 reduziert wird. Bei dieser Oxidation entsteht eine trans-Doppelbindung.
Für Chemie-Anfänger:
Bei C=C-Doppelbindungen kann man zwischen trans- und cis-Konfiguration unterscheiden. Bei der trans-Konfiguration befindet sich die eine Alkylgruppe auf der einen Seite der Doppelbindung und die andere Alkylgruppe auf der gegenüberliegenden Seite. Bei der cis-Konfiguration befinden sich beide Alkylgruppen auf der gleichen Seite. Wer Einzelheiten dazu wissen möchte, geht auf die Lexikonseite zur cis-trans-Isomerie.
Dieser Schritt ist notwendig, da das Enzym, das für den nächsten Schritt zuständig ist, nur Fettsäuren in trans-Konfiguration als Substrat erkennt, was natürlich an der Struktur des aktiven Zentrums dieses Enzyms liegt (Schlüssel-Schloss-Prinzip).
Hydratisierung
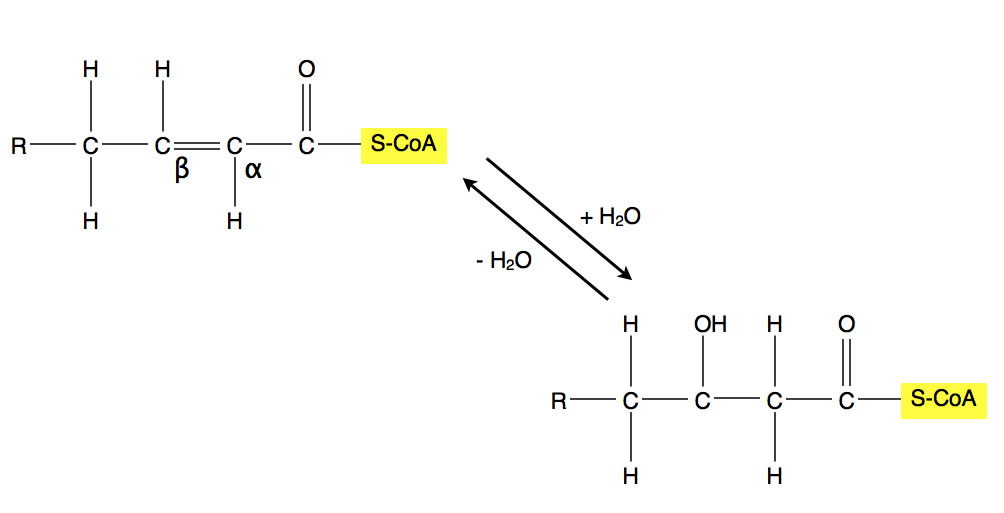
Addition von Wasser an die neue Doppelbindung
Im zweiten Schritt wird ein Wasser-Molekül an die neu entstandene Doppelbindung addiert. Das beta-C-Atom erhält so eine OH-Gruppe. Wer jetzt ein wenig Ahnung von Biochemie hat, weiß schon, was als Nächstes kommt: Die OH-Gruppe wird oxidiert, so dass eine neue Carbonylgruppe entsteht.
Oxidation durch NAD+
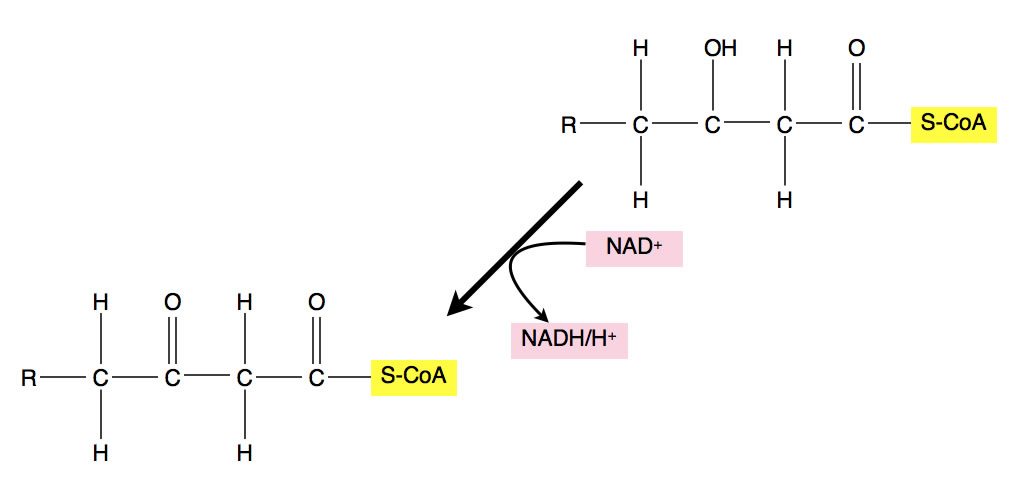
Oxidation der OH-Gruppe
Das Reaktionsprodukt besitzt jetzt zwei C=O-Gruppen: Eine in der ehemaligen COOH-Gruppe, und eine am beta-C-Atom. Wer jetzt genau hinsieht, kann schon ein Essigsäure-Molekül in dem Reaktionsprodukt erkennen. Für die Leute, die das noch nicht sehen, habe ich das obige Bild mal etwas verändert:
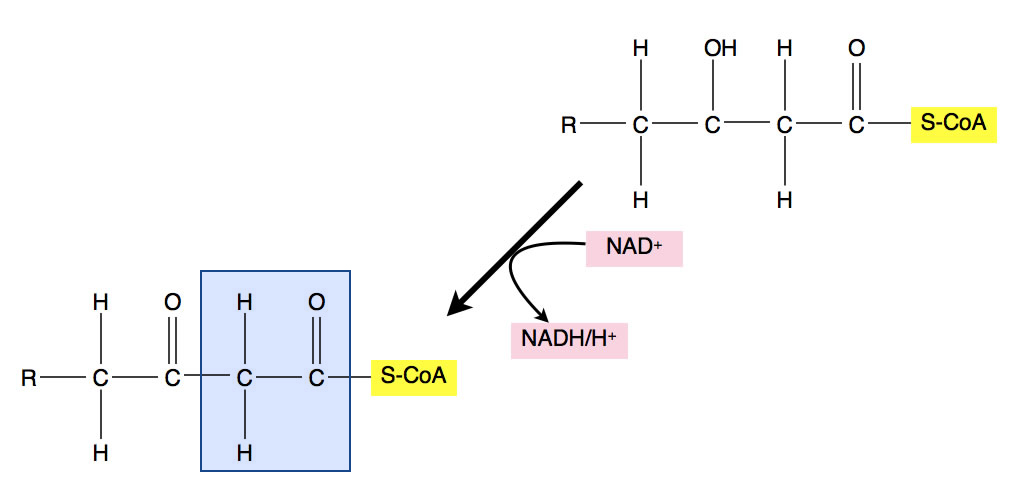
Oxidation der OH-Gruppe
Die Acetylgruppe ist im Prinzip ein Essigsäure-Rest. Allerdigs darf man diesen Rest nicht mit dem negativ geladenem Acetat-Ion verwechseln: Acetylrest = CH3-C=O-; Acetat-Ion = CH3-COO-.
Thiolyse
Die jetzt zweifach oxidierte Fettsäure (einmal durch FAD, einmal durch NAD+) trennt nun die Acetylgruppe mit dem daran hängenden Coenzym-A-Molekül ab:
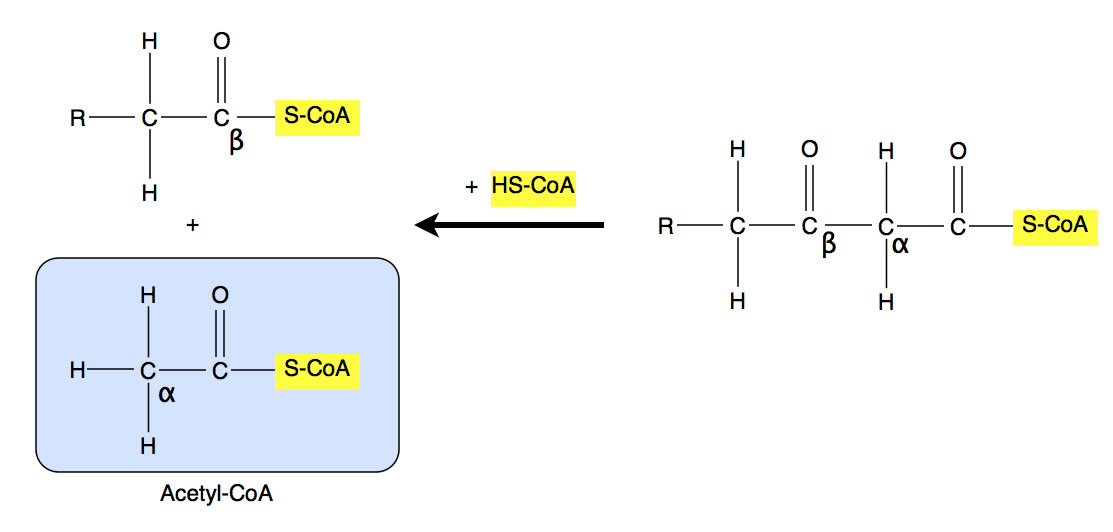
Abspaltung von Acetyl-CoA
Ein weiteres CoA-Molekül kommt dazu und setzt sich an die restliche Fettsäure, die jetzt um zwei C-Atome verkürzt ist.
Gesamtschau
Hier sehen wir noch einmal alle vier Schritte der beta-Oxidation in einer Zusammenfassung. Bei einer Fettsäure wie Stearinsäure mit 18 C-Atomen muss diese beta-Oxidation also neunmal ablaufen, bis die gesamte Fettsäure abgebaut ist.
Probleme
Bei ungeradzahligen gesättigten Fettsäuren entsteht ebenfalls Acetyl-CoA aus jeweils zwei C-Atomen. Nur wenn die letzten drei C-Atome abgebaut werden müssen, gibt es ein Problem. Dieses Problem wird dadurch gelöst, dass am Ende nicht Acetyl-CoA entsteht, sondern Propionyl-CoA, also eine Verbindung mit einem C-Atom mehr.
Bei ungesättigten Fettsäuren gibt es ebenfalls Probleme, weil die Enzyme der beta-Oxidation nicht mit den cis-Doppelbindungen zurecht kommen. Diese cis-Doppelbindungen müssen durch weitere Schritte und weitere Enzyme erst in trans-Doppelbindungen umgewandelt werden, damit die Hydratisierung erfolgen kann.
Energieausbeute
Wie man in der Abbildung 7 leicht sehen kann, entstehen pro "Runde" der beta-Oxidation eine FADH2- und ein NADH/H+-Einheit. Das sind also zwei Reduktionsäquivalente, die direkt in die Atmungskette der Mitochondrien eingespeist werden können.
Nicht zu vergessen ist das Acetyl-CoA, das ja eigentlich das Hauptprodukt der beta-Oxidation darstellt. Das Acetyl-CoA kann direkt in den Citratzyklus eingespeist und dort zu Redukationsäquivalenten abgebaut werden, die dann wieder in die Atmungskette einfließen.
Beispiel Palmitinsäure[1]
Löffler hat in seinem Buch die Energiebilanz für den Abbau der Palmitinsäure aufgestellt und kommt zu folgendem Ergebnis:
Die vollständige Oxidation der Palmitinsäure (16 C-Atome) liefert 8 Acetyl-CoA-Moleküle. Dazu muss die beta-Oxidation 7 mal durchlaufen werden, wobei 7 FADH2 und 7 NADP/H+ entstehen.
Wenn in der Atmungskette FADH2 oxidiert wird, entstehen 2 Moleküle ATP. Bei der Oxidation von NADP/H+ entstehen sogar 3 ATP-Moleküle. Pro Durchlauf der beta-Oxidation sind das dann 5 Moleküle ATP, bei einem siebenmaligem Durchlauf also 35 Moleküle ATP.
Wird Acetyl-CoA in den Citratzyklus eingespeist, werden ebenfalls Reduktionsäquivalente hergestellt. Pro Acetyl-CoA entstehen in der Atmungskette dann 12 ATP. Bei 8 Molekülen Acetyl-CoA sind das dann 96 ATP-Moleküle.
Zusammen ergibt das dann die eindrucksvolle Zahl von 131 ATP-Molekülen, die aus einem Palmitinsäure-Molekül gewonnen werden können. Allerdings muss man 2 ATP-Moleküle abziehen, die für die Bildung der aktivierten Fettsäure benötigt worden sind. In der Gesamtbilanz kann also ein Palmitinsäure-Molekül 129 ATP-Moleküle liefern.
Vergleich langkettige - kurzkettige Fettsäuren
Interessant wird es, wenn man die Energieausbeute langkettiger und kurzkettiger Fettsäuren vergleicht. Eine kurzkettige Fettsäure mit - sagen wir mal - 6 C-Atomen durchläuft die beta-Oxidation zweimal. Dabei entstehen 3 Acetyl-CoA-Moleküle sowie 2 FADH2 und 2 NADP/H+, die in der Atmungskette zu 10 ATP verwertet werden. Aus den 3 Acetyl-CoA-Molekülen entstehen 36 ATP, zusammen sind das dann 46 ATP. Von diesen 46 ATP aber müssen 2 ATP für die Aktivierung der Fettsäure abgezogen werden. Von den 46 gewonnenen ATP bleiben also nur 44 übrig, das sind 95,7%. Bei dem Abbau von Palmitinsäure dagegen bleiben von 131 gewonnen ATP 129 übrig, das sind 98,5%.
Je länger eine Fettsäure also ist, desto günstiger ist sie für die Energiegewinnung. Das liegt daran, dass eine Fettsäure nur einmal aktiviert werden muss, unabhängig davon wie viele C-Atome sie hat[5].
Quellen:
- Löffler, Funktionelle Biochemie, Berlin 1994
- Landesbildungsserver Baden-Württemberg, "Abbau von Glycerin"
- Römpp Chemie-Lexikon, 9. Auflage 1992
- Wikipedia, Artikel "beta-Oxidation"
- Schlieper, Grundfragen der Ernährung, Hamburg 2017