KI-Zusammenfassung
Die Ringspannung bezeichnet die energetische Destabilisierung von ringförmigen Molekülen gegenüber spannungsfreien Kettenverbindungen. Sie setzt sich aus drei Beiträgen zusammen: Baeyer-Spannung (Winkelspannung durch Abweichung von idealen Bindungswinkeln), Pitzer-Spannung (torsionale Spannung durch ekliptische Bindungen) und Prelog-Spannung (transannulare sterische Abstoßungen nicht benachbarter Atome im Ring). Die Größe der Ringspannung hängt stark von der Ringgröße und Konformation ab und erklärt viele physikalische und chemische Eigenschaften der Cycloalkane.
Allgemeines zur Ringspannung
"Die Ringspannung ist eine zusätzliche chemische Bindungsenergie, die in einem aus mehreren Atomen gebildeten ringförmigen Molekül (bspw.: Cyclobutan) gespeichert ist beziehungsweise zuvor für dessen Ringschluss aufgewendet werden muss. Sie ist in den meisten Fällen umso größer, je kleiner der Ring ist. Ihre Ursache sind verschiedene stereochemische Effekte, vor allem die Winkelspannung. " [1]
Ringspannung bei Cycloalkanen
Dieses wichtige Thema wurde auf einer eigenen Seite in der Abteilung "Studienvorbereitung Organische Chemie" ausführlich erläutert.
Die folgende Graphik zeigt die Ringenergien der Cycloalkane C3 bis C16. Die Daten stammen aus der engl. Wikipedia.
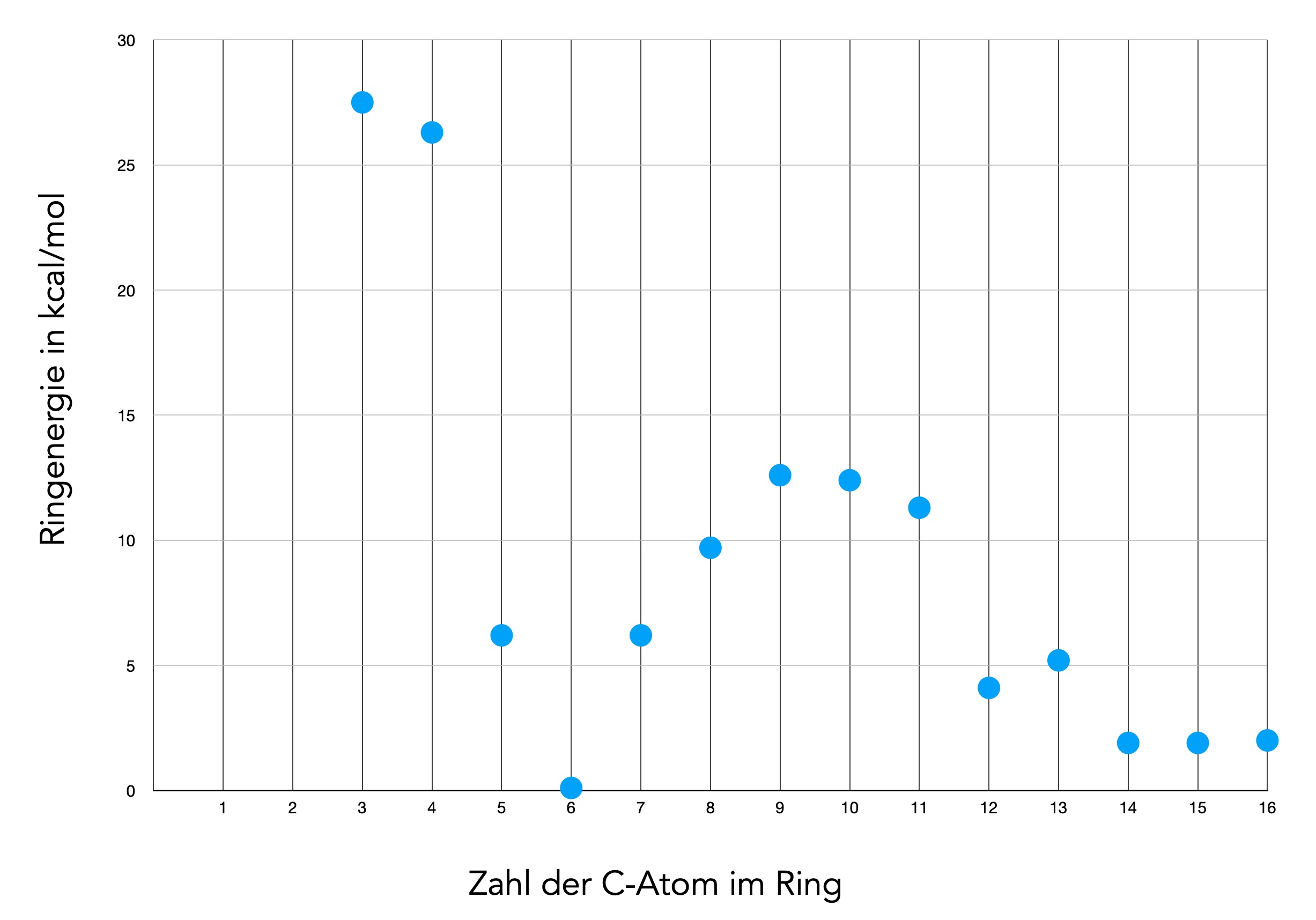
Abhängigkeit der Ringenergie von der Ringgröße
Autor: Ulrich Helmich 01/2026. Daten aus der engl. Wikipedia. Lizenz: Public domain
Man sieht sehr schön, dass die Ringenergie bei kleinen Ringen (C3, C4) am größten ist, hauptverantwortlich hierfür ist vor allem die Baeyer-Spannung (Winkelspannung), weil die C-C-C-Bindungswinkel im Ring sehr stark von dem Tetraederwinkel abweichen. Zusätzlich trägt bei diesen kleinen Ringen auch eine erhebliche Pitzer-Spannung (Torsionsspannung) durch ekliptische Bindungen zur hohen Ringspannung bei.
Bei mittleren Ringen (C5 bis C7) ist die Ringspannung sehr gering und erreicht ihr Minimum beim Cyclohexan. Cylohexan nimmt eine Sessel-Konformation ein, bei der sowohl die Winkelspannung fast 0 ist und bei der auch die Torsionsspannung so gut wie keine Rolle spielt. Eine transannulare Wechselwirkung ist bei dem mittelgroßen Molekül noch nicht vorhanden.
Bei größeren Ringen (C8 bis C11) nimmt die Ringspannung wieder zu. Ursache hierfür sind zunehmend transannulare Wechselwirkungen (Prelog-Spannung), bei denen sich nicht benachbarte Atome oder Gruppen über den Ring hinweg räumlich zu nahe kommen.
Wenn die Ringe noch größer werden (ab C12), können die Moleküle ihre Konformation so anpassen, dass sich gegenüberliegende Atome wieder weiter voneinander entfernen. Dadurch nimmt die transannulare Spannung erneut ab, und die Ringspannung wird insgesamt wieder kleiner.
Quellen:
- Wikipedia, Artikel "Ringspannung", abgerufen am 31.01.2026
- LaTSCHA, H.P; Kazmaier, U.; Klein, H.: Organische Chemie - Chemie Basiswissen II. 8. Auflage, Springer-Spektrum 2023.
- Laborhelfer.de, Artikel "Ringspannung", abgerufen am 31.01.2026
- engl. Wikipedia, Artikel "Ring strain", abgerufen am 31.01.2026