KI-Zusammenfassung (bearbeitet)
Aminosäuren sind die Bausteine der Proteine. Chemisch gesehen sind es Aminocarbonsäuren, also Verbindungen mit einer Amino-Gruppe, einer Carboxy-Gruppe, einem H-Atom und einem variablen Rest am zentralen C-Atom.
In wässriger Lösung liegen sie oft als Zwitterionen vor und können je nach pH-Wert positiv, negativ oder insgesamt neutral geladen sein.
Besonders wichtig sind die 20 proteinogenen Aminosäuren, die sich nach ihren Seitenketten zum Beispiel in unpolare, polare, saure und basische Aminosäuren einteilen lassen.
Einige Aminosäuren sind für den Menschen essentiell und müssen mit der Nahrung aufgenommen werden.
Diese KI-Zusammenfassung wurde im März 2026 von ChatGPT erstellt und von mir dann überarbeitet.
Die beiden einfachsten Aminosäuren
Aminosäuren sind chemisch gesehen Carbonsäuren mit mindestens einer Amino-Gruppe und müssten daher genauer als Aminocarbonsäuren bezeichnet werden. Die einfachste proteinogene Aminosäure ist Glycin. Es lässt sich formal von der Essigsäure ableiten und kann daher auch als Aminoessigsäure oder systematisch als 2-Aminoethansäure bezeichnet werden:
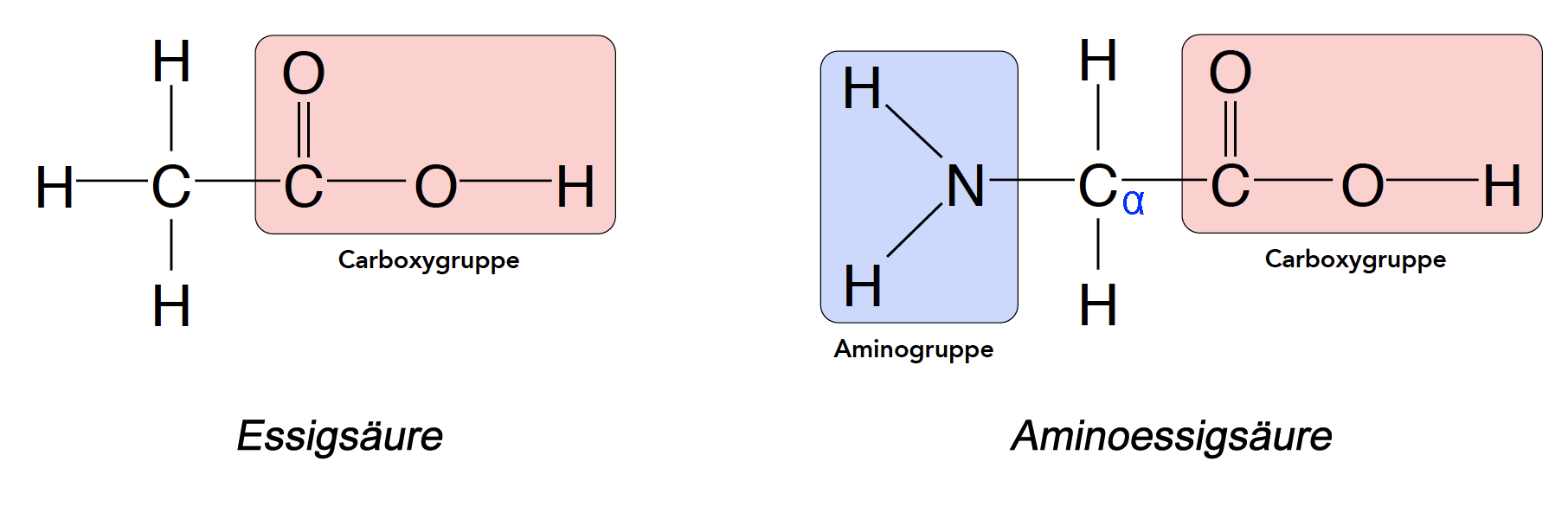
Aminosäuren sind mit der Essigsäure verwandt
Autor: Ulrich Helmich, Lizenz: Public domain
Die zweit-einfachste proteinogene Aminosäure ist das von der Propansäure abgeleitete Alanin. Der systematische Name lautet 2-Aminopropansäure:
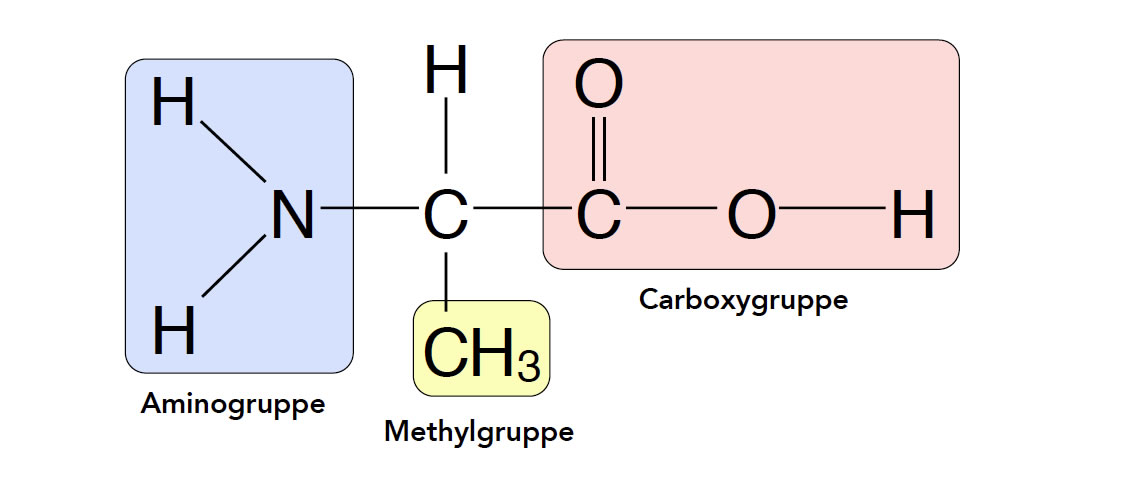
Das Alanin-Molekül
Autor: Ulrich Helmich, Lizenz: Public domain
Beim Alanin ist ein H-Atom am C2-Atom der Propansäure durch eine Amino-Gruppe ersetzt. Daher ist der wissenschaftliche Name des Alanins 2-Aminopropansäure.
Glycin ist die einzige proteinogene Aminosäure, deren zentrales C-Atom nicht chiral ist. Alanin besitzt dagegen bereits ein chirales C-Atom; deshalb gibt es Alanin in zwei spiegelbildlichen Formen. In Proteinen kommt fast ausschließlich die L-Form vor.
Allgemeiner Aufbau einer Aminosäure
Es gibt Hunderte von Aminosäuren in Natur und Technik, aber besonders wichtig sind die sogenannten proteinogenen Aminosäuren (proteinogen = Protein bildend). Diese 20 Aminosäuren - in Sonderfällen auch 21 oder 22 - sind die Bausteine der Peptide und Proteine. Hier einmal der allgemeine Aufbau einer proteinogenen Aminosäure:
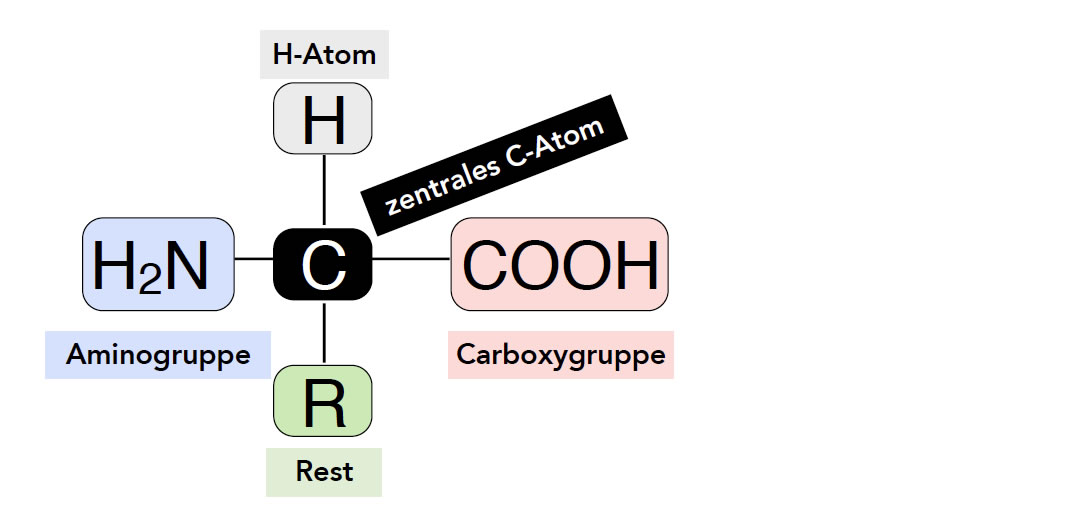
Allgemeiner Grundaufbau einer proteinogenen Aminosäure
Autor: Ulrich Helmich, Lizenz: Public domain
Ein zentrales C-Atom ist verbunden mit
- einer Amino-Gruppe NH2
- einer Carboxy-Gruppe COOH
- einem H-Atom
- einem variablen Rest R
Dieses zentrale C-Atom wird oft als α-C-Atom bezeichnet. Der Rest R bestimmt die besonderen chemischen Eigenschaften der jeweiligen Aminosäure.
Proteinogen und biogen - ein Unterschied
Als proteinogene Aminosäuren bezeichnet man die Aminosäuren, die während der Translation in entstehende Proteine eingebaut werden. Für die 20 Standard-Aminosäuren existieren Codons im genetischen Code; in Sonderfällen können auch Selenocystein und Pyrrolysin eingebaut werden.
Die biogenen Aminosäuren sind dagegen alle Aminosäuren, die in Lebewesen vorkommen oder von ihnen gebildet werden. Dazu gehören natürlich die proteinogenen Aminosäuren, aber auch viele weitere Aminosäuren wie Ornithin, Citrullin, GABA oder Taurin. Diese Aminosäuren entstehen im Stoffwechsel aus anderen Aminosäuren, Kohlenhydraten, Fetten oder anderen Verbindungen. Einzelheiten dazu siehe "Biogene Aminosäuren" auf dieser Homepage.
Eigenschaften der Carboxyl- und der Amino-Gruppe
Die Carboxy-Gruppe ist sauer
Die Carboxy-Gruppe verleiht der Aminosäure ihre sauren Eigenschaften. Sie ist in der Lage, ein Proton abzugeben. Das geschieht vor allem dann, wenn sich die Aminosäure in einem protonenarmen neutralen oder alkalischen Lösungsmittel befindet.
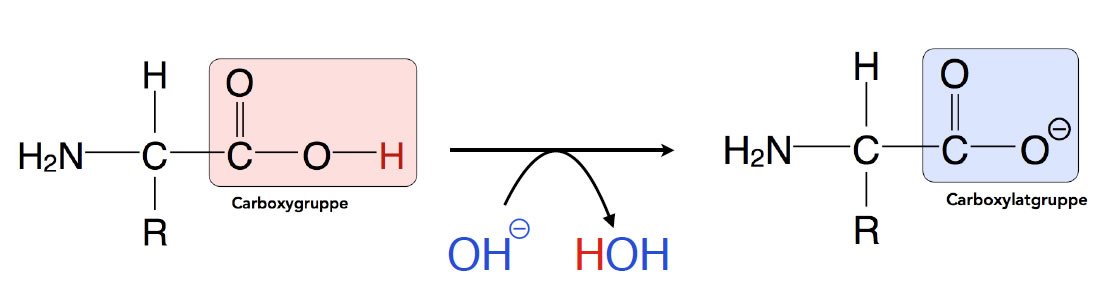
Die Carboxy-Gruppe kann ein Proton an eine Base abgeben
Autor: Ulrich Helmich, Lizenz: Public domain
Damit die Carboxy-Gruppe ihr Proton abgeben kann, muss natürlich eine Base aus der Umgebung bereit sein, dieses Proton aufzunehmen. In wässrigen Lösungen übernimmt häufig Wasser diese Rolle; bei höheren pH-Werten kommen auch Hydroxid-Ionen OH- in Frage. Die Carboxy-Gruppe liegt danach als Carboxylat-Gruppe COO- vor.
Die Amino-Gruppe ist basisch
Die Amino-Gruppe verleiht der Aminosäure ihre basischen Eigenschaften. Das elektronegative Stickstoff-Atom besitzt ein freies Elektronenpaar und verhält sich daher als Base. Es kann also ein Proton aufnehmen; dadurch wird aus der Amino-Gruppe eine NH3+-Gruppe:
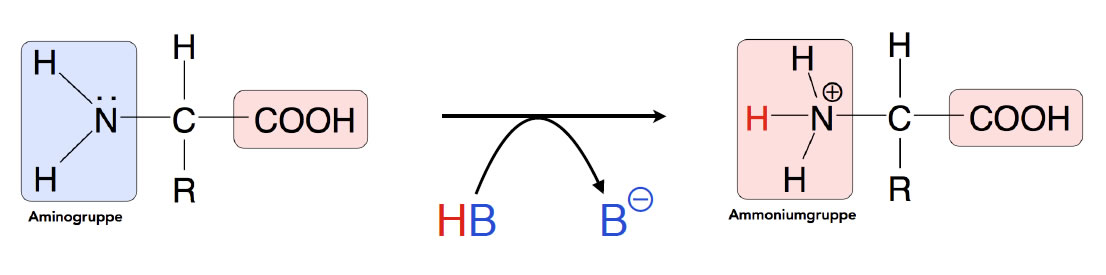
Die Amino-Gruppe kann ein Proton von einer Säure aufnehmen
Autor: Ulrich Helmich, Lizenz: Public domain
Das Proton H+ muss natürlich irgendwo herkommen. Diese Protonenaufnahme funktioniert also nur dann, wenn ein Protonendonator, also eine Säure, im Lösungsmittel vorhanden ist. In der Abbildung wird die Säure durch HB symbolisiert. Aus der Amino-Gruppe ist dann eine Ammonium-Gruppe geworden.
Bildung von Zwitterionen
Aminosäuren liegen in Wasser oft nicht als ungeladene Moleküle vor, sondern als sogenannte Zwitterionen:
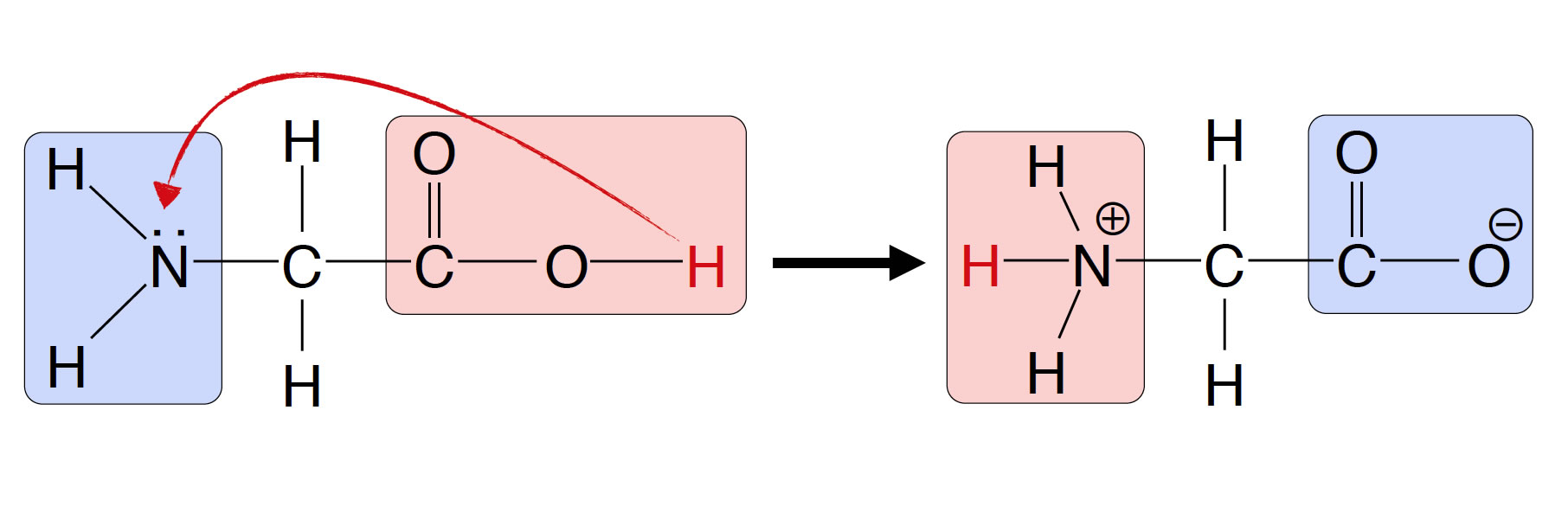
Bildung eines Zwitterions
Autor: Ulrich Helmich, Lizenz: Public domain
Die Carboxy-Gruppe reagiert als Säure und gibt ein Proton ab, die Amino-Gruppe reagiert als Base und nimmt ein Proton auf. Es entsteht ein Zwitterion, das gleichzeitig eine positive und eine negative Ladung trägt, insgesamt aber elektrisch neutral ist.
Ob das abgegebene Proton direkt an die Amino-Gruppe derselben Aminosäure übergeht, wie es in vielen Formeldarstellungen angedeutet wird, ist eher unwahrscheinlich. In wässriger Lösung werden Protonen vielmehr über das Lösungsmittel übertragen.
Die pH-Abhängigkeit der Ladung einer Aminosäure
Eine Aminosäure kann je nach pH-Wert des Lösungsmittels positiv oder negativ geladen sein oder als Zwitterion vorliegen. Betrachten wir dazu die folgende Abbildung:
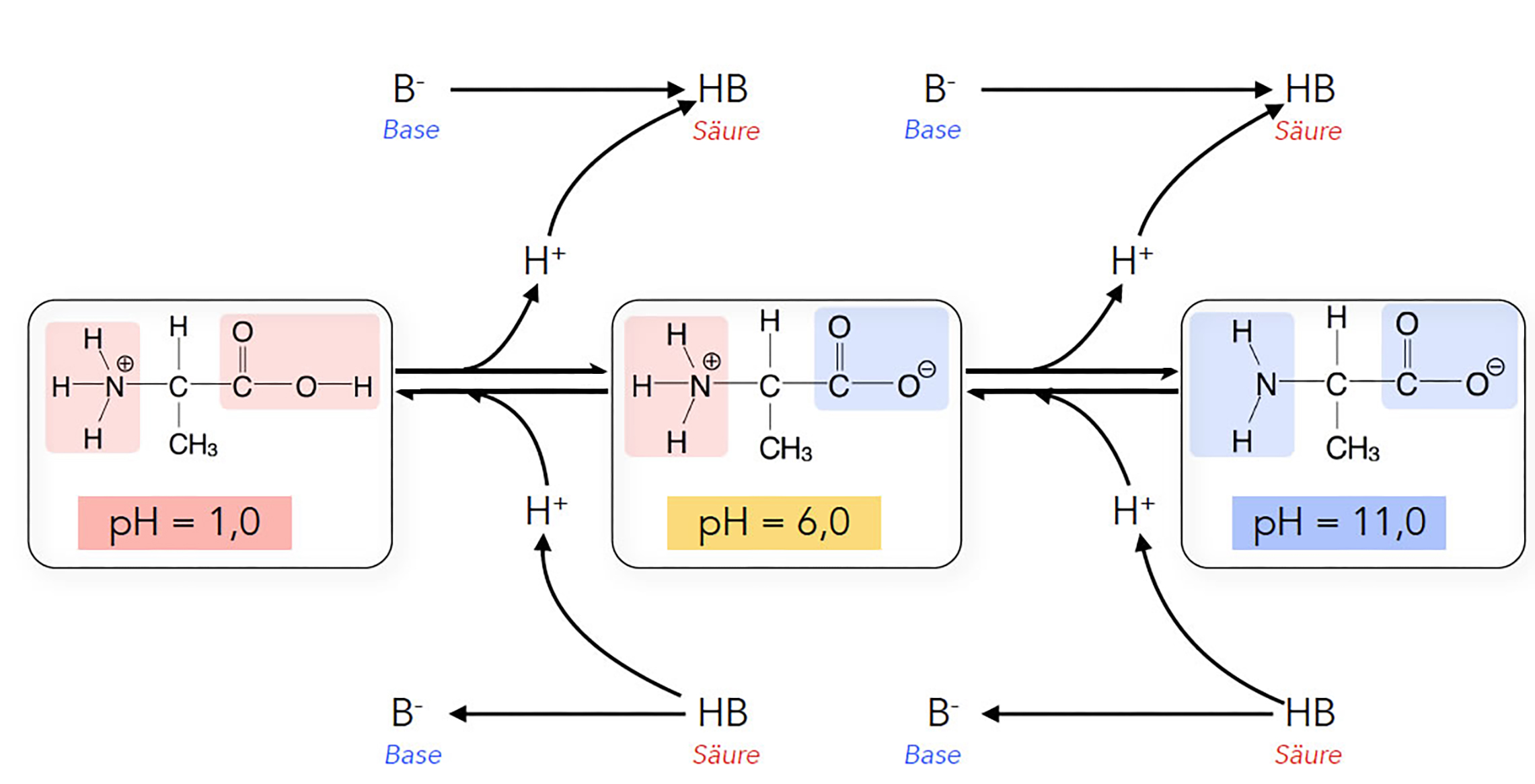
Die pH-Abhängigkeit der Ladung einer Aminosäure
Autor: Ulrich Helmich, Lizenz: Public domain
Bei einem pH-Wert von 1 hat die Amino-Gruppe ein Proton aufgenommen, und auch die COOH-Gruppe behält ihr Proton in einem derart sauren und protonenreichen Lösungsmittel. Die Aminosäure liegt daher insgesamt positiv geladen vor.
Gibt man jetzt eine Lauge in das Lösemittel, steigt der pH-Wert, die Konzentration der OH--Ionen im Lösemittel nimmt zu, die Konzentration der H+-Ionen nimmt ab. Offensichtlich hat die Carboxy-Gruppe stärkere Säureeigenschaften als die Ammoniumgruppe, denn sie gibt ihr Proton zuerst ab und liegt dann als negativ geladene Carboxylat-Gruppe vor, während die Ammonium-Gruppe immer noch positiv geladen ist. Die Aminosäure liegt jetzt also als Zwitterion vor.
Wenn der pH-Wert noch weiter steigt, beispielsweise auf pH = 11, liegen noch weniger Protonen im Lösungsmittel vor. Der "Zwang", ein Proton an das Lösemittel abzugeben, wird dadurch noch größer (Le-Chateliersches Gesetz oder "Prinzip des kleinsten Zwangs"). Daher gibt schließlich auch die Ammonium-Gruppe ihr zusätzliches Proton an das Lösungsmittel ab und wird zur elektrisch neutralen Amino-Gruppe
Isoelektrischer Punkt
Den pH-Wert, bei dem eine Aminosäure nach außen hin keine Nettoladung trägt (also als Zwitteion vorliegt), bezeichnet man als isoelektrischen Punkt. Dieser Wert ist eine charakteristische Stoffeigenschaft jeder Aminosäure.
Isoelektrischer Punkt = der pH-Wert, bei dem die Nettoladung einer Aminosäure 0 ist.
Auf der Lexikon-Seite "Aminosäuren (chemische Aspekte)" finden Sie weitere Informationen zu diesem Thema. Außerdem wird dort auch die Stereo-Chemie der Aminosäuren besprochen.
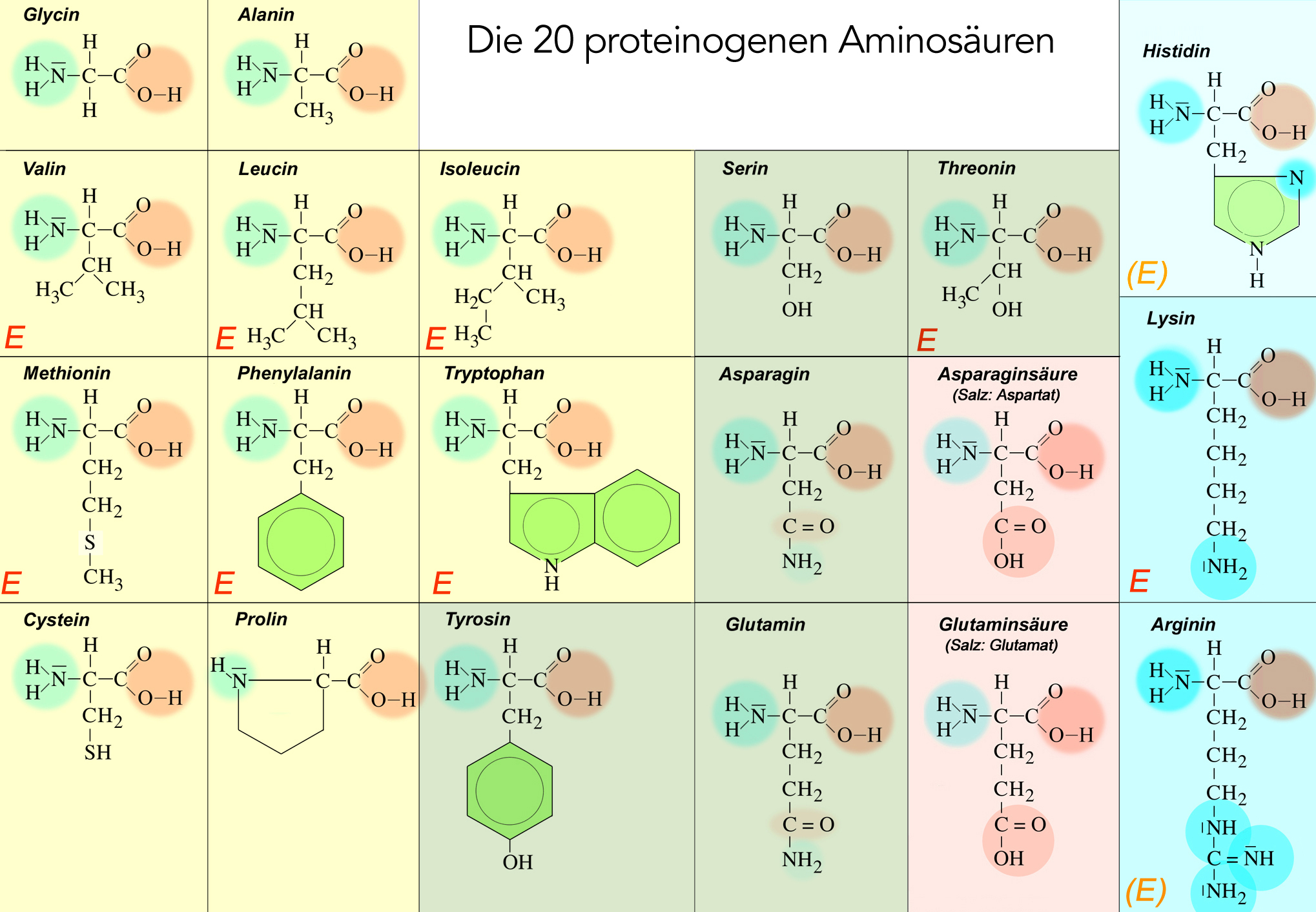
Überblick über die 20 proteinogenen Aminosäuren
Hier sehen Sie die 20 Standard-Aminosäuren, aus denen die meisten Proteine aufgebaut sind.
Einteilung der Aminosäuren
Die proteinogenen Aminosäuren kann man nach verschiedenen Kriterien in mehrere Gruppen einteilen. In Ernährungslehre und Medizin sehr gebräuchlich ist die Einteilung in essentielle, nicht-essentielle und bedingt essentielle Aminosäuren.
Essentielle Aminosäuren
Viele Aminosäuren kann der menschliche Körper selbst herstellen. Einige müssen jedoch mit der Nahrung aufgenommen werden. Sie sind beispielsweise in Fisch, Fleisch, Milchprodukten, Eiern, Hülsenfrüchten und Nüssen enthalten. Diese wichtigen Aminosäuren bezeichnet man als essentielle Aminosäuren.
Essentielle Aminosäuren = Aminosäuren, die der Körper nicht in ausreichender Menge selbst herstellen kann und die deshalb mit der Nahrung aufgenommen werden müssen.
Zu den für den Menschen essentiellen Aminosäuren zählen Valin, Leucin, Isoleucin, Methionin, Phenylalanin, Tryptophan, Threonin, Lysin und Histidin. Arginin ist vor allem in Wachstumsphasen und in bestimmten Stoffwechselsituationen wichtig und gilt daher als bedingt essentiell. Cystein ist normalerweise nicht essentiell, da es aus Methionin gebildet werden kann, wird aber in vielen Lehrbüchern noch als essentielle Aminosäure aufgeführt.
Aminosäuren mit unpolaren bzw. polaren Seitenketten
Aminosäuren mit unpolaren Seitenketten
Die Aminosäuren mit unpolaren Resten sind in dem Bild oben leicht grau unterlegt. Es handelt sich um die Aminosäuren Glycin, Alanin, Valin, Leucin, Isoleucin, Methionin, Phenylalanin, Tryptophan und Prolin.
Aminosäuren mit polaren neutralen Seitenketten
Diese Aminosäuren haben zwar polare Reste, die aber weder sauer noch basisch reagieren. Dazu gehören die im Bild grün hinterlegten Aminosäuren Serin, Threonin, Asparagin, Glutamin, Cystein und Tyrosin. Die Polarität der Seitenketten wird vor allem durch OH-, SH- oder Amid-Gruppen verursacht.
Aminosäuren mit polaren sauren Seitenketten ( = "saure Aminosäuren")
Asparaginsäure und Glutaminsäure (im Bild rot unterlegt) haben in der Seitenkette eine zusätzliche Carboxy-Gruppe. Diese kann ein Proton abgeben; daher liegen die Seitenketten bei physiologischem pH-Wert oft negativ geladen vor. Die zugehörigen Anionen heißen Aspartat bzw. Glutamat.
Aminosäuren mit polaren basischen Seitenketten ( = "basische Aminosäuren")
Hierzu gehören die Aminosäuren Histidin, Lysin und Arginin- im Bild blau unterlegt. Ihre Seitenketten können Protonen aufnehmen und sind daher basisch. Glutamin besitzt zwar ebenfalls eine NH2-Gruppe in der Seitenkette, diese ist jedoch Teil einer Amid-Gruppe und daher nicht basisch.
Weitere interessante Aminosäuren
Interessant sind die Aminosäuren mit aromatischen Ringsystemen in der Seitenkette: Phenylalanin, Tyrosin, Tryptophan und - mit Einschränkung - Histidin. Solche Ringsysteme beeinflussen unter anderem Lichtabsorption und Wechselwirkungen in Proteinen.
Bemerkenswert sind auch die beiden schwefelhaltigen Aminosäuren Methionin und Cystein. Cystein ist besonders wichtig, weil zwei Cystein-Reste miteinander Disulfidbrücken bilden können. Solche Bindungen stabilisieren die Raumstruktur vieler Proteine.
Ungewöhnlich ist schließlich die Aminosäure Prolin. Genau genommen besitzt Prolin keine freie primäre Amino-Gruppe, sondern eine sekundäre Amino-Gruppe, die in einen Ring eingebaut ist. Dadurch beeinflusst Prolin die Faltung von Proteinen besonders stark.
Darunter versteht man Aminosäuren, die zwar biologisch gebildet werden, aber nicht während der Translation in Proteine eingebaut werden. Inzwischen kennt man mehrere Hundert solcher Verbindungen. Auf dieser Ergänzungs-Seite wird kurz auf dieses Thema eingegangen, und einige Beispiele für nicht-proteinogene, aber biogene Aminosäuren werden vorgestellt.