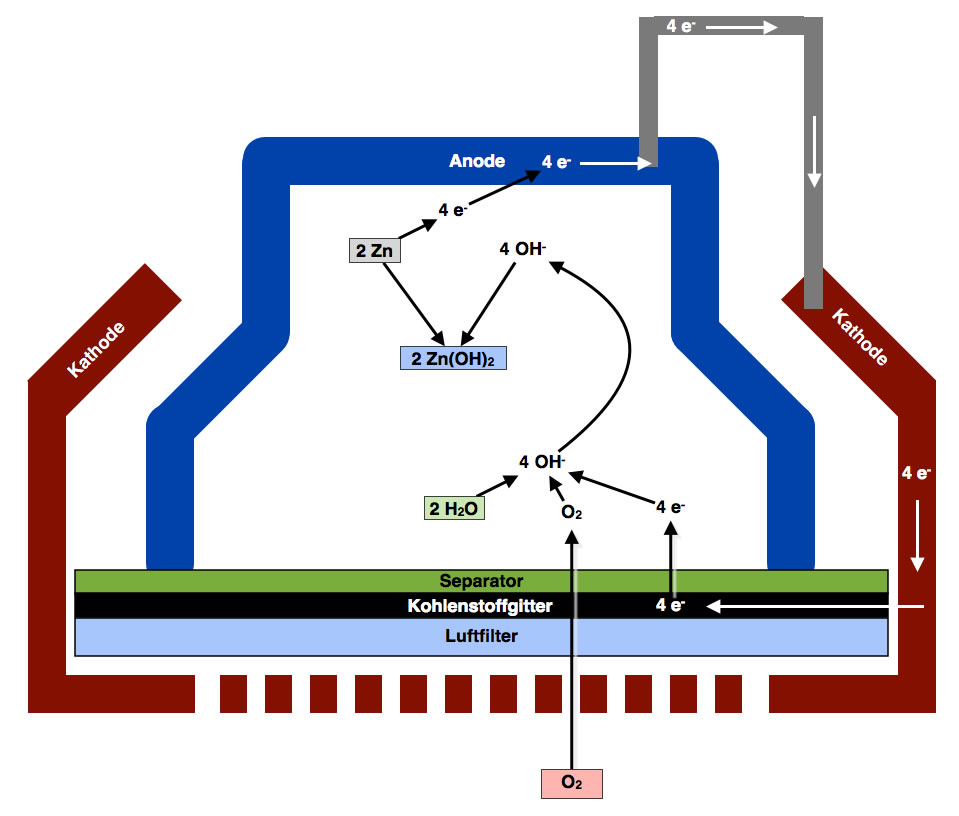
Hier sehen wir eine vereinfachte Schemazeichnung einer Zink-Luft-Batterie, wie sie auch in den meisten Schulbüchern steht.
Reaktionen an der Anode
Die Reaktionen des Minuspols, der Anode, sind zunächst recht einfach. Das Zink wird oxidiert und gibt dabei je zwei Elektronen ab:
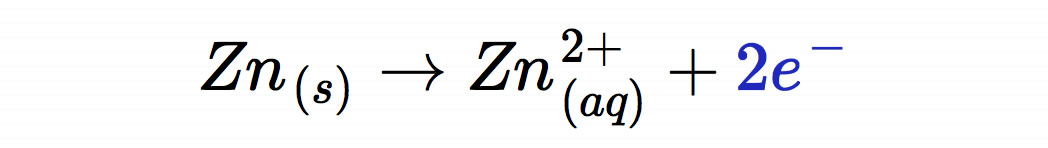
Reaktionen an der Kathode
Sauerstoff dringt durch die kleinen Poren im Boden der Batterie ein und wird dort reduziert:
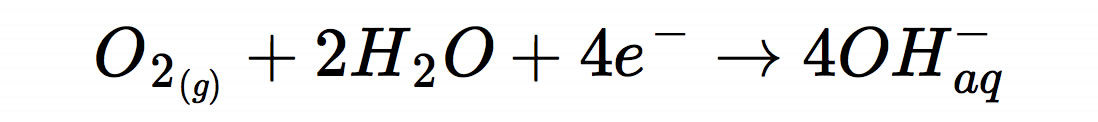
Die Hydroxid-Ionen reagieren dann mit den Zink-Ionen zu Zinkhydroxid Zn(OH)2.
Laut Wikipedia sind die Reaktionen der Zink-Luft-Batterie etwas komplexer. Ich habe das obige Schema mal entsprechend erweitert:
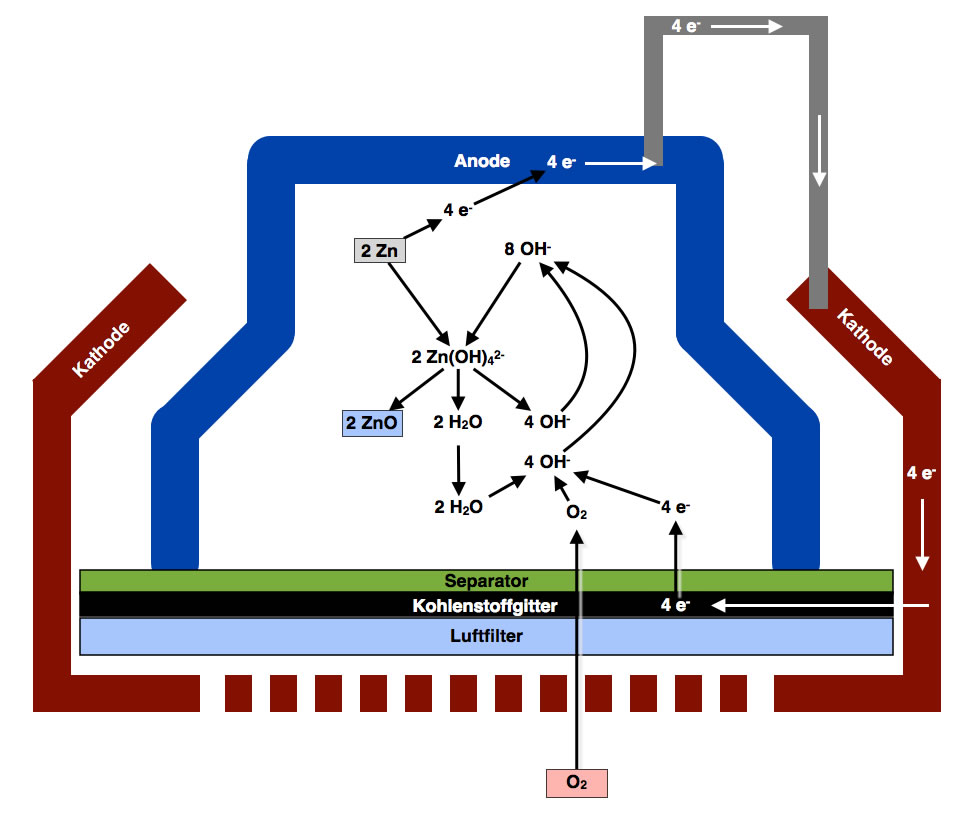
Danach entsteht nicht Zinkhydroxid als Endprodukt, sondern Zinkoxid. Im Prinzip handelt es sich aber um die gleiche Reaktion.