Lernziele
Wenn Sie diese Seite durchgearbeitet haben, sollten Sie wissen
- wie man eine Apparatur zur Erzeugung eines Gases aufbaut
- wie man aus konz. Schwefelsäure und Kochsalz Chlorwasserstoff herstellen kann.
Versuch
Nachdem Sie nun einige Säure-Base-Titrationen durchgeführt und damit wichtigen Stoff der Sekundarstufe I wiederholt haben, sollen Sie nun lernen, was der Unterschied zwischen einer Säure und einer sauren Lösung ist und welche Rolle dabei die Protonen bzw. Oxonium-Ionen spielen. Der Säure-Begriff von BRÖNSTED ist Voraussetzung für das gesamte Thema "Säuren, Basen und analytische Verfahren". In fast jeder Abituraufgabe zum Thema "Säuren und Basen" wird ein Eingehen auf das BRÖNSTED-Konzept erwartet.
Versuch 2
Herstellung und Untersuchung von Salzsäure
Material:
Geräte: 1 Erlenmeyerkolben 250ml, 1 Tropftrichter mit Druckausgleich und passendem Stopfen, 1 Winkelrohr, 1 Glastrichter, 1 Becherglas 250 ml sowie 2 Schlauchstücke. Außerdem eventuell eine Apparatur zur Messung der elektrische Leitfähigkeit in dem Becherglas.
Chemikalien: 20 ml konz. Schwefelsäure (Vorsicht, extrem ätzend!), 5 g Natriumchlorid, dest. Wasser, Universalindikator und Silbernitrat.
Durchführung:
Bauen Sie zunächst folgenden Versuch auf.
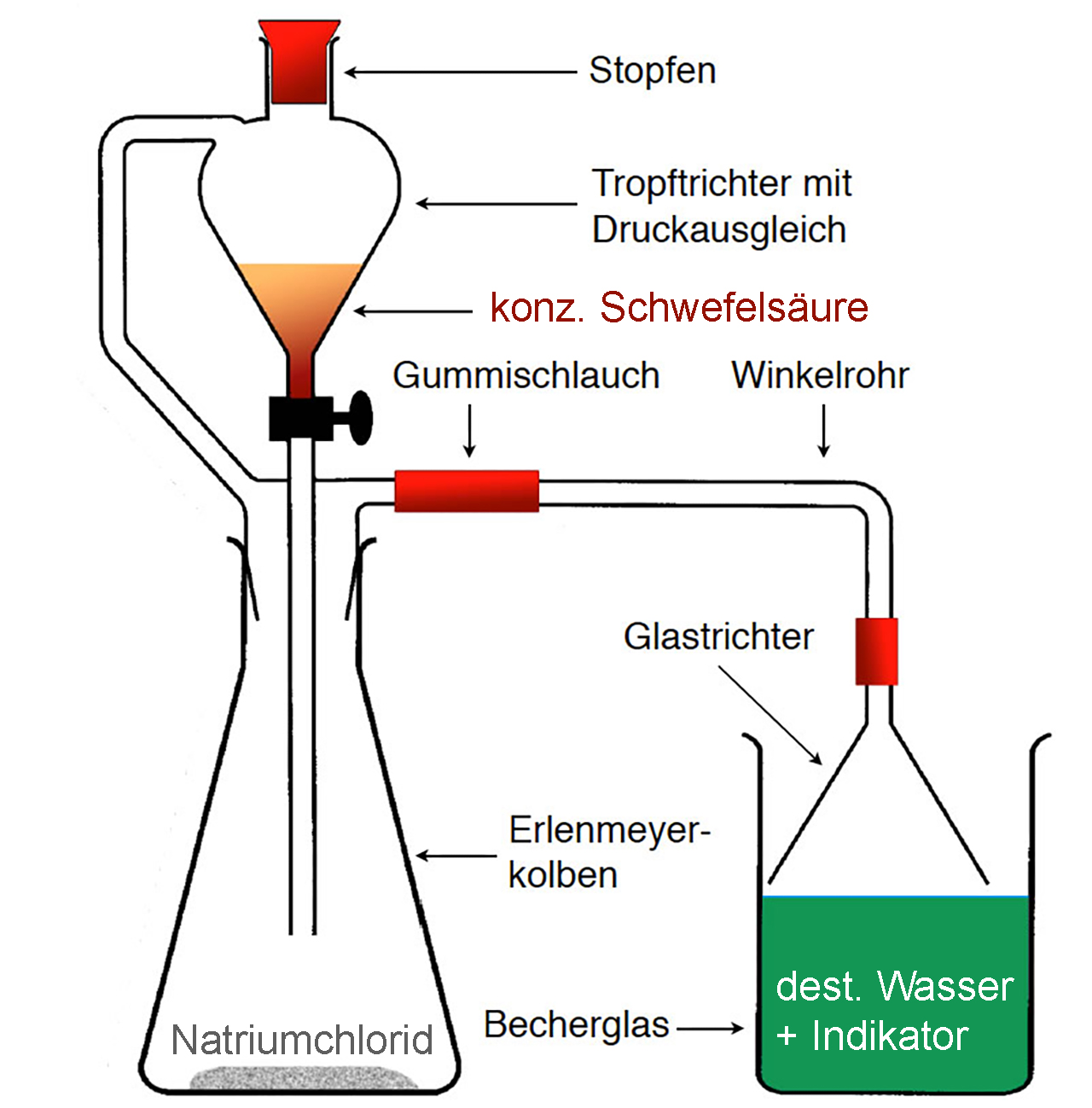
Eine einfache Version des Versuchs
Man kann den Versuch noch um eine Leitfähigkeitsmess-Apparatur ergänzen, so dass man kontinuierlich die elektrische Leitfähigkeit in dem Becherglas verfolgen kann.
Bevor Sie mit dem eigentlichen Versuch beginnen, entnehmen Sie eine kleine Probe des mit Universalindikator versetzten Wassers und geben Sie ein paar Tropfen Silbernitrat-Lösung dazu.
Nun öffnen Sie den Hahn des Tropftrichters. Die konz. Schwefelsäure H2SO4(l)tropft auf das Natriumchlorid NaCl(s), dabei entsteht gasförmiger Chlorwasserstoff HCl(g).
Dieser Chlorwasserstoff wird durch das Glasrohr und den Trichter auf das destillierte Wasser geleitet, dem etwas Universalindikator zugesetzt wurde. Außerdem wird die elektrische Leitfähigkeit des Wassers laufend überprüft. Am Ende des Versuchs wird eine weitere Probe des Wassers mit einigen Tropfen Silbernitratlösung versetzt.
Beobachtungen:
- Während der HCl-Einleitung ändert sich die Farbe des Indikators von grün über gelb und orange nach rot,
- Die elektrische Leitfähigkeit nimmt während des Versuchs deutlich zu.
- Vor dem Versuch fiel die Silbernitrat-Probe negativ aus, nach dem Versuch kann man eine deutliche Trübung erkennen.
Die Deutung des Versuchs finden Sie auf der nächsten Seite.