KI-Zusammenfassung
NAD+ und NADP+ sind wichtige Coenzyme des Stoffwechsels. Beide können bei Redoxreaktionen formal ein Hydrid-Ion aufnehmen und werden dadurch zu NADH bzw. NADPH reduziert. Der entscheidende Unterschied liegt nicht in ihrer eigentlichen chemischen Reaktivität, sondern in ihrer biologischen Verwendung: NAD+ wird vor allem in abbauenden Stoffwechselwegen eingesetzt, NADPH dagegen vor allem in aufbauenden Stoffwechselwegen.
Diese Arbeitsteilung ist für die Zelle sehr vorteilhaft. Im katabolen Stoffwechsel werden Elektronen häufig auf NAD+ übertragen, während im anabolen Stoffwechsel viele Reduktionen mit Hilfe von NADPH stattfinden. Auf diese Weise kann die Zelle zwei voneinander getrennte Redoxsysteme aufrechterhalten: eines für Oxidationen und eines für Reduktionen.
Beide Coenzyme sind Wasserstoff-Transporter
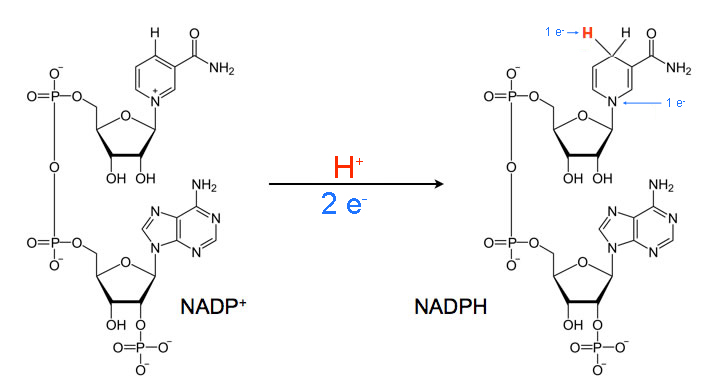
NAD+ (Nicotinamid-Adenin-Dinucleotid) und NADP+ (Nicotinamid-Adenin-Dinucleotid-Phosphat) sind Wasserstoff-Transportsysteme der Zelle, die sowohl bei anabolen (aufbauenden) als auch bei katabolen (abbauenden) Stoffwechselwegen eine wichtige Rolle spielen.
Die oxidierten Formen, also NAD+ und NADP+, können zwei Elektronen und ein Proton aufnehmen, formal also ein Hydrid-Ion H-. Dabei entstehen die reduzierten Formen NADH bzw. NADPH.
Die reduzierten Formen NADH und NADPH können diese Elektronen und das gebundene Proton wieder auf andere Moleküle übertragen. Dadurch werden diese Moleküle reduziert. Aus einer Carbonsäure kann so beispielsweise ein Aldehyd werden oder aus einem Aldehyd ein primärer Alkohol.
Was ist der Unterschied zwischen NADH und NADH/H+ ?
Die oxidierten Formen der Coenzyme, also NAD+ und NADP+, nehmen bei einer Reduktion formal zwei Elektronen und ein Proton auf. Die eigentlichen reduzierten Formen heißen daher NADH und NADPH. Warum findet man dann in vielen Schulbüchern, aber auch in der Fachliteratur und auf dieser Homepage häufig die Schreibweisen NADH/H+ bzw. NADPH/H+ ?
Das liegt daran, dass bei der Oxidation eines Substrats um zwei Stufen tatsächlich nicht nur zwei Elektronen, sondern meist auch zwei Protonen freiwerden. Schauen wir uns dazu die Oxidation eines primären Alkohols zu einem Aldehyd an:
R-CH2-OH → R-CHO + 2 H+ + 2 e-
Das Coenzym NAD+ nimmt dabei formal ein Hydrid-Ion auf, also zwei Elektronen und ein Proton. Das zweite Proton verbleibt im Cytoplasma beziehungsweise im wässrigen Milieu der Zelle. Dieses Proton ist nicht fest an das NADH gebunden. Darum ist die Schreibweise NADH/H+ im Grunde eine formale Schreibweise, mit der deutlich gemacht werden soll, dass bei der Reaktion insgesamt zwei Protonen freiwerden, von denen aber nur eines direkt an der Reduktion des Coenzyms beteiligt ist.
Bei einer späteren Reduktion eines anderen Substrats werden dann wieder zwei Elektronen und insgesamt zwei Protonen benötigt. NADH liefert die beiden Elektronen und ein Proton; das zweite Proton stammt aus dem umgebenden Medium. Deshalb findet man in Reaktionsgleichungen oft die Schreibweise NADH + H+ oder verkürzt NADH/H+.
Warum gibt es NAD+ und NADP+ ?
Wieso benötigt die Zelle eigentlich zwei verschiedene Wasserstoff-Transporter? In ihrem rein physikalisch-chemischen Verhalten unterscheiden sich die beiden Moleküle nur wenig. Die zusätzliche Phosphat-Gruppe des NADP+ ist zu weit vom Reaktionszentrum des Moleküls entfernt, um dessen chemisches Verhalten stark zu verändern. Durch diese Phosphat-Gruppe besitzt das NADP+-Molekül aber eine etwas andere Form als das NAD+-Molekül und kann daher mit anderen Enzymen zusammenarbeiten als NAD+ (Schlüssel-Schloss-Prinzip).
NAD+ arbeitet im Katabolismus
Das Coenzym NAD+ wird hauptsächlich im Katabolismus eingesetzt, also im abbauenden Stoffwechsel. Schauen wir uns dazu einmal die Glycolyse und den Citratzyklus näher an, zwei wichtige Prozesse des Glucose-Abbaus.
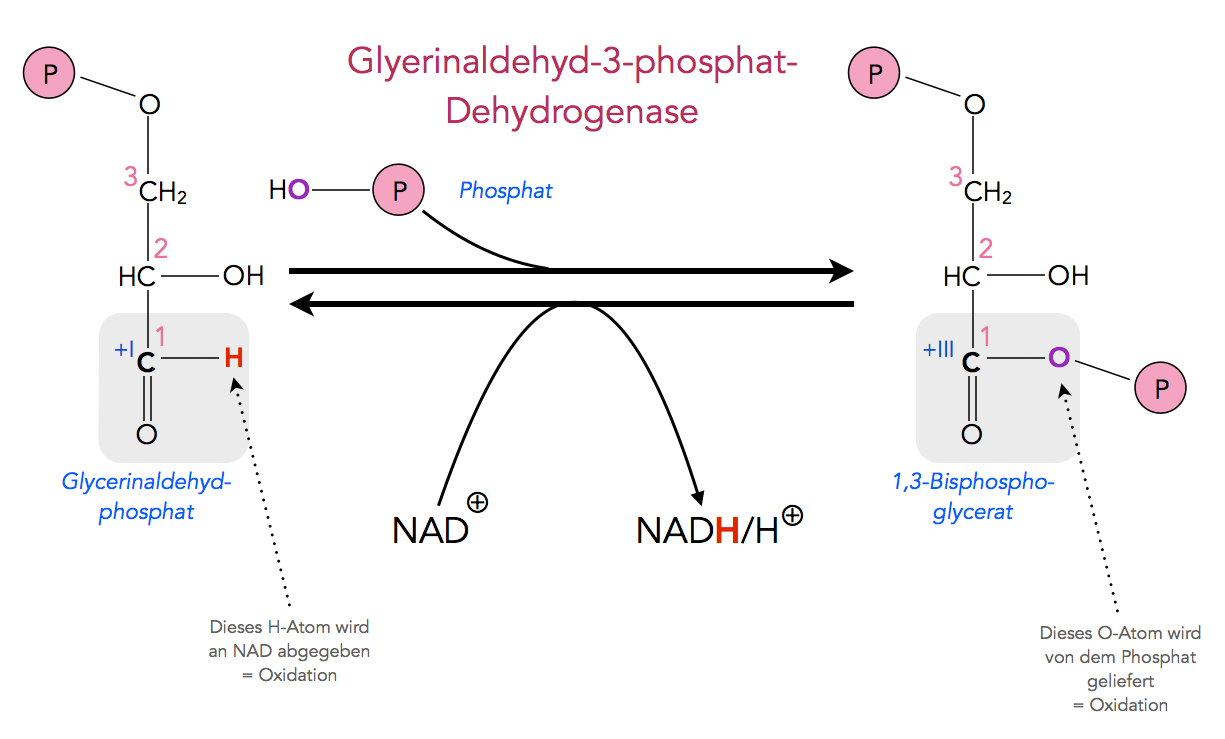
Im Schritt 5 der Glycolyse wird Glycerinaldehyd-3-phosphat zu 1,3-Bisphosphoglycerat oxidiert. Chemisch gesehen entspricht das der Oxidation eines Aldehyds. NAD+ spielt hierbei eine entscheidende Rolle als Akzeptor für zwei Elektronen und ein Proton. Das zweite Proton wird an das umgebende Medium abgegeben.
Im dritten Schritt des Citratzyklus wird Isocitrat zunächst zu Oxalsuccinat oxidiert:
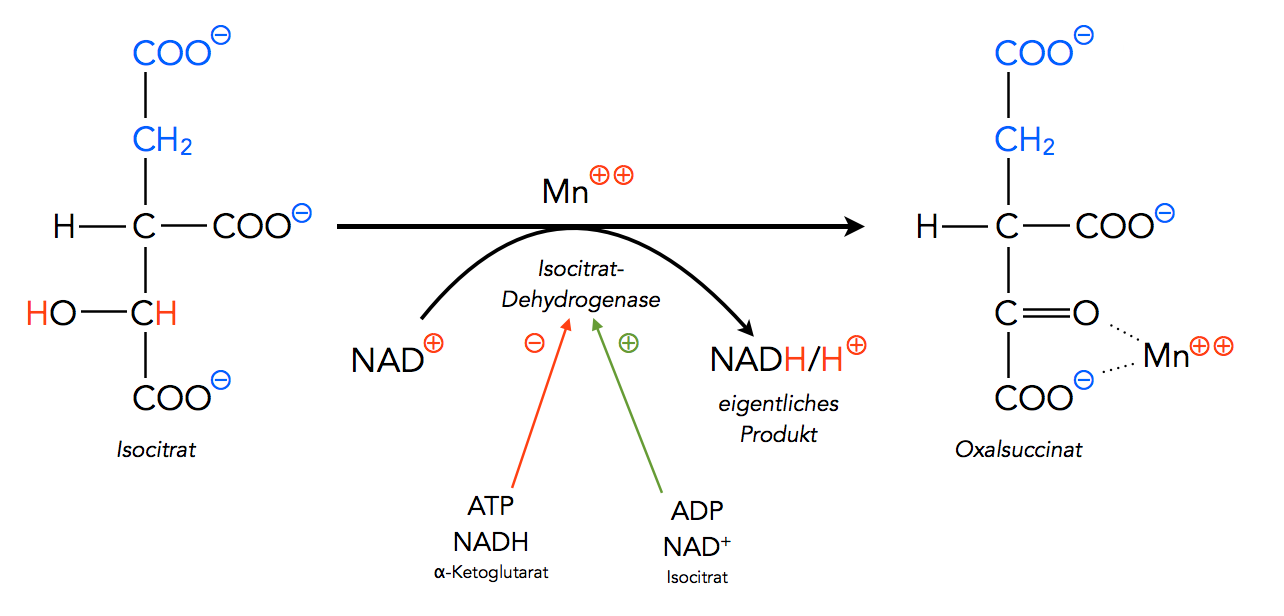
Schritt 3: Isocitrat + NAD+ ==> Oxalsuccinat + NADH/H+
Autor: Ulrich Helmich 2022, Lizenz: Public domain.
Auch hier dient NAD+ als Akzeptor für zwei Elektronen und ein Proton. Auch im Schritt 5 sowie im Schritt 9 des Citratzyklus ist NAD+ der entsprechende Elektronenakzeptor.
NADP+ arbeitet im Anabolismus
Dieses Coenzym wird hauptsächlich bei anabolen Stoffwechselvorgängen eingesetzt, also im aufbauenden Stoffwechsel. Ein wichtiges Beispiel für einen solchen anabolen Stoffwechselprozess ist die Synthese von Fettsäuren; hier wird NADPH zu NADP+ oxidiert.
Aus dem Schulunterricht kennen Sie vielleicht noch den Ablauf der Photosynthese.
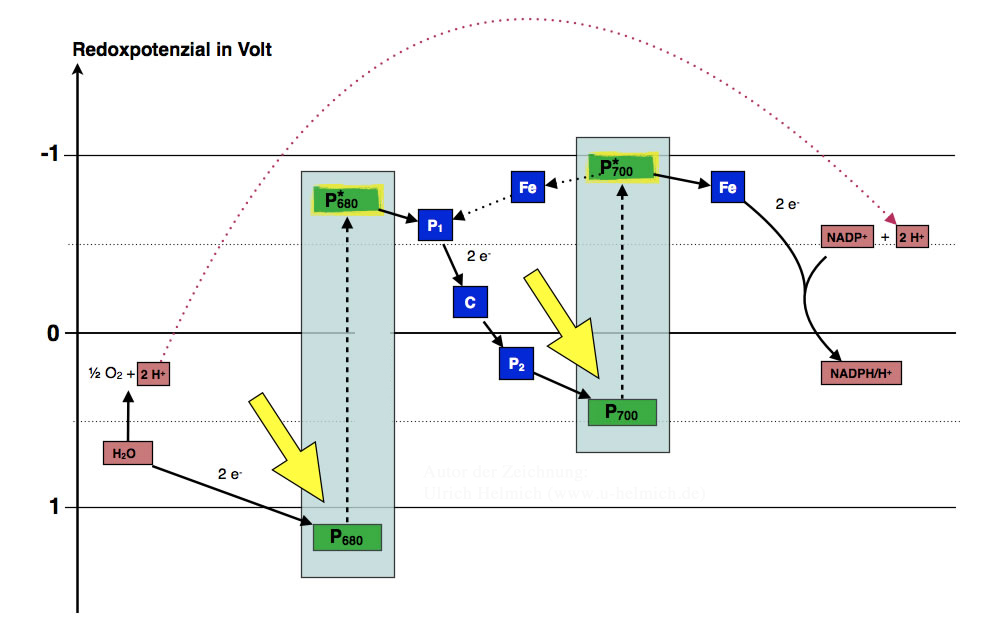
Das Zick-Zack-Schema der Lichtreaktion
Autor: Ulrich Helmich 2015, Lizenz: Public domain.
In der Lichtreaktion wird Wasser in Sauerstoff, Elektronen und Protonen zerlegt. Die Elektronen werden dann über ein ausgeklügeltes System von Enzymen und Pigmenten auf NADP+ übertragen. Die zur Reduktion von NADP+ benötigten Protonen stammen aus dem Stroma des Chloroplasten.
Vorteile dieser Arbeitsteilung
Die Bildung der reduzierten Formen NADH und NADPH erfolgt in unterschiedlichen Stoffwechselwegen. Da es zwei Formen dieses Coenzyms gibt, nämlich NAD+ und NADP+, können die Verhältnisse NAD+/NADH bzw. NADPH/NADP+ getrennt und unabhängig voneinander reguliert werden.
Innerhalb einer Zelle laufen stets anabole und katabole Prozesse nebeneinander ab. Bei anabolen Prozessen werden Substrate häufig reduziert; daher müssen viele Wasserstoff-Donatoren zur Verfügung stehen. Bei katabolen Prozessen dagegen werden viele Stoffe oxidiert; daher werden dort viele Wasserstoff-Akzeptoren benötigt.
Mit anderen Worten: In der Zelle muss für oxidative, also abbauende Vorgänge viel NAD+ zur Verfügung stehen, während für reduktive, also aufbauende Vorgänge viel NADPH benötigt wird. Mit einem einzigen Coenzym wäre das nur schwer zu leisten. Daher haben sich im Laufe der Evolution zwei unterschiedliche Coenzyme etabliert: NAD+ vor allem für den Katabolismus und NADPH vor allem für den Anabolismus.
Quellen:
- Alberts, Heald et al. Molekularbiologie der Zelle, 7. Auflage, Weinheim 2025.