Eine anerkannte Theorie zur Entstehung des Lebens geht davon aus, dass die ersten Zellen nicht in einer Art "Ursuppe" entstanden sind, sondern in Spalten und Poren feuchter Minerale oder in Hydrothermalquellen. Eisen- und Schwefelhaltige Minerale sind dafür bekannt, dass sie organische Reaktionen katalysieren, und solche Katalysereaktionen haben wahrscheinlich eine entscheidende Rolle bei der Entstehung des Lebens gespielt.
Ähnlich wie die Landtiere einen Rest des Meerwassers in Form von Blutplasma mit sich führen, finden sich heute noch in vielen wichtigen Enzymen sogenannte Eisen-Schwefel-Cluster als Überbleibsel aus der Vorzeit.
Typen von Fe-S-Clustern
Es gibt verschiedene Arten von Fe-S-Clustern. Die Häm-Eisenproteine wie Hämoglobin behören nicht dazu, diese besitzen zwar Eisen in ihren Molekülen und natürlich auch jede Menge Schwefel-Atome in den Cystein-Resten der Peptidketten, aber keine Fe-S-Cluster.
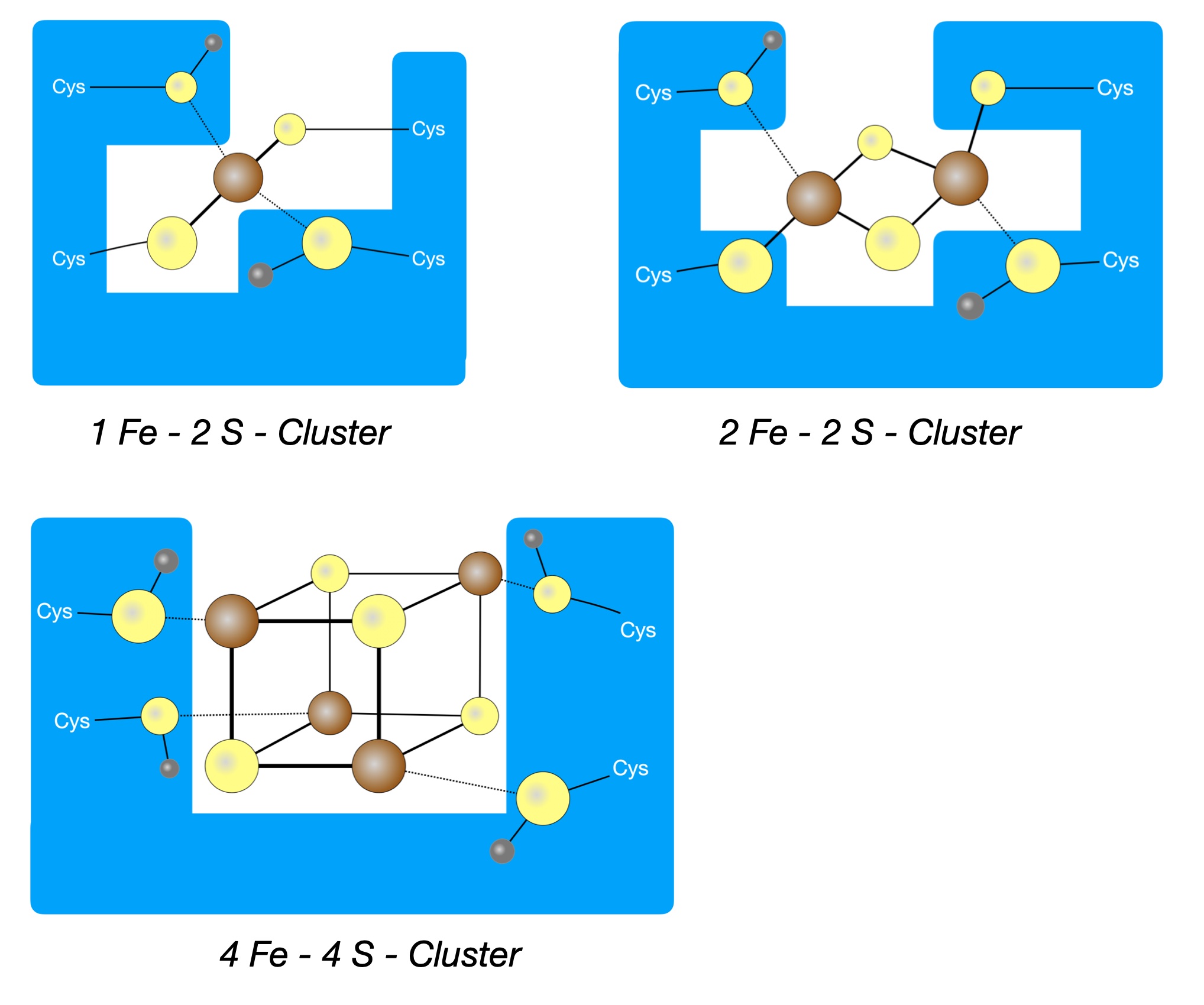
Drei Typen von Eisen-Schwefel-Clustern
Braun: Fe-Atome, gelb: S-Atome, grau: H-Atome, blau: das umgebende Protein
Autor: Ulrich Helmich 07/2024, Lizenz: Public domain
Die obigen drei Bilder sind nach Vorgaben aus [1] und [2] entstanden, sie stellen eine Kombination aus den Original-Zeichnungen dar. Wenn Sie diese Abbildung für Ihren eigenen Unterricht gebrauchen und modifizieren wollen, können Sie gern meine Original-Pages-Datei herunterladen (nur für Apple-Computer und iOS-Geräte).
1 Fe - 2 S - Cluster
Dies ist die einfachste Form von Fe-S-Clustern. Ein Eisen-Atom wird von den Schwefel-Atomen aus vier Cystein-Resten festgehalten. Zwei S-Atome binden kovalent an das Eisen-Atom, zwei andere S-Atome binden über elektrostatische Bindungen. Dieser Typ von Fe-S-Cluster kommt beispielsweise in der NADH:Q-Oxidoreduktase vor [2].
2 Fe - 2 S - Cluster
Dieser Cluster wird ebenfalls von vier Cystein-Resten zusammengehalten. Zwischen den beiden Eisen-Atomen befinden sich zwei kovalent gebundene Schwefel-Atome, die nicht an Cystein-Reste gekoppelt sind. Ein solcher 2 Fe - 2 - S - Cluster kommt zum Beispiel in verschiedenen Cytochromen vor [3].
4 Fe - 4 S - Cluster
Auch dieser komplex aufgebaute Cluster wird von vier Cystein-Resten zusammengehalten. Die vier Eisen-Atome und die vier Schwefel-Atome des eigentlichen Clusters bilden nach [1] die Ecken eines Würfels, nach [2] ist das ganze Gebildet deutlich "schiefer", also kein Würfel.
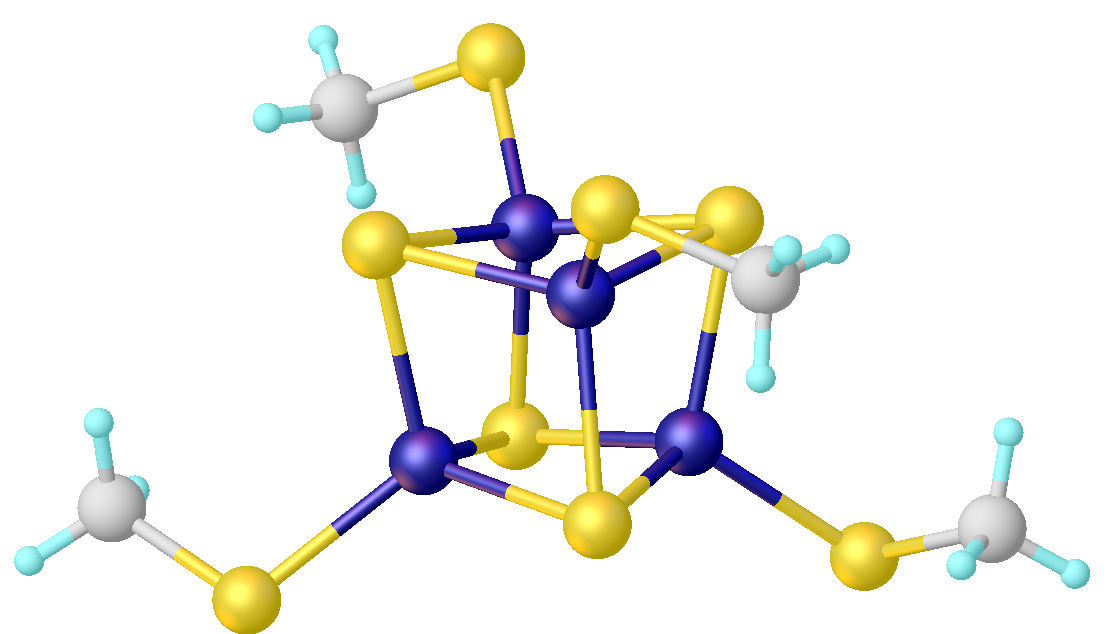
Ein 4 Fe - 4 S - Cluster
Autor: Smokefoot, Lizenz: Creative Commons Attribution-Share Alike 4.0 International license.
In der engl. Wikipedia [4] findet man dieses schöne Bild eines solchen Clusters.
Komplexere Fe-S-Cluster
Einen noch viel komplexeren Eisen-Schwefel-Cluster findet man in der Wikipedia:

Der Cofaktor der Nitrogenase
Audiophilly, Public domain, via Wikimedia Commons
Hier zählen wir sieben Eisen-Atome und neun Schwefel-Atome, und außerdem ein Stickstoff-Atom. Dieses Gebilde ist laut [3] der Cofaktor der Nitrogenase.
Eine Liste der menschlichen Proteine mit solchen Eisen-Schwefel-Clustern findet sich in dem Artikel der deutschsprachigen Wikipedia.
Funktion von Fe-S-Clustern
Ein Eisen-Ion kann als Fe2+ vorliegen oder als Fe3+. In den Fe-S-Clustern wechseln die Eisen-Atome zwischen diesen beiden Zuständen:
$Fe^{2+} \rightleftharpoons Fe^{3+} + e^{-} $
Proteine mit Fe-S-Clustern eignen sich daher gut, um Redoxreaktionen zu katalysieren, bei denen Elektronen aufgenommen oder abgegeben werden. Vor allem aber, wenn es darum geht, Elektronen von A nach B zu transportieren wie zum Beispiel bei den Elektronentransportketten der Photosynthese oder der Atmungskette, spielen Proteine mit Fe-S-Clustern eine entscheidende Rolle.
Das Fe-S-Protein nimmt beispielsweise ein Elektron von einem Elektronendonator A auf, dabei werden die Fe3+-Ionen zu Fe2+-Ionen reduziert. Im nächsten Schritt gibt das Fe-S-Protein die Elektronen an einen Elektronenakzeptor B ab, die Fe2+-Ionen des Clusters werden wieder zu Fe3+-Ionen oxidiert, während der Elektronenakzeptor B reduziert wird.
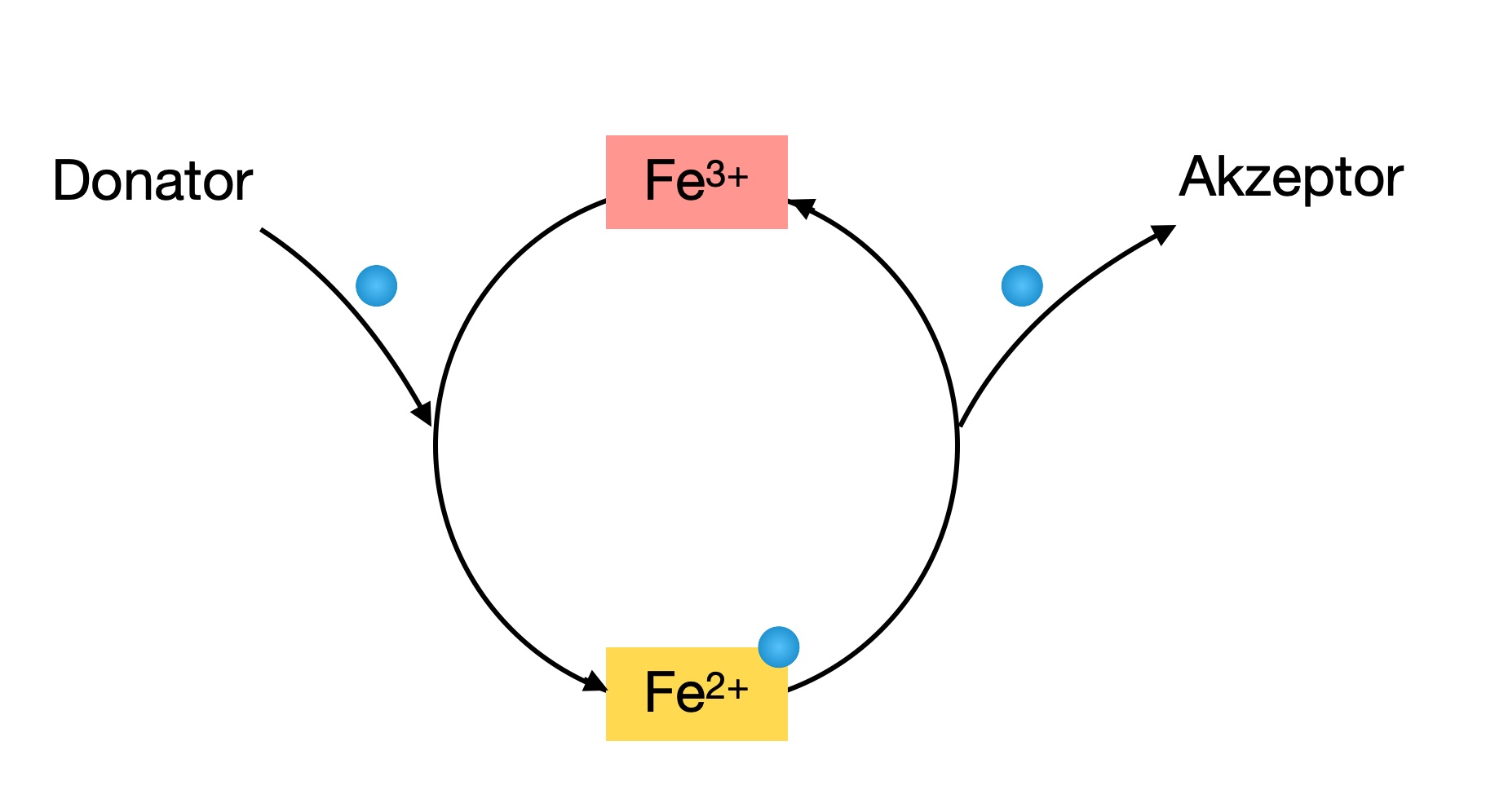
Fe-S-Cluster transportiert Elektronen von A nach B
Autor: Ulrich Helmich 07/2024, Lizenz: Public domain
Während Coenzyme wie FAD oder NAD gleichzeitig mit den Elektronen auch Protonen übertragen, werden durch die Fe-S-Cluster ausschließlich Elektronen transportiert [5].
Quellen:
- Lüttge, Faszination Pflanzen, Springer-Verlag 2017
- Berg, Tymoczko, Gatto jr., Stryer: Stryer Biochemie, 8. Auflage, Springer Berlin Heidelberg 2018.
- Wikipedia, Artikel "Eisen-Schwefel-Cluster".
- engl. Wikipedia, Artikel "Iron-sulfur cluster"
- DocCheck Flexikon, Artikel "Eisen-Schwefel-Cluster"