KI-Zusammenfassung
Unter Denaturierung versteht man die Veränderung der natürlichen Raumstruktur eines Proteins. Dabei bleiben die Aminosäure-Ketten meist erhalten, aber Sekundär-, Tertiär- oder Quartärstruktur werden gestört. Die Folge ist oft ein Verlust der biologischen Funktion, zum Beispiel bei Enzymen.
Ausgelöst werden kann eine Denaturierung unter anderem durch Hitze, Säuren, Laugen, Alkohol, Salze oder Schwermetall-Ionen. Diese Stoffe oder Bedingungen zerstören wichtige Wechselwirkungen im Protein, etwa Wasserstoffbrücken, Ionenbindungen oder hydrophobe Wechselwirkungen. Häufig entfalten sich die Proteinmoleküle dabei und lagern sich anschließend zu größeren Aggregaten zusammen.
Im Alltag kann man Denaturierung an vielen Beispielen beobachten: Ein Ei wird beim Kochen fest, Milch flockt bei Zugabe von Säure aus, und beim Desinfizieren werden Proteine von Mikroorganismen geschädigt. Die Denaturierung ist also ein biologisch und praktisch sehr wichtiges Phänomen.
Inhalt dieser Seite
Versuch zur Denaturierung von Proteinen
Material:
2 Tassen, 7 Reagenzgläser, Reagenzglasständer, Messzylinder (100 ml), 5 Tropfpipetten, Wasserbad.
Ein Hühnerei, Salzsäure (verdünnt), Kupfersulfatlösung (5 %), Ethanol, Natronlauge (verdünnt), Ammoniumsulfatlösung (gesättigt), dest. Wasser.
Durchführung:
Stellen Sie zunächst eine Eiweißlösung her:
- Ei aufschlagen,
- in einer Tasse Eigelb und Eiklar trennen,
- das Eiklar in der anderen Tasse mit 100 ml dest. Wasser versetzen und gut vermischen,
- die Eiklar-Lösung auf sieben Reagenzgläser verteilen und die Gläser jeweils etwa zu einem Viertel bis Drittel füllen.
Führen Sie dann folgende Teilversuche mit den sieben Reagenzgläsern durch:
- ein Reagenzglas in ein heißes Wasserbad stellen,
- ein Reagenzglas mit etwas Salzsäure versetzen,
- ein Reagenzglas mit etwas Kupfersulfatlösung versetzen,
- ein Reagenzglas mit etwas Natronlauge versetzen,
- ein Reagenzglas mit etwas Ethanol versetzen,
- ein Reagenzglas mit gesättigter Ammoniumsulfatlösung versetzen,
- ein Reagenzglas mit dest. Wasser versetzen (Kontrollversuch).
Beobachten Sie genau, in welchem Reagenzglas eine Denaturierung stattfindet und wie sie sich äußert. Dokumentieren Sie Ihre Versuchsergebnisse.
Denaturierung ↑
Bei der Denaturierung eines Proteins verändert sich dessen räumliche Struktur. Betroffen sind vor allem die Tertiärstruktur und gegebenenfalls auch die Sekundärstruktur; bei Proteinen mit mehreren Untereinheiten kann auch die Quartärstruktur verändert werden. Die Primärstruktur bleibt dabei in der Regel erhalten, die Reihenfolge der Aminosäuren wird also meist nicht verändert.
Wenn sich die räumliche Struktur eines Proteins stark verändert, geht oft auch seine biologische Funktion verloren. Ein Enzym beispielsweise verliert dann seine enzymatische Aktivität, weil sich auch die Form seines aktiven Zentrums ändern kann.
1. Denaturierung durch Hitze ↑
Bei der Hitzedenaturierung werden vor allem die schwachen Wechselwirkungen gestört, die ein Protein stabilisieren, also zum Beispiel Wasserstoffbrücken, Ionenbindungen, hydrophobe Wechselwirkungen und van-der-Waals-Kräfte. Durch die Zufuhr thermischer Energie nehmen die Bewegungen der Atome und Moleküle zu; dadurch wird die gefaltete Struktur instabiler. Die kovalenten Peptidbindungen werden dabei normalerweise nicht aufgebrochen, die kovalenten Disulfidbrücken innerhalb eines Proteins dagegen können durch starke Hitze gespalten werden. Hitzedenaturierungen sind manchmal reversibel, oft aber irreversibel.
1.1 Fieber
Lebewesen werden durch starke Hitze geschädigt. Auch ein Anstieg der Körpertemperatur kann biologische Prozesse beeinflussen. Fieber dient aber nicht dazu, die Proteine von Krankheitserregern einfach "wegzudenaturieren", sondern ist Teil der Immunabwehr: Viele Abwehrreaktionen laufen bei erhöhter Temperatur schneller oder wirksamer ab, und manche Erreger vermehren sich dann schlechter. Sehr hohes Fieber ist allerdings gefährlich, weil dann lebenswichtige Vorgänge im Körper gestört werden können. Auch die Proteine des Körpers können bei Temperaturen über 40 ºC zunehmend geschädigt werden. Darum sollte man bei hohem Fieber Gegenmaßnahmen ergreifen (fiebersenkende Medikamente, Wadenwickel etc.).
1.2 Disulfid-Brücken
Disulfid-Brücken tragen bei vielen Proteinen zusätzlich zur Stabilisierung der Tertiärstruktur bei. Durch bloßes Erhitzen werden sie normalerweise nicht gespalten; meist werden zunächst die schwächeren nichtkovalenten Wechselwirkungen gestört. Trotzdem kann ein stark erhitztes Protein seine ursprüngliche Form dauerhaft verlieren. Ein einmal gekochtes Hühnerei kann daher nicht mehr in den ursprünglichen flüssigen Zustand zurückversetzt werden.
1.3 Sterilisieren
Anwendungen findet die Hitzedenaturierung zum Beispiel beim Autoklavieren, also beim Sterilisieren medizinischer Geräte mit heißem Wasserdampf unter erhöhtem Druck.
1.4 Enzyme haben ein Temperaturoptimum
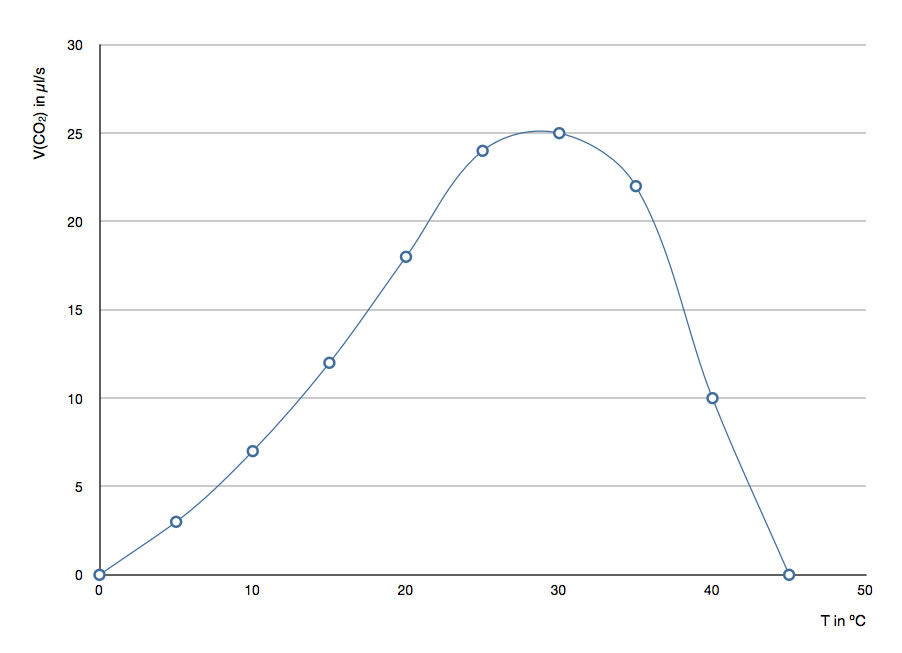
Temperaturabhängigkeit der Aktivität eines Enzyms
Autor: Ulrich Helmich 2021, Lizenz: CC BY-NC-SA 4.0
In der Abbildung sehen wir, wie die Aktivität eines Enzyms von der Temperatur abhängt. Es handelt sich um eine typische Optimumskurve: Bei einer Temperatur von 30 ºC arbeitet unser Beispielenzym am besten. Bei niedrigeren Temperaturen setzt das Enzym seine Substrate langsamer um.
Bis zu einem gewissen Punkt nimmt die Reaktionsgeschwindigkeit mit steigender Temperatur zu. Dies entspricht der RGT-Regel (Reaktionsgeschwindigkeits-Temperatur-Regel), nach der viele biochemische Reaktionen bei einer Temperaturerhöhung um 10 ºC etwa zwei- bis dreimal so schnell ablaufen.
Eigentlich müsste das Enzym bei 40 ºC doppelt bis dreimal so schnell arbeiten wie bei 30 ºC. Das ist aber nicht der Fall, im Gegenteil, die Enzymaktivität sinkt rapide. Die RGT-Regel gilt nämlich nur in einem begrenzten Temperaturbereich. Wird dieser Bereich überschritten (in unserem Beispiel ca. 30 ºC), beginnt das Enzym zu denaturieren, und seine Aktivität sinkt wieder.
Die Tertiärstruktur verändert sich dann, und das wirkt sich auch auf das aktive Zentrum des Enzyms aus, das ja für die Bindung und Umsetzung des Substrats verantwortlich ist. Das Schlüssel-Schloss-Prinzip funktioniert nicht mehr: Wenn das Schloss verformt ist, passt der Schlüssel nicht mehr hinein.
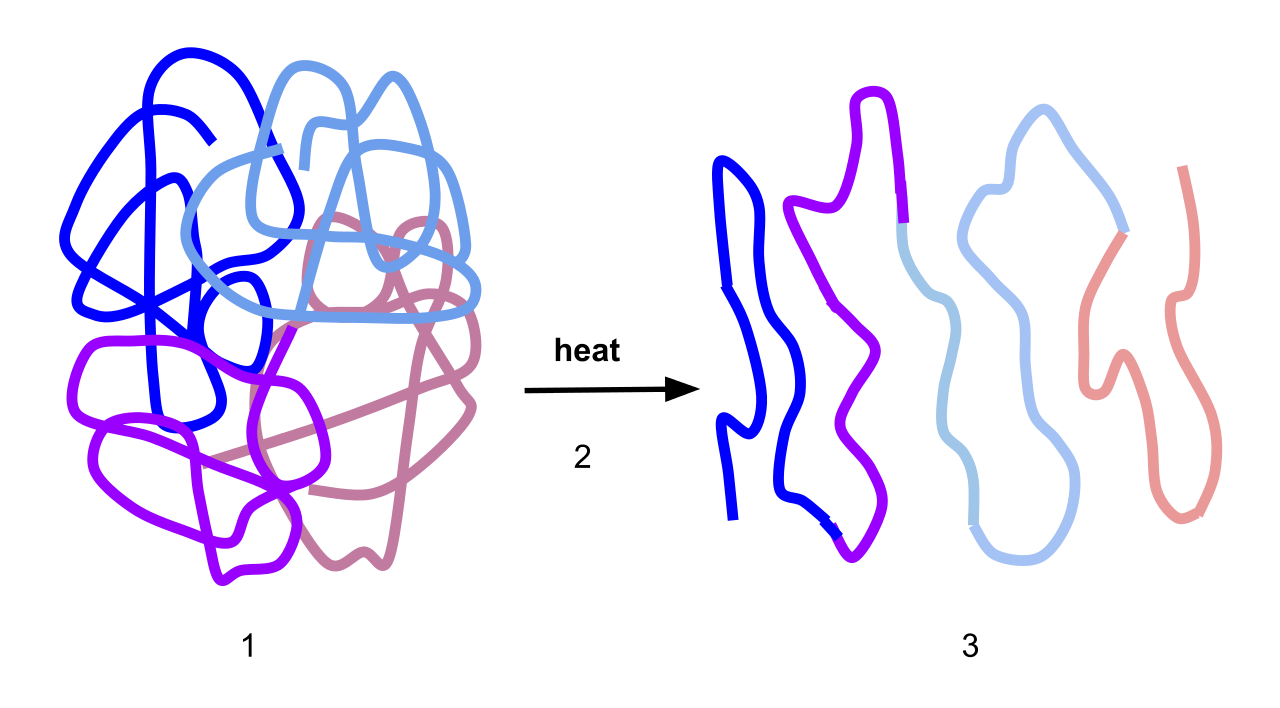
Entfaltung eines Proteins durch Hitze
Scurran15, CC BY-SA 4.0, via Wikimedia Commons
Auf diesem Bild ist sehr schön dargestellt, wie sich ein globuläres Protein unter Hitzeeinwirkung entfaltet.
2. Denaturierung durch Säuren und Laugen ↑
2.1 Säuren
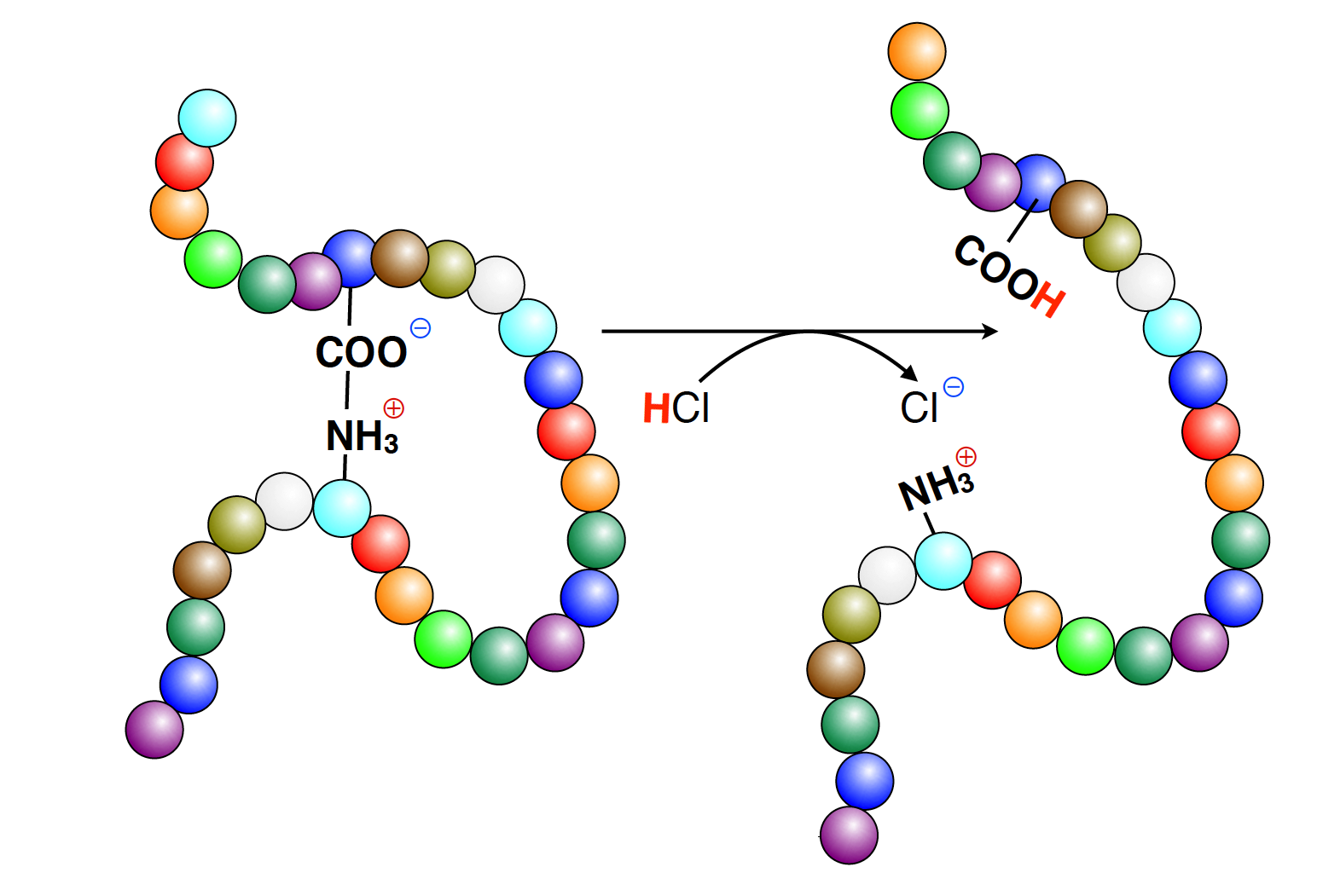
Veränderung der Tertiärstruktur durch Zugabe einer Säure
Autor: Ulrich Helmich, Lizenz: Public domain
Säuren wie beispielsweise HCl (Salzsäure) geben Protonen H+ ab, die sich dann an negativ geladene Carboxylat-Gruppen in den Seitenketten saurer Aminosäuren anlagern können:
$R\mbox{-}COO^{-} + H^{+} \to R\mbox{-}COOH$
Diese Seitenketten verlieren dann ihre negative Ladung. Dadurch werden Ionenbindungen gestört, die zur Stabilisierung der Tertiärstruktur beitragen.
In der Abbildung oben wird aus der negativ geladenen COO--Gruppe eine neutrale COOH-Gruppe. Damit verlieft die NH3+-Gruppe in der Seitenkette der einen Aminosäure ihren Bindungspartner.
2.2 Laugen
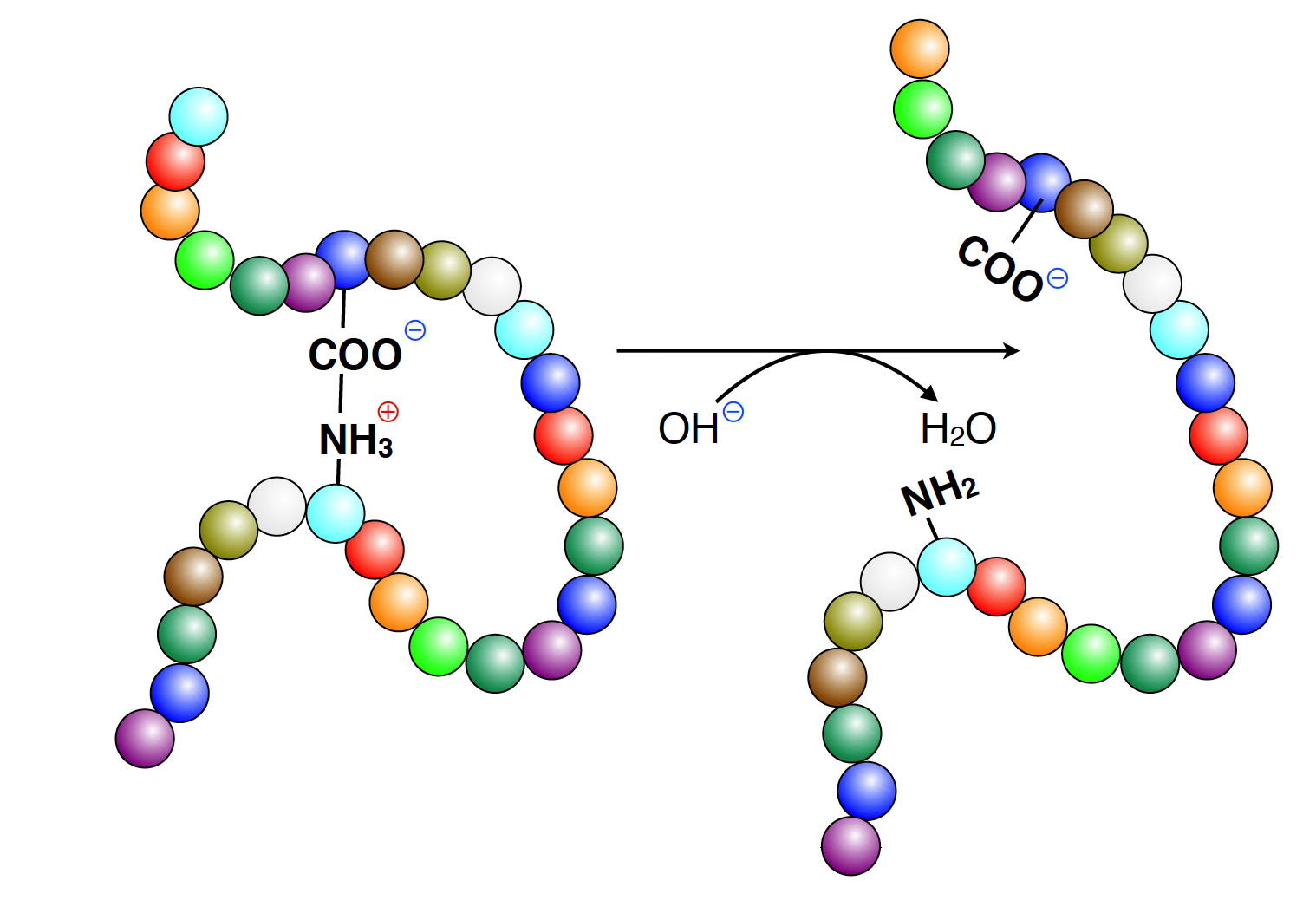
Veränderung der Tertiärstruktur durch Zugabe einer Lauge
Autor: Ulrich Helmich, Lizenz: Public domain
Laugen enthalten Hydroxid-Ionen OH-, die Protonen aus positiv geladenen NH3+-Gruppen aufnehmen können, wie sie in den Seitenketten basischer Aminosäuren vorkommen:
$R\mbox{-}NH_3^{+} + OH^{-} \to R\mbox{-}NH_2 + H_2O$
Dadurch verlieren die Seitenketten von basischen Aminosäuren wie Lysin oder Arginin ihre positive Ladung. Auch hierdurch werden Ionenbindungen und damit die Tertiärstruktur des Proteins gestört.
Außerdem können starke pH-Änderungen auch Wasserstoffbrücken beeinflussen, die zur Stabilisierung von Sekundärstrukturen wie alpha-Helix und beta-Faltblatt beitragen.
2.3 Hydrolyse schädigt die Primärstruktur
Bei einem starken Überschuss an Säure oder Lauge und längerer Einwirkungszeit kann es sogar zur Hydrolyse von Peptidbindungen kommen. Dann wird nicht nur die räumliche Struktur verändert, sondern das Proteinmolekül selbst chemisch gespalten; die Primärstruktur wird also zerstört.
2.4 Enzyme haben ein pH-Optimum
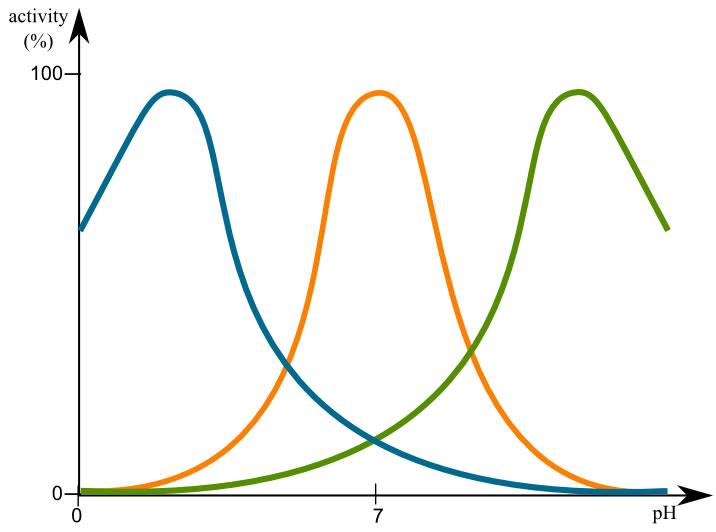
pH-Abhängigkeit der Enzymaktivität von drei unterschiedlichen Enzymen
Gal m, CC BY 3.0, via Wikimedia Commons
Auf diesem Bild sieht man drei verschiedene Enzyme und wie ihre Aktivität vom pH-Wert abhängt. Das blau gezeichnete Enzym hat beispielsweise eine optimale Aktivität bei einem pH-Wert von etwa 2 bis 3, das orange gezeichnete Enzym hat sein pH-Optimum bei pH 6 bis 8, und das grün gezeichnete Enzym hat sein pH-Optimum im stark alkalischen Bereich, also ungefähr bei pH 10 bis 11.
Die Enzyme unseres Verdauungssystems unterscheiden sich ebenfalls in ihrer pH-Abhängigkeit. Das Pepsin des Magens muss zum Beispiel bei stark sauren pH-Werten optimal arbeiten. Im Dünndarm dagegen herrscht ein leicht alkalisches Milieu. Trypsin und Chymotrypsin arbeiten daher bei höheren pH-Werten gut. Pepsin, das mit dem Nahrungsbrei in den Dünndarm gelangt, wird dort rasch inaktiv.
3. Denaturierung durch weitere Faktoren ↑
Salze bestehen aus positiv und negativ geladenen Ionen. Bei hohen Salzkonzentrationen können diese Ionen die Hydrathülle der Proteine und ihre ionischen Wechselwirkungen verändern. Dadurch verlieren viele Proteine ihre Löslichkeit und flocken aus. Ein bekanntes Beispiel ist das Aussalzen von Proteinen mit Ammoniumsulfat.
Für Experten: Aussalzen mit Ammoniumsulfat
Beim Aussalzen mit Ammoniumsulfat passiert im Wesentlichen Folgendes: In Wasser gelöste Proteine sind von einer Hydrathülle aus Wassermolekülen umgeben. Gibt man viel Ammoniumsulfat hinzu, dann binden die Sulfat- und Ammonium-Ionen sehr viele Wassermoleküle an sich. Für die Proteine bleibt dadurch weniger frei verfügbares Wasser übrig, das ihre Hydrathülle stabilisiert.
Zusätzlich führt die hohe Salzkonzentration dazu, dass Ladungen an der Proteinoberfläche stärker abgeschirmt werden. Die Proteine stoßen sich also gegenseitig weniger ab und können sich leichter annähern. Dadurch werden hydrophobe Wechselwirkungen zwischen Proteinmolekülen begünstigt. Die Folge ist, dass die Proteine aggregieren und schließlich ausfallen.
Die Primärstruktur der Proteine wird dadurch nicht verändert. Entfernt man das Salz wieder vorsichtig, können manche Proteine sich erneut lösen und dabei sogar ihre Funktion wiedererlangen. In der Biochemie nutzt man das Verfahren des Aussalzens daher oft zur Reinigung von Proteinen.
3.1 Denaturierung durch Schwermetalle
Metall-Ionen wie Cu2+, Pb2+, Hg2+ oder Cd2+ können an bestimmte Gruppen von Aminosäure-Seitenketten binden, vor allem an Schwefel-haltige Gruppen von Cystein. Außerdem können die positiv geladenen Metall-Ionen mit den negativ geladenen Carboxy-Gruppen in den Seitenketten Komplexe bilden.
Dadurch wird die normale Raumstruktur des Proteins stark gestört. Diese Art der Denaturierung ist oft irreversibel.
3.2 Denaturierung durch Tenside
Auch Tenside aus Wasch- oder Spülmitteln können Proteine denaturieren. Sie wechselwirken sowohl mit hydrophoben als auch mit hydrophilen Bereichen des Proteins und stören dadurch die stabilisierenden Wechselwirkungen in der Raumstruktur.
3.3 Denaturierung durch Ethanol und andere organische Lösungsmittel
Ethanol und andere organische Lösungsmittel beeinflussen vor allem Wasserstoffbrücken und hydrophobe Wechselwirkungen, welche die Sekundär- und Tertiärstruktur stabilisieren. Diese Art der Denaturierung wird beim Desinfizieren genutzt.
3.4 Denaturierung durch destilliertes Wasser
Natürlich vorkommende Proteine liegen nie isoliert vor, sondern sind mit Salzen und organischen Molekülen assoziiert, die teilweise auch für den Erhalt der Tertiärstruktur verantwortlich sind. Entfernt man diese Komponenten durch Dialyse, kann die Raumstruktur oft nicht mehr aufrecht erhalten werden, es kann dann ebenfalls zu einer Denaturierung kommen.
3.5 Denaturierung durch Luftsauerstoff
Sauerstoff kann Schwefel-haltige Gruppen in Proteinen oxidativ verändern. Besonders betroffen sind dabei Cystein-Reste. Unter milden Bedingungen entstehen dabei eher Disulfid-Brücken; bei stärkerer Oxidation sind auch weitergehende Oxidationsprodukte wie Sulfon-Gruppen möglich. Solche Reaktionen können die Struktur und Funktion eines Proteins verändern.
- Unter milden Bedingungen:
Cystein-SH + HS-Cystein → Cystein-S-S-Cystein (Disulfidbrücke) - Unter stärkeren Bedingungen:
Cystein-SH → Cystein-SO3H (Sulfon-Gruppe).
4. Erklärung des Ausflockens von Milch
Gibt man genügend Essig in einen Topf mit Milch, so flockt diese aus. Die Säure verändert die Ladungsverhältnisse der Milchproteine und damit auch ihre Wasserlöslichkeit.
Im Innern eines gefalteten Proteins befinden sich oft viele hydrophobe Aminosäure-Seitenketten. In einem polaren Lösungsmittel wie Wasser ist es energetisch ungünstig, wenn sich solche hydrophoben Gruppen an der Oberfläche befinden.
Durch das Entfalten des Proteins gelangen diese hydrophoben Seitenketten nun in Kontakt mit Wasser. Dadurch wird die Löslichkeit des Proteins weiter herabgesetzt.
Hinzu kommt ein zweiter Effekt: Der Kontakt hydrophober Seitenketten mit Wasser ist energetisch ungünstig. Die entfalteten Proteinketten lagern sich deshalb neu zusammen, und zwar so, dass ihre hydrophoben Bereiche möglichst wenig Kontakt mit Wasser haben. So entstehen immer größere Aggregate aus Proteinketten, die man schließlich mit bloßem Auge als Flocken erkennen kann.
Solche Prozesse spielen auch eine wichtige Rolle, wenn man ein Ei kocht, ein Spiegelei zubereitet oder Brot und Kuchen backt.
Quellen:
- Wikipedia: Denaturierung
- Hilka de Groot, Ernährungswissenschaft, Haan-Gruiten 2011
- Chemieunterricht.de: Zu den Mechanismen der Proteinfällung
- Chemie-schule.de: Denaturierung