Natrium, das Element mit der Ordnungszahl 11, wurde 1807 von Davy durch Schmelzflusselektrolyse gewonnen.
Natrium ist ein leichtes Metall. Es hat eine Dichte von 0,97 g/cm3 und schwimmt daher gerade noch auf dem Wasser. Außerdem ist Natrium ein sehr weiches Metall, man kann es mit dem Messer schneiden, es ist weicher als Lithium. Natrium schmilzt bereits bei 98 ºC, also wesentlich eher als Lithium, und die Siedetemperatur beträgt 890 ºC, ist also ebenfalls niedriger als bei Lithium. Im Vergleich zu anderen Metallen ist Natrium sehr reaktiv. An der Luft läuft es innerhalb weniger Minuten trüb an, und mit Wasser reagiert Natrium heftig unter Bildung von Wasserstoff.
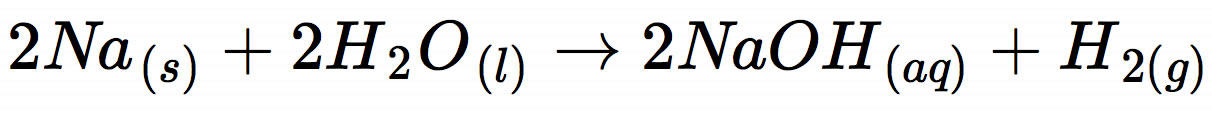
Aufgrund seiner Eigenschaften könnte man annehmen, dass Natrium gar kein "richtiges" Metall ist. Das Element Natrium weist aber dennoch alle Eigenschaften eines typischen Metalls auf. Wenn man ein Stück Natrium durchschneidet, glänzt die Schnittfläche metallisch. Außerdem leitet Natrium den Strom recht gut und ist auch ein guter Wärmeleiter. Schließlich geht Natrium chemische Reaktionen mit Nichtmetallen ein, die für viele Metalle typisch sind.
Wegen seiner hohen Reaktivität kommt Natrium in der freien Natur nicht in elementarer Form vor, sondern nur in Form von Natriumsalzen wie Natriumchlorid oder Natriumcarbonat. Diese Salze werden wie auch das Element vielfältig eingesetzt; alle Anwendungen hier aufzuzählen, würden den Rahmen sprengen.
Anwendungen von Natrium
- Flüssiges Natrium wird wegen seiner hohen Wärmeleitfähigkeit und wegen seines geringen Schmelzpunktes als Kühlmittel in Flugzeugmotoren und Kernkraftwerken verwendet.
- In den Natriumdampflampen, die man oft an Straßenkreuzungen, Fußgängerüberwegen oder anderen Gefahrenstellen sieht, befindet sich metallisches Natrium. Wenn die Lampe leuchtet, verdampft das Natrium und strahlt gelbes Licht aus, das aufgrund seiner Wellenlänge auch Nebel, Regen oder Dunst durchdringt.
- In der Natrium/Schwefel-Batterie wird ebenfalls metallisches Natrium eingesetzt. Diese Batterie - eigentlich ein Akkumulator - liefert viermal so viel Energie wie ein Bleiakku, der immer noch in den meisten Fahrzeugen eingesetzt wird.
- Bei der Herstellung von Titan und anderen Metallen wird elementares Natrium als Reduktionsmittel eingesetzt.
- Wegen seiner Reaktion mit Wasser zu festem NaOH und gasförmigem Wasserstoff kann man Natrium im Labor als Trocknungsmittel einsetzen. Allerdings nur für Stoffe, die nicht selbst mit Natrium reagieren. 96%igen Ethanol könnte man beispielsweise nicht mit Natrium trocknen, da Ethanol wegen seiner OH-Gruppe mit Natrium reagiert.