N- und O-Glycoside
Schauen wir uns zunächst einmal die Defintion des Begriffs "Glycosid" an. Im DocCheck Flexikon wird dieser Begriff recht prägnant definiert:
"Als Glykoside bezeichnet man natürliche oder künstliche Verbindungen, die durch die Kondensationsreaktion zwischen der Halbacetal-Gruppe eines ringförmigen Zuckers und der Hydroxy-, Amino- oder Sulfhydrylgruppe eines anderen Moleküls (gegebenenfalls eines zweiten Zuckers) entstanden sind."
Wir wollen diese kompakte Definition nun etwas näher auseinandernehmen. Was ist beispielsweise die Halbacetal-Gruppe eines ringförmigen Zuckers?
Halbacetalgruppe eines ringförmigen Zuckers
Schauen wir uns dazu einmal den "Standardzucker" an, die Glucose:
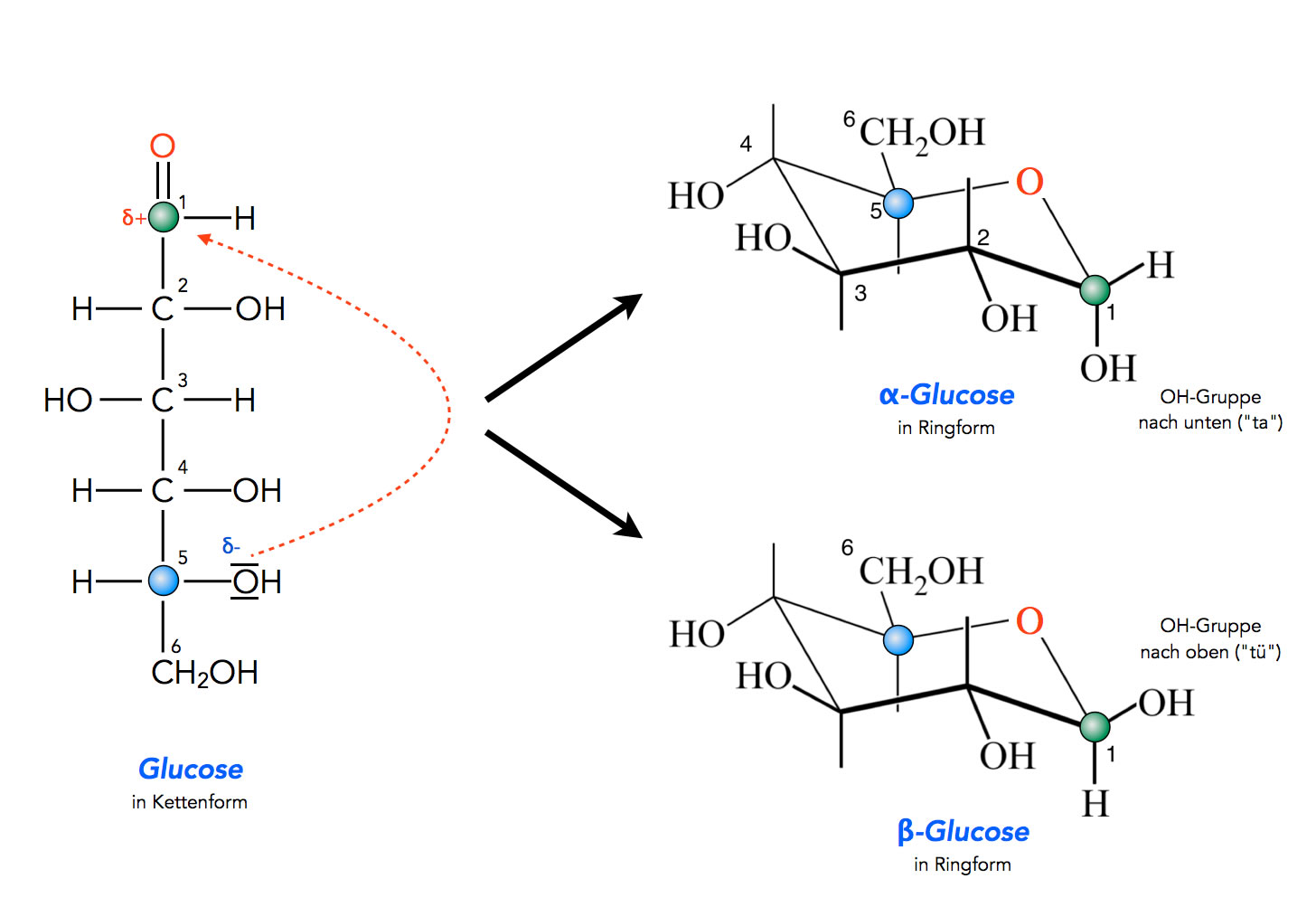
Ringbildung bei der Glucose
Autor: Ulrich Helmich, Lizenz: Public domain.
Glucose kommt bekanntlich sowohl in der Kettenform wie in der Ringform vor. In einer wässrigen Lösung überwiegt aber die Ringform deutlich. Bei der Ringbildung reagiert die OH-Gruppe am 5. C-Atom der Glucose-Kette mit der C=O-Gruppe an Position 1. Chemisch gesehen handelt es sich bei dieser Reaktion um eine nucleophile Addition, genauer um eine Halbacetal-Bildung. Auf der Seite über Monosaccharide wird näher auf diese Reaktion eingegangen.
Diese Seite aus dem regulären Chemiekurs behandelt die Addition von Alkoholen an Aldehyde und Ketone und somit die Bildung von Halbacetalen.
Auf dieser Seite wird auf die Stereochemie der Monosaccharide ausführlich eingegangen, auch auf die Chemie der Ringbildung.
Durch die Ringbildung können zwei verschiedene Glucose-Ringe entstehen. Bei der α-Glucose "schaut" die OH-Gruppe am C1-Atom nach "unten", während sie bei der β-Glucose nach "oben" gerichtet ist.
Interessant in dem Zusammenhang mit Aminosäuren und Proteinen ist aber die OH-Gruppe am C1-Atom aus einem anderen Grund: Sie kann nämlich Verbindung mit anderen Molekülen aufnehmen. Bei der Bildung von Di- und Polysacchariden beispielsweise kondensiert diese OH-Gruppe mit einer OH-Gruppe eines anderen Monosaccharid-Moleküls. Bei der Bildung von Glycosiden dagegen reagiert diese OH-Gruppe mit - und jetzt kommen wir wieder auf die Definition zurück - "einer Hydroxy-, Amino- oder Sulfhydrylgruppe eines anderen Moleküls".
In der Natur kommen viele Glycoside vor. Wir wollen uns hier einmal den Wirkstoff des Roten Fingerhuts näher anschauen, ein Herzglykosid. In der Wikipedia finden wir eine Strukturformel:
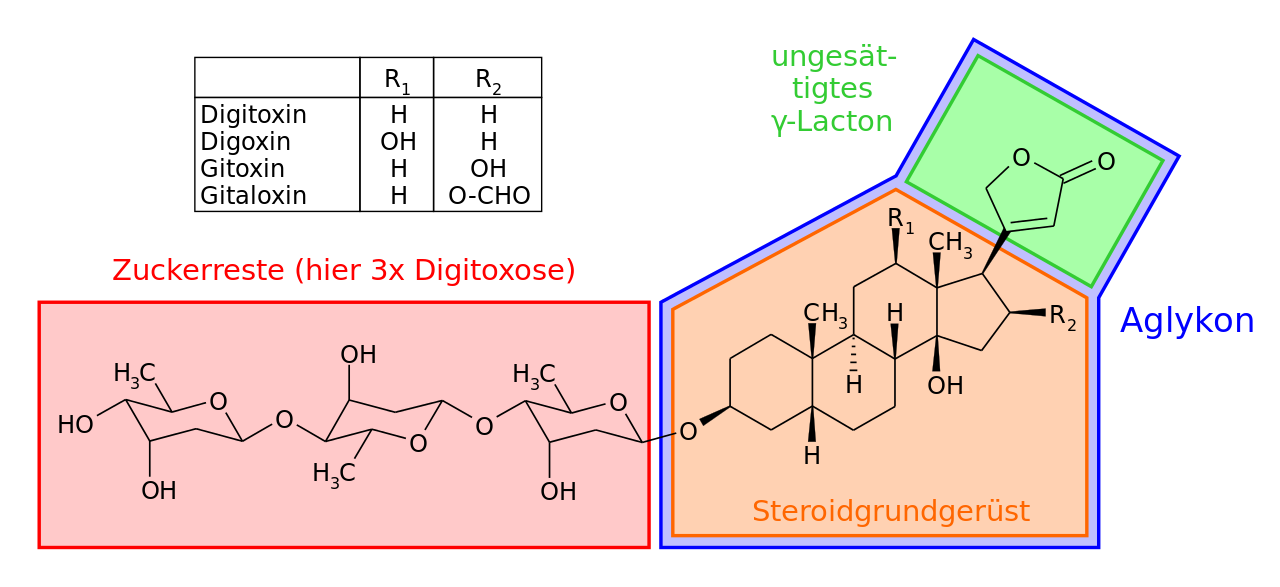
Struktur der herzwirksamen Steroide am Beispiel der Digitalisglykoside
Master Uegly, CC BY-SA 3.0, via Wikimedia Commons
Die Zuckerkomponente des Digitalis-Wirkstoffs wird aus drei Digitoxose-Monomeren gebildet. Über die C1-OH-Gruppe des "rechten" Monomers wird die Verbindung zu einem Steroidgerüst aufgenommen, das dann noch mit einem kleineren Lacton-Molekül verbunden ist. Dieses Digitalis-Glycosid ist übrigens ein Beispiel für O-Glycoside, denn der Zuckerrest ist über ein O-Atom mit der anderen Komponente verbunden.
Medizinische Anwendung
Zitat aus dem Wikipedia-Artikel "Roter Fingerhut":
"Die Wirkstoffe des Fingerhuts sind Herzglykoside, die heute überwiegend aus dem Wolligen Fingerhut gewonnen werden. Herzglykoside regen den geschwächten Herzmuskel an, sich wieder stärker zusammenzuziehen. Im therapeutischen Einsatz von Digitalis steht der die Herzfrequenz senkende Effekt von Digitalis immer mehr im Vordergrund gegenüber der Stärkung der Herzleistung. "
N-Glycoside
Bei N-Glycosiden ist der Zuckerrest über ein N-Atom mit der anderen Komponente verbunden. Ein klassisches Beispiel ist die Desoxyribonucleinsäure. Schauen wir uns DNA-Nucleotide einmal näher an.
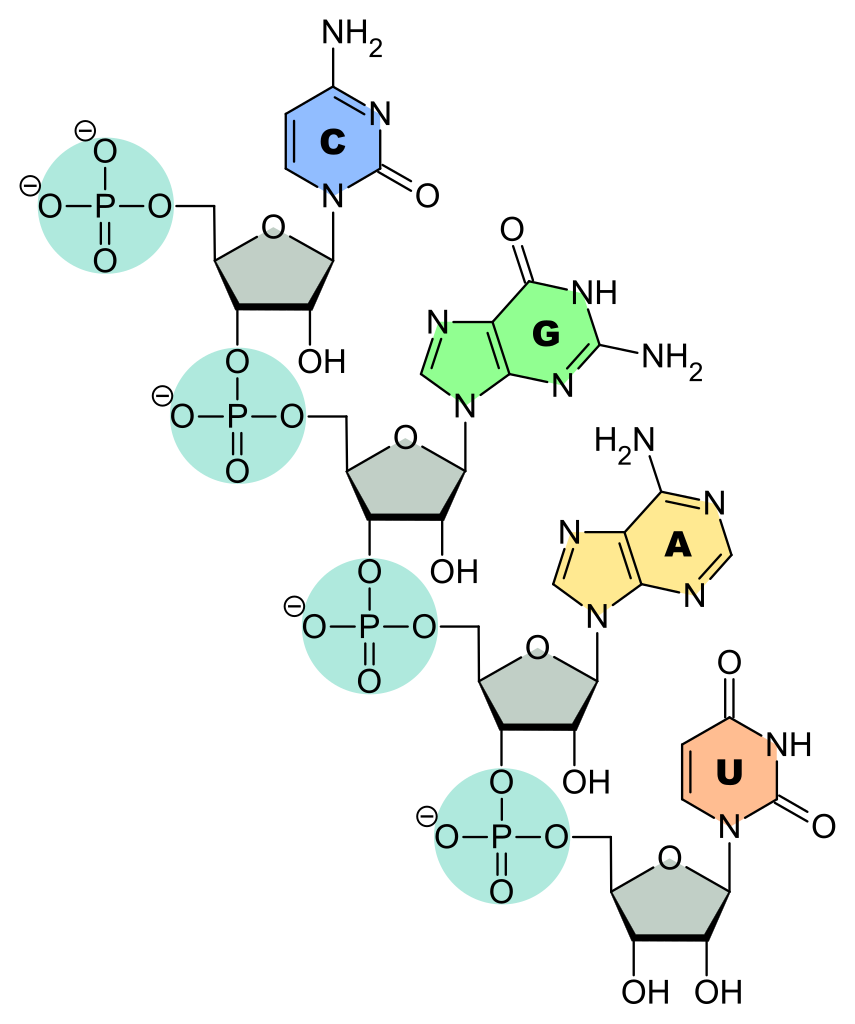
Vier Nukleotide mit je verschiedener Base (C, G, A, U) in N-glykosidischer Bindung
Sponk, Public domain, via Wikimedia Commons
Die Desoxyribose ist über ein N-Atom mit der jeweiligen Base verbunden.
S-Glycoside
Die Senföl-Glycoside sind die bekanntesten Beispiele für die S-Glycoside. Hier sehen wir die Strukturformel von Senföl, einem Glycosid, das vor allem in Kreuzblütlern wie dem Raps vorkommt:

Allgemeine Struktur der Senfölglycoside
Autor: Ulrich Helmich, Lizenz: Public domain
Es gibt über 120 verschiedene Senfölglycoside, die sich nur im Rest R unterscheiden. Glucose ist immer der Zucker in diesen Verbindungen. Die Glycoside sind pflanzeneigene Giftstoffe, die vor allem gegen Tierfraß helfen.
Medizinische Anwendung
Zitat aus dem Wikipedia-Artikel "Senfölglycoside":
"Senföle (z. B. Allylsenföl) werden therapeutisch als örtlich wirkende Hautreizmittel (Rubefacientia) eingesetzt. Sie wirken teilweise stark antibakteriell. Zubereitungen aus senfölhaltigen Pflanzen werden ebenfalls heilkundlich verwendet. Kapuzinerkresse etwa wirkt aufgrund ihres Gehaltes an Benzylsenföl bakteriostatisch (bei grampositiven und gramnegativen Bakterien sowie in vitro gegen multiresistente Staphylokokken), virustatisch (in vitro auch 90 Prozent Reduktion bei H1N1-Viren), antimykotisch und hyperämisierend."