Ein Bereich der Erdatmosphäre, in dem die Konzentration von Ozon O3 besonders hoch ist. Wie man auf der folgenden NASA-Graphik (Public domain) sieht, ist die Ozon-Konzentration in ca. 20 km Höhe am größten, also im unteren Bereich der Stratosphäre.
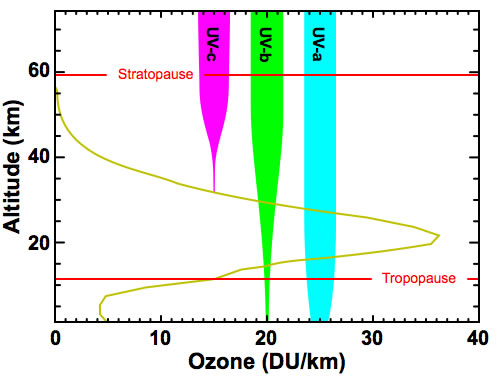
Absorption der UV-Strahlung durch die Ozonschicht (37 DU/km = 1013 Moleküle/cm3)
Quelle: Wikipedia, Artikel "Ozonschicht". Autor: NASA.
This file is in the public domain in the United States because it was solely created by NASA. NASA copyright policy states that "NASA material is not protected by copyright unless noted".
Die Ozonkonzentration in der Luft wird nicht, wie sonst üblich, in mol/l gemessen, sondern in DU/km. Unter DU versteht man die DOBSON-Einheit (engl. Dobson unit). Was man unter 1 DU versteht, wird in dem Wikipedia-Eintrag folgendermaßen erklärt:
Dabei gilt die Festlegung, dass eine reine Ozonschicht mit einer Dicke von 1 mm genau 100 DUs entspricht.
Das entspricht ungefähr 0,45 mmol/m2 oder 2,69 * 1020 Ozon-Moleküle/m2.
Wirkung der Ozonschicht
Das Vorhandensein der Ozonschicht ist für das Leben auf der Erde von enormen Vorteil, denn die Hauptwirkung des Ozons besteht darin, die von der Sonne her eindringende gefährliche UV-Strahlung zu absorbieren. Die sehr kurzwellige und damit energiereiche UV-c-Strahlung (im Bereich um 200 nm) wird von der Ozonschicht vollständig absorbiert, die etwas längerwellige UV-b-Strahlung (um 300 nm) wird zum größten Teil absorbiert; ein kleiner Teil gelangt auf den Erdboden. Die langwellige UV-a-Strahlung (um 350 nm) wird so gut wie nicht absorbiert, sie gelangt ungehindert zur Erdoberfläche.
UV-Strahlung verursacht bekanntlich Schäden in der Erbsubstanz, der DNA der Lebewesen, die nur teilweise durch zelluläre Reparatursysteme beseitigt werden können. Mutationen und Hautkrebs sind die folgenreichsten Auswirkungen solcher UV-Strahlung.
Absorption von UV-c durch Sauerstoff
Sauerstoff-Moleküle (O2) werden durch energiereiches UV-Licht in Sauerstoff-Atome gespalten. Die Wellenlänge der Strahlung muss allerdings unter 240 nm liegen, sonst ist das Licht nicht energiereich genug für diese Photolyse.
Je eines dieser Sauerstoff-Radikale bindet sich nun an ein Sauerstoff-Molekül, und dabei entsteht das Ozon O3.
Es ist also nicht so, dass das Ozon das UV-Licht absorbiert, sondern der Luftsauerstoff absorbiert das UV-Licht, und dabei entsteht das Ozon.
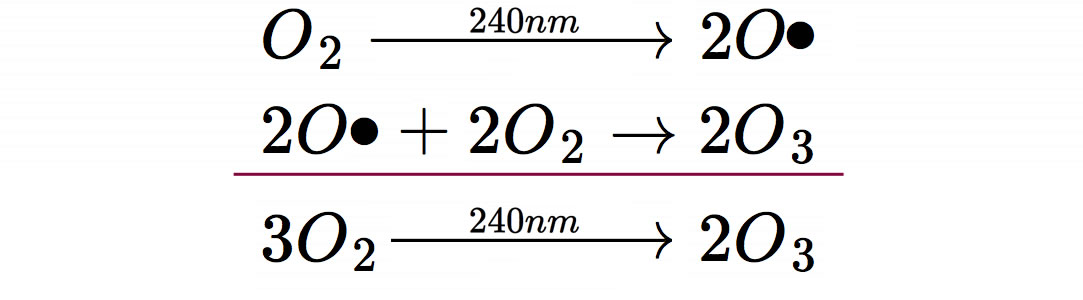
Insgesamt bilden sich also aus drei Sauerstoff-Molekülen durch Absorption von <240nm-Strahlung zwei Ozon-Moleküle.
Absorption von UV-b durch Ozon
Das so gebildete Ozon absorbiert jetzt die etwas längerwellige UV-b-Strahlung, die im Bereich um 300 nm liegt. Ein Ozon-Molekül spaltet dabei ein Sauerstoff-Atom ab, es entsteht dann ein Sauerstoff-Molekül. Das Sauerstoff-Atom reagiert dann aber gleich wieder mit einem Sauerstoff-Molekül zu neuem Ozon, so dass die Ozon-Menge im Grunde konstant bleibt.

Ein "Kettenabbruch" kann stattfinden, wenn entweder zwei Sauerstoff-Atome aufeinander stoßen, oder wenn ein Sauerstoff-Atom auf ein Ozon-Molekül trifft. Dann bilden sich zwei Sauerstoff-Moleküle.