Im Prinzip muss man unterscheiden zwischen der Absorption von Materie und der Absorption von Strahlung.
Absorption von Materie
Hierunter versteht man die gleichmäßige Verteilung eines Stoffes in einem anderem Stoff [1]. Auch Lösungvorgänge wie zum Beispiel das Lösen eines Feststoffes oder Gases in einer Flüssigkeit werden als Absorption bezeichnet [3]. Nicht zu verwechseln ist der Vorgang der Absorption mit dem Vorgang der Adsorption.
Bei der Adsorption wird ein Stoff nicht von einem anderen Stoff aufgenommen, sondern er lagert sich nur an der Oberfläche dieses Stoffes an. Aktivkohle ist hierfür ein gutes Beispiel; wenn Flüssigkeiten durch einen Aktivkohlefilter laufen, werden bestimmte Teilchen nicht absorbiert, sondern lagern sich lediglich an die Oberfläche der Aktivkohleteilchen an.
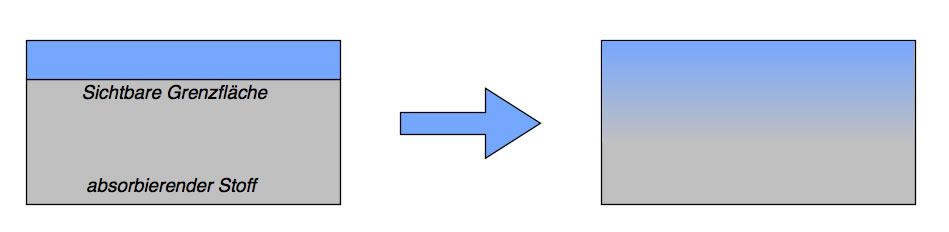
Der Vorgang der Absorption
Autor: Ulrich Helmich 2016, Lizenz: Public domain.
Bei der Absorption verschwindet die sichtbare Grenzfläche zwischen den beiden Stoffen, und das Volumen des absorbierenden Stoffes (grau gezeichnet) nimmt durch die Aufnahme des absorbierten Stoffes zu. Bei einer Adsorption würde die Grenzfläche im Prinzip erhalten bleiben, und das Volumen des adsorbierenden Stoffes würde sich nicht verändern.
Absorption von Strahlung
Wenn elektromagnetische Strahlung wie beispielsweise Licht beim Durchgang durch einen Stoff abgeschwächt wird, spricht man ebenfalls von Absorption. Dabei wird ein Teil der Strahlung in eine andere Energieform umgewandelt, zum Beispiel Wärmeenergie oder Anregungsenergie [2].
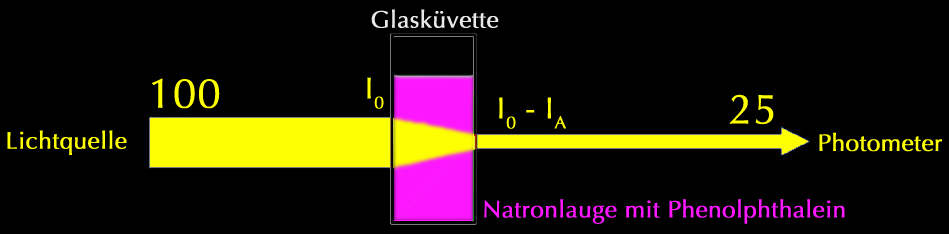
Absorption von gelbem Licht durch den Farbstoff Phenolphthalein
Autor: Ulrich Helmich 2016, Lizenz: Public domain.
Der Begriff Absorptionsvermögen beschreibt, welcher Prozentsatz der Strahlung absorbiert wurde. Im obigen Beispiel hätte das Absorptionsvermögen also den Wert 0,75 bzw. 75%.
Weitere Einzelheiten zu Absorption, Absorptionsspektren etc. siehe die große Abteilung "Farbstoffchemie" auf dieser Homepage und speziell die Seite über Absorptionsspektren.
Quellen:
- RÖMPPs Chemie-Lexikon, 7. Auflage 1972
- Spektrum Lexikon der Chemie, Stichwort "Absorption"
- Wikipedia, Artikel "Absorption (Chemie)"