Dieses Thema ist eng verwandt mit dem Säure-Base-Konzept von BRÖNSTED. Nach BRÖNSTED sind Säuren ja Protonendonatoren, während Basen Protonenakzeptoren sind.
Nun kann eine Säure ihr Proton aber nur dann abgeben, wenn ein Protonenakzeptor in der Nähe ist, der das Proton aufnimmt. Umgekehrt kann eine Base nur dann ein Proton aufnehmen, wenn eine Säure in der Nähe ist, die ihr Proton abgibt.
Säuren und Basen gehören also zusammen, alleine können sie zwar vorkommen, aber dann keine Säure-Base-Reaktion eingehen.
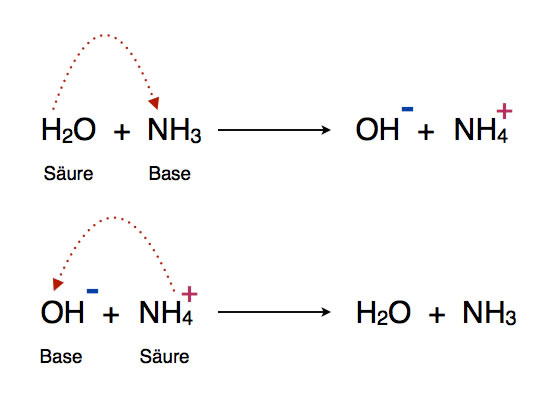
Schauen Sie sich dieses Bild mal näher an. Oben sieht man, wie ein Wasser-Molekül ein Proton an ein Ammoniak-Molekül abgibt. Wasser-Moleküle sind hier die Säuren, Ammoniak-Moleiüle die Basen.
Im unteren Teil des Bildes sieht man die Rückreaktion. Die Ammonium-Ionen können wieder ein Proton an die Hydroxid-Ionen abgeben, dabei entstehen Wasser-Moleküle und Ammoniak-Moleküle. Hier sind die Ammonium-Ionen die Säuren, während die Hydroxid-Ionen die Basen sind.
Das folgende Bild findet man in vielen Schulbüchern:
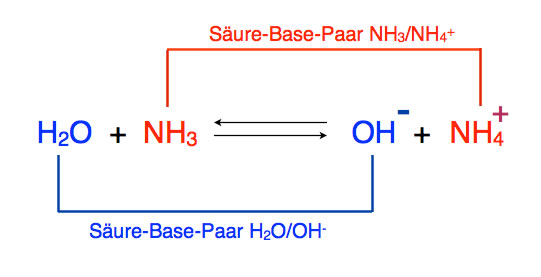
Die Zeichnung verdeutlicht, dass aus der Säure H2O durch die Protonenabgabe die Base OH- wird. Umgekehrt kann bei der Rückreaktion aus der Base OH- wieder die Säure H2O werden. H2O und OH- bilden zusammen das Säure-Base-Paar H2O/OH-.
Das Gleiche gilt für das Säure-Base-Paar NH3/NH4+. Aus der Base NH3 wird durch Aufnahme eines Protons die Säure NH4+. Wenn diese das Proton wieder abgibt, bildet sich die Base NH3.
Solche zusammengehörigen Säure/Base-Paare wie H2O/OH- und NH4+/NH3 bezeichnet man als korrespondierende Säure-Base-Paare, oft auch als konjugierte Säure-Base-Paare. Beide Begriffe bedeuten im Grunde das Gleiche. Das Wort "konjugiert" betont dabei den Aspekt, dass die beiden Teilchen als Paar zusammenwirken (Paar-Aspekt), während das Wort "korrespondierend" den Aspekt betont, dass das eine Teilchen Protonen mit dem anderen Teilchen austauscht (Austausch-Aspekt).
Verbindungen wie Wasser können sowohl als Säure wie auch als Base auftreten, je nachdem, welche Eigenschaft der Reaktionspartner hat. Mit Ammoniak reagiert Wasser als Säure, mit Chlorwasserstoff dagegen als Base. Neben dem H2O/OH--Paar gibt es also auch noch das H3O+/H2O-Paar.
Abitur NRW
In den meisten Abituraufgaben, die irgendetwas mit Säuren oder Basen zu tun haben, müssen die Schüler in der Lage sein, solche Säure-Base-Paare in den Reaktionen bzw. in den Reaktionsgleichungen zu identifizieren und zu benennen.