Aquaporine sind integrale Membranproteine mit einer hydrophilen Pore, durch die Wasser-Moleküle die Zellmembran passieren können. Aquaporine kommen nicht nur in Eukaryotenzellen vor, sondern in den Membranen aller Lebewesen, also auch in den Zellmembranen von Bakterien und Archaeen.
Man unterteilt die Aquaporine in zwei Klassen: Gewöhnliche Aquaporine und Aquaglyceroproteine. Die gewöhnlichen Aquaporine leiten nur Wasser-Moleküle, während die Aquaglyceroproteine auch andere kleinere Moleküle durch die Membran lassen, zum Beispiel Glycerin oder Harnstoff [1].
Struktur
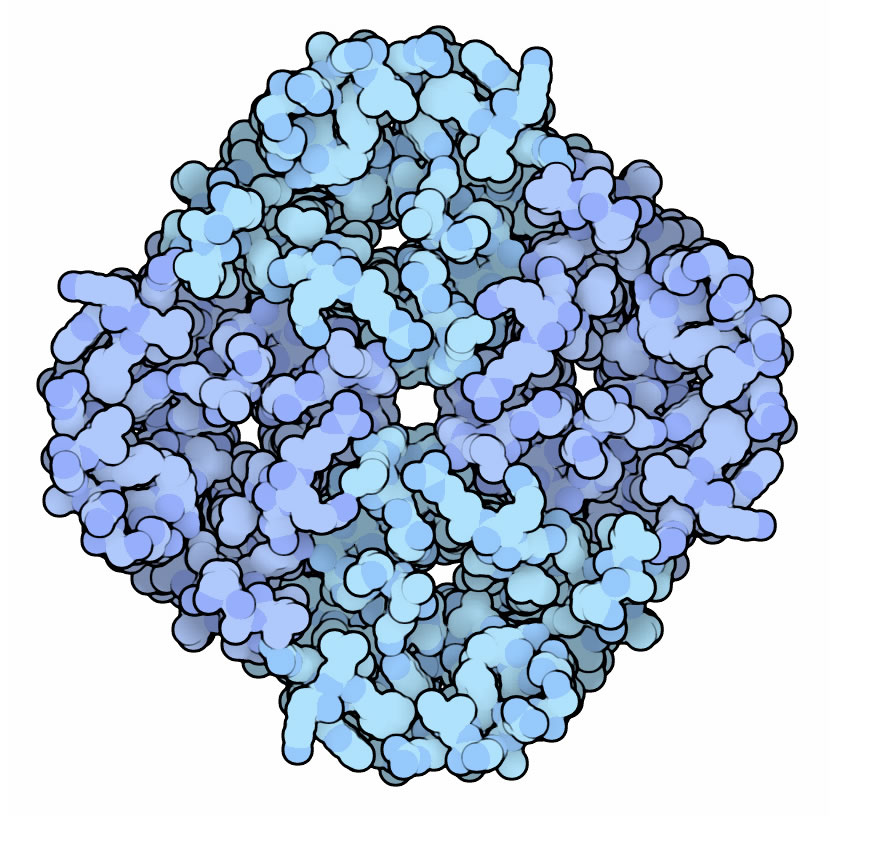
Ein Aquaporin-Molekül in der Aufsichtc
Quelle: engl. Wikipedia, Artikel "Aquaporin", Autor: David Goodsell, Lizenz: Creative Commons Attribution 3.0 Unported license.
Hier sehen wir ein Aquaporin-Molekül in der Aufsicht. Die Zeichnung von David Goodsell ist sehr eindrucksvoll, die Farbwahl hätte aber etwas besser sein können. Man kann nur erahnen, dass das Aquaporin aus vier Untereinheiten besteht, von denen jede eine kleine Wasserpore besitzt. Ich habe mal versucht, das ganze etwas deutlicher darzustellen:
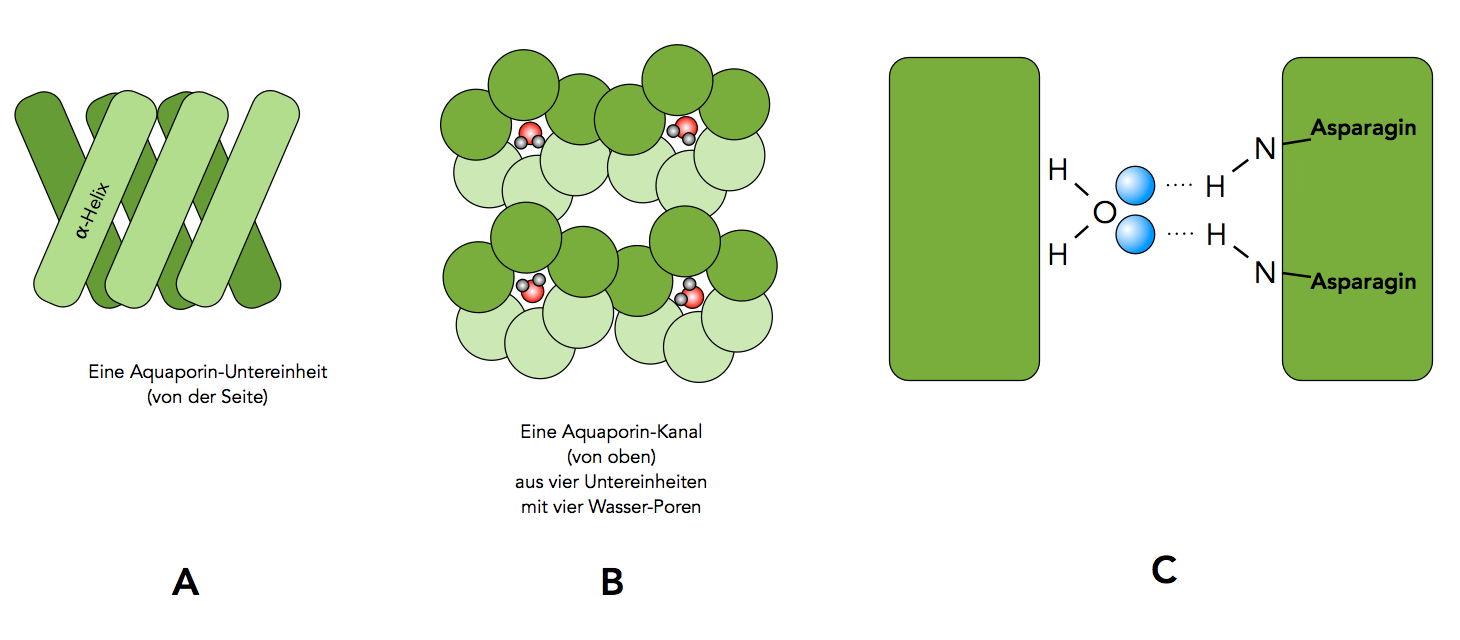
Aquaporine in verschiedenen Ansichten. Mit Doppelklick Ansicht vergrößern.
Autor: Ulrich Helmich 2021, Lizenz: Public domain
In Bild A sieht man, dass eine Aquaporin-Untereinheit aus sechs alpha-Helices besteht, die die Membran durchziehen. Die Helices sind in der seitlichen Ansicht nur schematisch angedeutet, drei Helices befinden sich im Vordergrund, drei im Hintergrund der Skizze.
In Bild B sieht man ein Aquaporin in der Aufsicht, also von oben. Man sieht die vier Untereinheiten, jede aus sieben Helices bestehend. Jede Untereinheit hat eine kleine Pore, in die genau ein Wasser-Molekül passt. Eigenartigerweise dient die größere Zentrale Pore nicht dem Wasser-Transport.
Wassertransport
In Bild C findet man die Antwort auf die noch gar nicht gestellte Frage, wieso ein Aquaporin eigentlich keine Protonen leitet. In jeder wässrigen Lösung findet man Protonen, selbst in einer starken Lauge mit dem pH-Wert 14 beträgt die Protonenkonzentration noch 10-14 mol/l. Bei pH-Werten, wie sie in der Zelle herrschen, ist die Protonenkonzentration um den Faktor 10 Millionen größer. Die Protonen einer wässrigen Lösung bewegen sich allerding nicht wie normale Ionen, also wie Na+ oder SO42-, sondern über einen viel raffinierteren Mechanismus, der als Grotthus-Mechanismus bezeichnet wird. In meinem Chemie-Lexikon finden Sie nähere Informationen zu diesem Transportmechanismus.
Das Wasser-Molekül in Bild C besitzt zwei freie Elektronenpaare, die durch die kleinen blauen Kügelchen angedeutet werden. Zwei Asparagin-Reste in einer der alpha-Helices bilden jetzt Wasserstoffbrücken-Bindungen mit diesen beiden freien Elektronenpaaren. Dadurch hat das Wasser-Molekül kein freies Elektronenpaar mehr übrig, mit dem es ein Proton nach dem Grotthus-Mechanismus "einschleppen" könnte [2].
Allerdings wird dieser Protonen-Vermeidungs-Mechanismus in der Wissenschaft noch diskutiert; das letzte Wort ist hier noch nicht gesprochen [1].
Auch in Pflanzenzellen kommen Aquaporine vor, ein Aquaporin-Typ erleichter im Blattgewebe das Eindringen von CO2, was ja für die Photosynthese wichtig ist [1]. Die Membran der Vakuole, der Tonopast, enthält ebenfalls Aquaporine.
Vorkommen
Aquaporine kommen hauptsächlich in Geweben vor, in denen viel Wasser benötigt oder freigesetzt wird, z.B. in der Niere (Rückgewinnung von Wasser aus dem Harn), in der Gallenblase, in der Augenlinse, im Gehirn und so weiter.
Quellen:
- Wikipedia, Artikel "Aquaporine"
- Alberts, Bruce et al. Molekularbiologie der Zelle, 6. Auflage, Weinheim 2017.